Семь комменсальных бактерий защитили кишечник мышей от колонизации патогеном после курса антибиотиков
При дисбиозе, вызванном терапией антибиотиками, кишечник могут колонизировать ванкомицинрезистентные энтерококки, приводя к тяжелым инфекциям, порой переходящим в системную форму. Группа ученых из Франции, используя математическое моделирование, собрала консорциум из семи комменсальных штаммов — после курса антибиотиков он защищал кишечник мышей от колонизации энтерококком и ускорял восстановление микробиоты. Эффект достигался за счет повышения видового разнообразия и воздействия на метаболизм, в том числе усиления выработки короткоцепочечных жирных кислот.
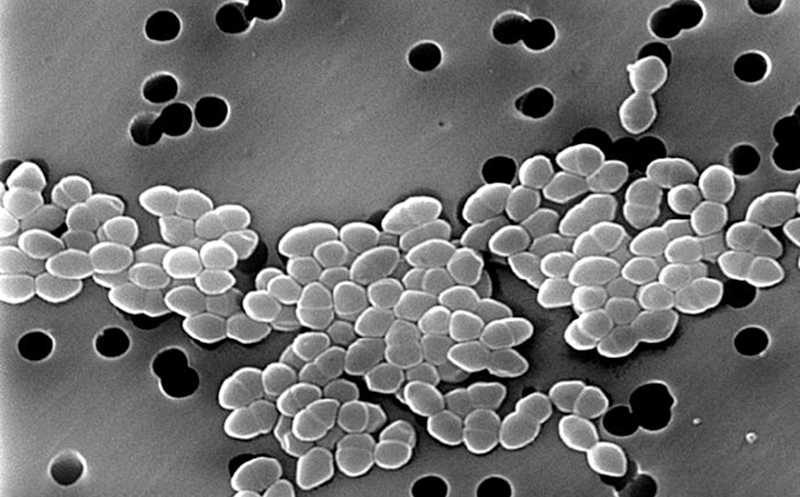
Ванкомицинрезистентный энтерококк (VRE) представляет собой серьезную клиническую проблему, особенно для иммунокомпрометированных пациентов. Эти бактерии способны колонизировать кишечник после антибиотикотерапии и затем вызывать системные инфекции. В норме кишечная микробиота обеспечивает барьер против таких патогенов, но при дисбактериозе он ослабевает. Для восстановления барьерной функции микробиоты могут применяться фекальные трансплантации или консорциумы живых комменсалов. Однако такие вмешательства требует рационального подбора штаммов, обладающих защитным эффектом. Группа ученых из Франции задалась целью выявить бактериальный консорциум, способный восстанавливать микробиоту и подавлять VRE, а также оценить его эффективность.
Исследование проводили на мышах — у них индуцировали дисбиоз трехдневным курсом клиндамицина, а затем инфицировали VRE. Параллельно некоторым животным вводили Mix7 — смесь из семи ключевых комменсальных бактерий, предварительно отобранных с помощью математического моделирования. Ученые провели регрессионный анализ, чтобы оценить, какие виды бактерий среди всех кандидатов ассоциированы со снижением доли VRE. Видовой состав определяли путем секвенирования генов 16s рРНК. На основе этого анализа авторы отобрали 15 видов-кандидатов, потенциально вовлеченных в защитный барьер микробиоты. Из них 6 штаммов получили в чистой культуре, а вместе с седьмым штаммом (Lachnospiraceae bacterium), добавленным для усиления эффекта, был сформирован консорциум Mix7.
Изменения в микробиоте мышей отслеживали при помощи 16S рРНК секвенирования, метаболомики (в том числе определения короткоцепочечных жирных кислот и ЯМР-анализа), а также проверки наличия VRE в фекалиях. Авторы оценивали как индивидуальную, так и кооперативную роль отдельных штаммов.
Итоговый консорциум включал четыре штамма из семейства Lachnospiraceae и по одному — из семейств Muribaculaceae, Ruminococcaceae и Lactobacillaceae. Он ускорял восстановление кишечной микробиоты (альфа- и бета-разнообразие) и снижал содержание VRE в фекалиях, особенно на пике колонизации (дни 4–7) и на финальных этапах (день 21). Однако наблюдалась индивидуальная вариабельность ответа: доля VRE снижалась не у всех мышей. У ответивших микробиота восстанавливалась быстрее, особенно за счет представителей Bacteroidota, и сопровождалась увеличением продукции SCFA (ацетат, бутират).
Ключевую роль играл штамм Muribaculum intestinale: его исключение из смеси лишало консорциум защитного действия, но сам по себе этот штамм был неэффективен. Интересно, что супернатанты от штаммов Mix7 не ингибировали рост VRE in vitro — это говорит об опосредованных механизмах действия. Кроме того, анализ показал, что большинство штаммов Mix7 имеют функциональные аналоги в человеческой микробиоте, что подтверждает возможность применения результатов на модели человека.
Таким образом, исследование демонстрирует, что правильно подобранный консорциум из комменсальных бактерий способен эффективно восстанавливать кишечную микробиоту после антибиотикотерапии и тормозить колонизацию кишечника VRE. Авторы работы заключили, что эффект консорциума зависит от исходного состояния микробиоты и реализуется через восстановление микробного и метаболического баланса, а не через прямое ингибирование VRE. Эти данные могут лечь в основу персонализированных живых биотерапевтических продуктов на основе комменсальных бактерий для профилактики и лечения инфекций, вызванных ванкомицинрезистентным энтерококком.
Кодирующий бактериоцин энтерококк вытеснил конкурентов в отдельной больнице и в мире


 Меню
Меню





 Все темы
Все темы




 0
0