Сердце рыбок данио регенерирует после инфаркта
Способность рыбки данио-рерио восстанавливать без рубцевания сердечную ткань после инфаркта давно известна. Исследователи из Германии выяснили, какие клетки и сигнальные пути в этом участвуют. Так, фибробласты из эндокарда и эпикарда начинают экспрессировать прорегенеративные гены, а периваскулярные клетки отвечают за восстановление сосудов.
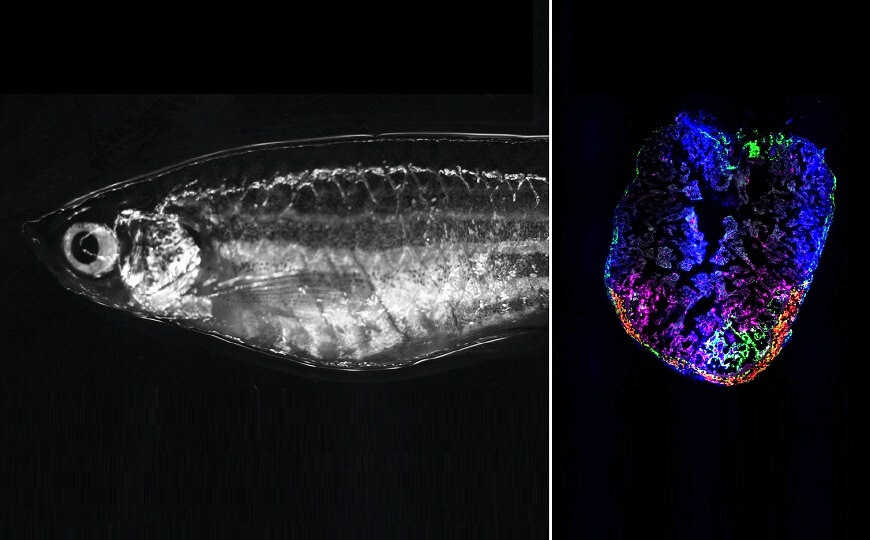
Взрослая рыбка данио и ее сердце через неделю после криотравмы. Транзиторно активированные фибробласты локализуются в области повреждения.
Credit:
Panáková Lab, MDC | Пресс-релиз
Повреждение кардиомиоцитов, вызванное инфарктом или другой патологией, у человека и других млекопитающих приводит к тому, что клетки отмирают и на их месте образуется рубцовая ткань, не способная к сокращению. Свою функцию сердце продолжает выполнять за счет остальных клеток миокарда, если только повреждение не очень обширное.
Некоторым позвоночным, например, рыбкам данио, повезло больше: их сердечная ткань может восстанавливаться. Ученые из Германии смоделировали инфаркт миокарда в сердцах таких рыбок и с помощью транскриптомики единичных клеток отследили регенерацию кардиомиоцитов.
Сначала исследователи на несколько секунд поднесли холодную иглу к сердцу рыбки данио — это вызывает воспалительную реакцию, за которой следует транзиторное (временное) рубцевание: фибробласты делятся и занимают место погибших кардиомиоцитов. Однако сердце скоро приступает к регенерации, кардиомиоциты дедифференцируются и начинают делиться. Эти процессы изучали и ранее, но сигнальные взаимодействия и типы клеток, которые в этом участвуют, никто еще не исследовал в деталях.
С помощью геномики единичных клеток ученые сравнили поврежденные и здоровые сердца рыб, чтобы понять, существуют ли специфические клетки, отвечающие за восстановление. Помимо зрелых кардиомиоцитов, они обнаружили небольшой кластер тех самых пролиферирующих кардиомиоцитов, которые экспрессировали гены, связанные с развитием: ttn.1, ttn.2, bves и synpo2lb. Кроме этого, в поврежденных сердцах ученые идентифицировали три новых кластера прорегенеративных фибробластов, которые после повреждения временно перешли в активированное состояние. Эти фибробласты экспрессировали ряд дополнительных генов, кодирующих важные для регенерации белки, например, коллаген-12.
Когда ученые «отключили» активированные фибробласты, которые экспрессировали коллаген 12, регенерация прекратилась. Вероятно, именно фибробласты и отвечают за восстановление. «В конце концов, они образуются прямо на месте повреждения», — говорит один из авторов профессор Ян Филипп Юнкер.
Чтобы определить, откуда произошли эти активированные фибробласты, исследователи использовали метод LINNAEUS, разработанный лабораторией Юнкера в 2018 году. LINNAEUS работает с «генетическими шрамами» — это своего рода штрихкод, отслеживающий происхождении каждой клетки. «Мы создаем этот штрихкод с помощью генетических ножниц CRISPR-Cas9. Если после повреждения две клетки имеют одинаковый штрих-код, это означает, что они связаны» — объясняет Юнкер.
Оказалось, что фибробласты происходят из эпикарда и эндокарда — внешнего и внутреннего слоя сердечной стенки. Клетки, продуцирующие коллаген-12, были обнаружены исключительно в эпикарде.
Ученые также заметили в регенерирующих сердцах рыб специфическое взаимодействие между периваскулярными клетками и эндотелием кровеносных сосудов — посредством передачи сигналов хемокинов Cxcl12b-Cxcr4a. Периваскулярные клетки регулируют образования кровеносных сосудов, и, вероятнее всего, новые сосуды в восстановленной сердечной ткани формируются благодаря им.
Ингибирование сигнального пути Wnt/β-катенин привело к снижению уровней периваскулярных клеток и всех эндокардиальных фибробластов, а количество фибробластов, вырабатывающих коллаген, не изменилось. Однако регенерация сердца при этом замедлилась — возможно, из-за снижения реваскуляризации.
Пока не ясно, почему такая регенерация недоступна млекопитающим: не хватает ли им сигналов фибробластов либо способности их считывать. Имитация сигналов возможна, и это могло бы стать новой терапевтической стратегией. А вот заставить клетки считывать сигналы — сложнее.
PCR.NEWS о регенерации конечности шпорцевой лягушки в носимом биореакторе. В ней тоже участвует сигнальный путь Wnt/β-катенин.
Источники
Hu B. et al. Origin and function of activated fibroblast states during zebrafish heart regeneration // Nature Genetics, published July 21, 2022, DOI: 10.1038/s41588-022-01129-5
Цитаты по пресс-релизу

 Меню
Меню





 Все темы
Все темы




 0
0











