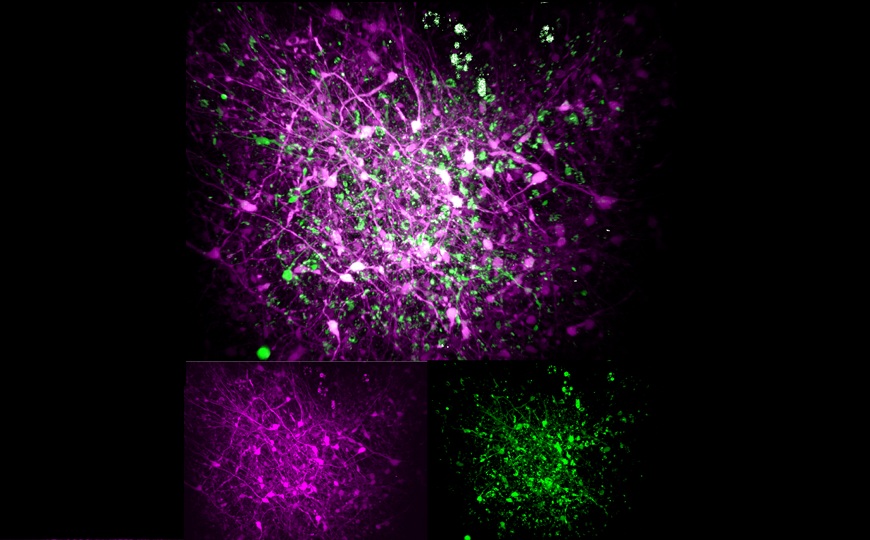
Синдром сухого глаза может быть связан с нарушениями аутофагии
Нарушения в работе слезных желез могут приводить к синдрому сухого глаза, который повышает риск повреждений роговицы и глазных инфекций. Авторы статьи в Stem Cell Reports вырастили из эмбриональных стволовых клеток человека органоиды слезных желез и показали, что при нарушениях аутофагии в них снижается способность вырабатывать компоненты слезы. Это связано с аномальным накоплением фактора транскрипции PAX6, регулирующего развитие глаз. В норме он подвергается деградации за счет аутофагии, а патологическое усиление его сигнала нарушает нормальное развитие слезной железы и ведет к гибели ее клеток. В качестве терапевтического средства ученые предложили использовать никотинамидмононуклеотид — они показали, что это соединение, хотя и не влияет на аутофагию, способно компенсировать вредные последствия ее дефицита.
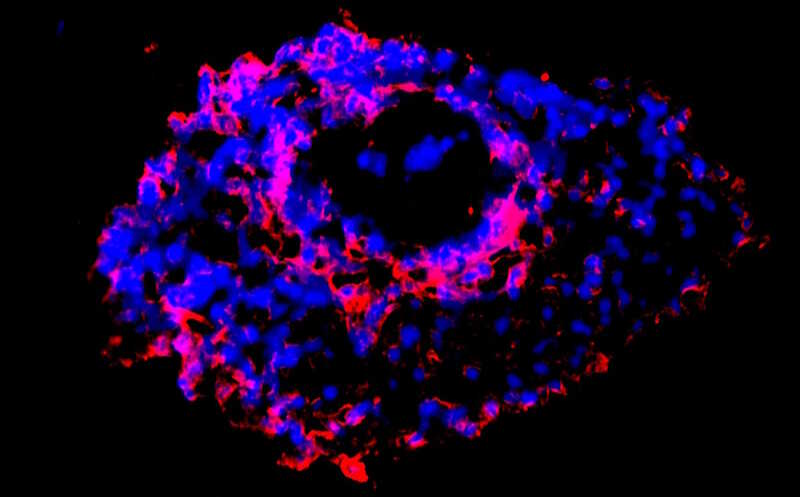
При нарушении аутофагии в органоиде слезной железы усиливается гибель клеток, маркером которой служит каспаза-3 (окрашена красным).
Credit:
Gamze Kocak in Sovan Sarkar lab at the University of Birmingham, UK |
пресс-релиз
Слезные железы отвечают за выработку компонентов слезной пленки, которая необходима для поддержания влажности и гомеостаза поверхности глаза. Нарушение их функционирования связано с синдромом сухого глаза, для которого сейчас существует только симптоматическое лечение. Один из процессов, ключевых для развития и работы многих желез, — это аутофагия, однако ее роль именно в слезных железах до сих пор не была охарактеризована. Авторы статьи в Stem Cell Reports показали на органоидах слезных желез, что аутофагия необходима для их функции, а также предложили потенциальное терапевтическое вмешательство для синдрома сухого глаза.
Для получения органоидов ученые использовали эмбриональные стволовые клетки человека (hESC). Аутофагию в них нарушили с помощью делеции в гене ATG5 — уже показано, что потеря его функции препятствует образованию аутофагосом. Пролиферативная способность ATG5−/− hESC, оцененная по уровню маркера пролиферации Ki-67, была сопоставима с таковой у клеток дикого типа.
Затем, адаптировав протокол дифференцировки органоидов слезных желез из плюрипотентных стволовых клеток, авторы получили самособирающиеся органоиды из ATG5+/+ и ATG5−/− hESC. Они содержали четыре слоя клеток-предшественников различных линий. Иммуноокрашивание шестинедельных органоидов подтвердило их многозональную структуру, однако зоны 3 и 4 (два наружных слоя) были менее организованы в органоидах с нокаутом ATG5.
Слезная железа состоит из трех основных типов клеток: ацинарных, протоковых и миоэпителиальных. Анализ на маркеры этих клеток (цитокератин 5, цитокератин 19 и гладкомышечный α-актин соответственно) и на дополнительные маркеры ацинарных/протоковых показал, что их экспрессия была снижена при нокауте ATG5. В нокаутных органоидах также экспрессировалось меньше CD44 — маркера железистых клеток. Аналогичные изменения наблюдались в органоидах дикого типа после обработки фармакологическими ингибиторами аутофагии.
Секвенирование тотальной РНК выявило четкие транскриптомные различия между ATG5+/+ и ATG5−/− органоидами. Среди 441 дифференциально экспрессируемого гена авторы обнаружили 94, которые были связаны с развитием глаз, и 82, участвующих в морфогенезе и дифференцировке. Экспрессия этих генов была значительно снижена в отсутствие аутофагии.
Далее авторы оценили влияние нарушений аутофагии на секреторную функцию органоидов. Слезные железы секретируют белки слезной жидкости лактоферрин, липокалин-2 и лизоцим, а также выделяют воду с помощью белка водного канала аквапорина-5 (AQP5). Экспрессия генов лактоферрина, липокалина и AQP5 была снижена при нокауте ATG5. Кроме того, в них была ниже активность фермента N-ацетил-β-d-глюкозаминидазы (NAG), который участвует в секреции лизоцима. Доля Ki-67+ клеток, напротив, была выше, чем в органоидах дикого типа, что свидетельствует об усилении пролиферации.
Предыдущие исследования на мышах показали, что транскрипционный фактор Pax6 необходим для развития слезных желез и нормальной выработки слез. Он экспрессировался в органоидах во время дифференцировки, причем на генном уровне его экспрессия была снижена при нокауте ATG5. А вот белок PAX6 существенно накапливался в нокаутных органоидах, предположительно, из-за нарушенной деградации. Это навело авторов на предположение, что PAX6 в норме разрушается путем аутофагии.
Поскольку накопление PAX6 коррелировало с нарушениями дифференцировки органоидов слезных желез, авторы решили проверить, связано ли это с его функцией. Проанализировав экспрессию генов-мишеней PAX6 — SOX2, FOXC1, TGFB2 и BMP4, — они обнаружили, что в органоидах с нарушенной аутофагией уровень первых трех генов возрастал, а оставшегося снижался. Это означает, что накопление PAX6 при дефиците аутофагии приводит к функциональному дисбалансу в его сигналинге.
Следующим шагом стал поиск фармакологических вмешательств, которые могли бы восстановить фенотип органоидов при дефиците ATG5. Индуцировать аутофагию в таких органоидах невозможно, и авторы выбрали два соединения, которые могли бы повлиять на нижележащие пути.
Одно из них — никотинамидмононуклеотид (NMN) — биодоступный предшественник NAD+. Уже было показано, что неспособность к аутофагии приводит к гибели клеток из-за истощения уровней NAD+ и NADH, и авторы предположили, что NMN сможет это предотвратить. Другое соединение — мелатонин, который вырабатывается в различных тканях глаза, включая слезные железы.
Оба соединения повышали экспрессию липокалина-2 и активность NAG в органоидах с нокаутом ATG5, что свидетельствует об улучшении секреторной функции. Однако на фенотипы, связанные непосредственно с аутофагией, влиял только NMN. Он уменьшал количество агресом — скоплений белковых агрегатов — и снижал гибель клеток до уровней, сопоставимых с диким типом. Кроме того, NMN ограничивал накопление PAX6 в отсутствие аутофагии, тогда как мелатонин не оказывал подобного эффекта.
Авторы предположили, что механизм, лежащий в основе влияния NMN на PAX6, может быть связан с гомеостазом митохондрий, и проверили эту гипотезу. Они показали, что это соединение снижает избыточную активность сиртуина 1 (SIRT1) — другой мишени аутофагии и одного из ключевых белков, регулирующих гомеостаз митохондрий.
Таким образом, недостаток аутофагии в клетках слезных желез может нарушать их развитие и секреторные функции. Это связано с аномальным накоплением PAX6 — ключевого фактора транскрипции для развития мозга и глаз. Однако на фенотип, вызванный аутофагией, можно воздействовать фармакологически — с помощью никотинамидмононуклеотида. Авторы рассчитывают, что их работа ляжет в основу создания средств для терапии синдрома сухого глаза.
Крупные нейроны при БАС погибают первыми из-за перегрузки защитных систем деградации


 Меню
Меню





 Все темы
Все темы



 0
0