Составлена первая карта боли на уровне белков
Для разработки методов лечения хронической боли, от которой страдает около 20% населения, важно понимать молекулярные механизмы этой патологии. Авторы статьи в Nature Communications составили первую протеомную карту ноцицепторов — сенсорных нейронов, обеспечивающих восприятие и передачу болевого сигнала. С помощью глубокой визуальной протеомики ученые охарактеризовали различные подтипы ноцицепторов мыши. Также они показали, что в механической сенсибилизации, при которой нервная клетка начинает реагировать на безвредный стимул как на болевой сигнал, может участвовать гликозилтрансфераза B3GNT2, однако ее роль требует дальнейшего изучения.
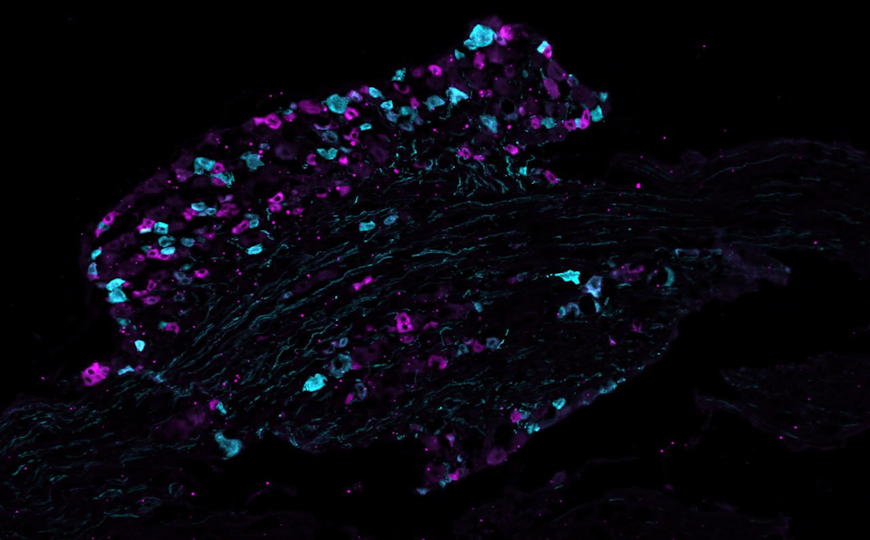
Различные субпопуляции ноцицепторов дорсального корешкового ганглия мыши.
Credit:
© Sampurna Chakrabarti, Max Delbrück Center |
пресс-релиз
Каждый пятый человек в мире страдает от хронической боли, и далеко не всем пациентам достаточно помогают существующие обезболивающие препараты. Для разработки новых терапевтических подходов необходимо учитывать молекулярные механизмы патологической боли. «Прежде всего мы должны точно понять, как сенсорные нервные клетки вызывают боль на молекулярном уровне — иными словами, какие белки участвуют в этом процессе», — объясняет профессор Гэри Левин, один из авторов работы и руководитель лаборатории молекулярной физиологии соматосенсорного восприятия в Центре имени Макса Дельбрюка (Берлин, Германия). И если секвенирование РНК отдельных клеток сенсорных нейронов уже выявило молекулярную основу их разнообразия, то на протеомном уровне таких данных недостает. Авторы статьи в Nature Communications составили первую протеомную карту сенсорных нейронов, участвующих в передаче болевого сигнала.
В культуре многие, но не все сенсорные нейроны обладают механочувствительностью. Электрофизиологические исследования методом пэтч-кламп на нейронах мыши показали, что почти все крупные (более 30 мкм в диаметре) сенсорные нейроны отвечают токами на механический стимул. Такие клетки обладают характеристиками механорецепторов. Более мелкие (до 30 мкм) сенсорные нейроны характеризуются более медленной кинетикой и сниженной частотой активации в ответ на механическое воздействие. Ученые обработали культуру нейронов, полученных из дорсальных корешковых ганглиев мыши, флуоресцентно меченным изолектином B4 (IB4) — он связывается с поверхностью непептидергических ноцицепторов. Частота токов в ответ на механический стимул — давление на клеточную мембрану — была намного ниже в IB4+, чем в IB4–-ноцицепторах.
Исследователи проанализировали протеом отдельных помеченных ноцицепторов мыши — пептидергических и непептидергических, — а также механорецепторов, в норме не передающих болевой сигнал. Они использовали глубокую визуальную протеомику — метод сочетает ИИ-анализ изображений, автоматическую лазерную микродиссекцию и высокочувствительную масс-спектрометрию. Протеомные данные для каждого подтипа были получены из 30–50 помеченных клеток, и метод позволил количественно определять до трех тысяч белков.
Авторы подробно охарактеризовали протеомный профиль, отличающий те и другие ноцицепторы от остальных подтипов клеток. Он характеризовался особым набором трансмембранных белков, и исследователи отмечают, что помимо маркеров их набор содержит потенциальные мишени для направленной терапии хронической боли.
Затем ученые сопоставили протеомные сигнатуры ноцицепторов и данные транскриптомов единичных клеток (scRNA-seq). Они выявили как совпадения, так и существенную разницу — из 554 уникальных маркеров на транскриптомном уровне 255 соответствовали протеомным маркерам. Это позволило выявить общие кластеры транскриптомов и протеомов, специфичные для типов клеток. Однако даже гены с малым количеством транскриптов (например, Mrgprd) выявлялись на протеомном уровне как специфичные маркеры.
Наконец, исследователи провели опыты по сенсибилизации ноцицепторов в культуре. Обработка фактором роста нервов (NGF), который провоцирует боль при воспалении in vivo, и активация протеинкиназы C сенсибилизировали пептидергические ноцицепторы к механическому стимулу. Это сопровождалось изменениями протеома. Авторы обнаружили, что в таких сенсибилизированных ноцицепторах повышается экспрессия гликозилтрансферазы B3GNT2. Опыты с нокдауном B3GNT2 указали на то, что этот фермент может выполнять важную функцию в сенсибилизации ноцицепторов.
Полученные результаты демонстрируют, что протеомика со сверхнизким входным объемом позволяет выявить специфические изменения в отдельных подтипах сенсорных клеток, непосредственно связанные с физиологией боли.
Генноинженерные цинковые пальцы выключили рецептор боли у обезьян
Источник
Chakrabarti, S., et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. // Nat Commun 17, 3437 (2026). DOI: 1038/s41467-026-71418-8
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0