Создан транспортер, доставляющий в кишечную палочку с расширенным генетическим кодом необычные аминокислоты
Для получения белков с необычными свойствами используется подход, называемый расширением генетического кода. Одному из кодонов, например, стоп-кодону UAG, ставят в соответствие аминокислоту, отсутствующую в природных белках. Однако проблема этого подхода состоит не только в создании эффективных тРНК и аминоацил-тРНК-синтетазы, но и в том, что неканоническая аминокислота с трудом проникает в клетку. Немецкие и швейцарские ученые получили с помощью направленной эволюции транспортер, доставляющий в клетку E. coli с расширенным генетическим кодом разветвленные пептиды, которые внутри клетки превращаются в разнообразные неканонические аминокислоты.
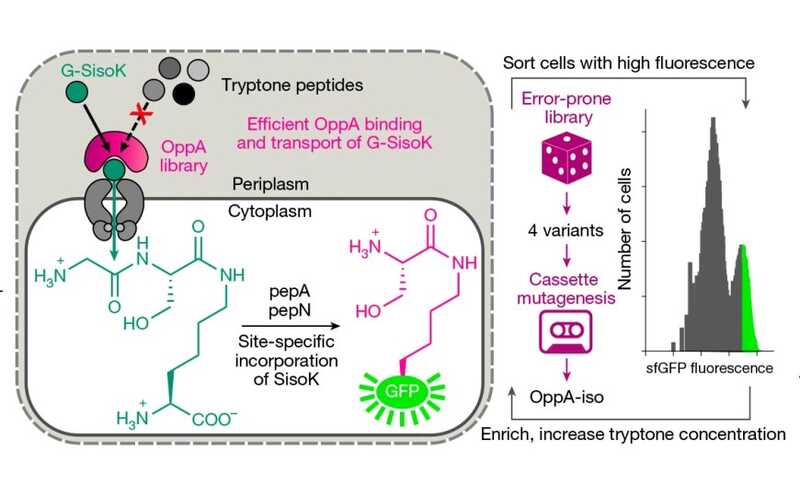
Эволюция транспортера, способного доставлять разветвленные пептиды в клетку кишечной палочки
Credit:
Nature (2025). DOI: 10.1038/s41586-025-09576-w | CC BY 4.0
Расширение генетического кода (GCE) и включение в состав белков неканонических аминокислот (ncAA) — мощный инструмент для получение белков с необычными функциями. Для этого может использоваться один из стоп-кодонов, чаще всего UAG (Amber) вместе с соответствующей тРНК и аминоацил-тРНК-синтетазой.
Тем не менее низкий выход модифицированного белка остается препятствием для его внедрения. Причина не только в недостаточно эффективном взаимодействии ортогональных молекул с клеточной системой трансляции и высокой стоимости ncAA, но также в плохой биодоступности ncAA и их низких внутриклеточных концентрациях. Чтобы преодолеть это ограничение, исследователи из Германии и Швейцарии сконструировали специальные транспортеры. В качестве основы они взяли бактериальный ABC-транспортер (ATP-binding cassette transporter); белковые комплексы, принадлежащие к этом семейству, переносят молекулы внутрь клетки, расщепляя АТФ. Полученные ими трансформеры доставляли внутрь клетки кишечной палочки E.coli трипептиды со специальной структурой, которые затем превращались в ncAA. Статья опубликована в Nature.
В своих предыдущих работах авторы встраивали в белки неканонические аминокислоты, которые позволяют получать белок-белковые конъюгаты, например, прикреплять к белку-мишени убиквитин или другую метку. Существуют ферменты, которые присоединяют метки к N- и C-концам аминокислотных цепочек. Авторы синтезировали «разветвляющие» аминокислоты на основе лизина (К), несущего на боковой цепи один или два аминокислотных остатка, распознаваемые таким ферментом. Вставка в белок подобной аминокислоты позволяет делать сшивку в любом положении, а не только по концевым группам. В новом исследовании авторы разработали транспортные механизмы для доставки таких конструкций в клетку.
В грамотрицательных бактериях, таких как E. coli, небольшие пептиды попадают в периплазму путем диффузии через порины внешней мембраны, а доставку через внутреннюю мембрану осуществляют транспортеры. Скрининг генома E. coli с помощью нокаутов отдельных генов показал, что для доставки выбранных авторами кеонструкций в клетку перспективен ABC-транспортер Opp (а также выявил пептидазы, необходимые для их процессинга).
Однако производство модифицированного белка снижалось в средах, богатых питательными веществами; авторы предположили, что короткие пептиды в среде, богатой триптоном и пептоном, конкурируют с их трипептидами за связывание с транспортером. Чтобы получить путем направленной эволюции более эффективный транспортер, «предпочитающий» ветвистые трипептиды линейным, авторы сконструировали систему, которая реагировала GFP-флуоресценцией на поглощение целевой конструкции. Это позволяло проводить отбор клеток по интенсивности флуоресценции. Конечный вариант OppA-iso, содержащий семь мутаций, в семь-десять раз повысил концентрации модифицированной аминокислоты в клетке. Штаммы E.coli с этим белком успешно включали ncAA в белки.
Если в клетку доставляли разветвленный трипептид, он расщеплялся до дипептида, высвобождая концевую аминокислоту. Таким образом, новый транспортер позволяет существенно расширить спектр доставки ncAA — оказалось, что в составе трипептида они лучше проникают в клетку, чем напрямую. Такой подход открывает путь к введению сразу двух модифицированных аминокислот в один белок.
В итоге становится возможной продукция в кишечной палочке белков с многими ранее недоступными ncAA, в том числе белков, подходящих для химиоферментативной конъюгации по любой точке. Кроме того, авторы разработали высокопроизводительную платформу направленной эволюции для конструирования транспортных систем, которые могли бы успешно доставлять в клетку неканонические аминокислоты. Они подчеркивают, что конструирование и оптимизация транспортеров — перспективная стратегия для улучшения импорта химически разнообразных «строительных блоков» для белков.
Четырехбуквенный код: как расширить спектр аминокислот в синтезируемом белке
Источник
Iype, T., et al. Hijacking a bacterial ABC transporter for genetic code expansion // Nature (2025). DOI: 10.1038/s41586-025-09576-w


 Меню
Меню





 Все темы
Все темы




 0
0