Создана плазмида, которая лишает бактерию устойчивости к антибиотикам
Американские исследователи сконструировали плазмиду, с помощью которой можно удалять ген устойчивости к антибиотикам у Enterococcus faecalis. Эффективность изобретения была продемонстрирована in vitro и на мышиной модели.
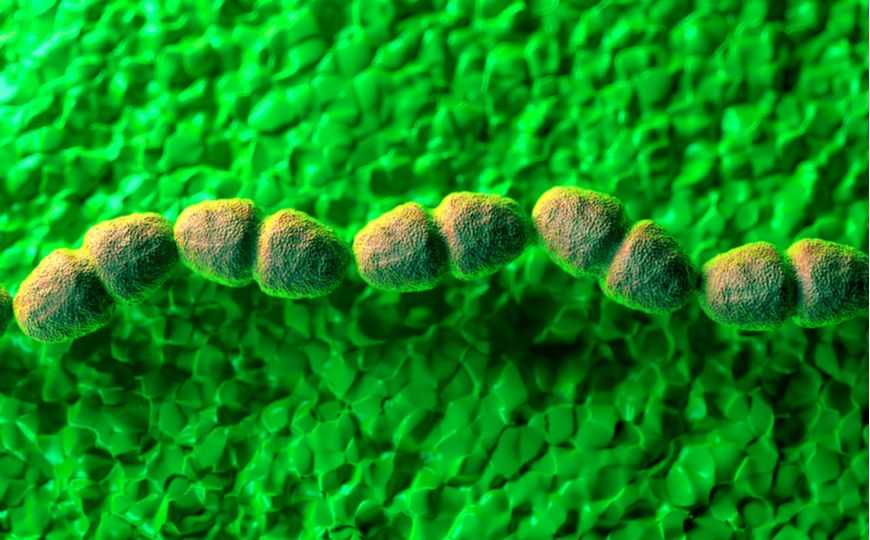
royaltystockphoto.com | Shutterstock.com
Enterococcus faecalis – естественный обитатель кишечной микрофлоры человека. Однако при нарушении микрофлоры из-за приема антибиотиков данный микроорганизм становится патогенным и приобретает устойчивость к одному или сразу нескольким антибиотикам. Сейчас E. faecalis — самая распространенная причина внутрибольничных заболеваний: появление патогенного организма с мультирезистентностью в микрофлоре больного существенно повышает риск заражения крови.
Для устранения гена устойчивости к антибиотикам была выбрана хорошо изученная система CRISPR- Cas9 — эндонуклеаза рестрикции Cas9 вносит двуцепочечный разрыв в участок гена, точно заданный гидовой РНК, что приводит к нокаутированию этого гена.
В предыдущих исследованиях система CRISPR c гидовой РНК, нацеленной на ген устойчивости, доставлялась в E. faecalis с помощью бактериофагов. Но изменчивость клеточной стенки бактерий, возникшая в ответ на заражение вирусом, снизила эффективность доставки.
Авторы статьи в журнале Antimicrobial Agents and Chemotherapy Американского общества микробиологов испробовали несколько способов борьбы с мультирезистентностью. Сначала они вводили в бактерии вектор с закодированной гидовой РНК к гену устойчивости, с расчетом на активацию собственной системы CRISPR в бактериях. Однако в мультирезистентных штаммах наблюдалась нехватка белка Cas9, из-за чего система не работала должным образом.
Затем было предложено доставлять систему CRISPR целиком на плазмиде PRP (плазмида, отвечающая на феромоны). (Клетка, не несущая PRP, выделяет феромоны, которые улавливает клеткой — донор плазмиды, в результате осуществляется быстрый и эффективный перенос копии плазмиды от донора к реципиенту через устанавливаемый контакт между клетками.) Таким образом, в качестве системы доставки CRISPR использовали штамм E. faecalis, несущий плазмиду PRP со всеми закодированными компонентами системы CRISPR. Механизм, очень похожий на тот, с помощью которого бактерии приобретают антибиотикорезистентность (а гены устойчивости также часто находятся в плазмидах), снова делает их чувствительными к антибиотикам.
В экспериментах in vivo на мышиной модели число копий гена устойчивости к антибиотикам снизилось в три раза.
«Мы предполагаем, что система такого типа может быть использована для возвращения восприимчивости к антибиотикам в популяции бактерий E. faecalis», — сказал соруководитель работы доктор Брек Дуэркоп. Он добавил, что дальнейшие исследования должны установить, в каких условиях плазмида может не передаваться клетке-реципиенту и как предотвращать подобные случаи.
Источники
Marinelle Rodrigues et al.// Conjugative delivery of CRISPR-Cas9 for the selective depletion of antibiotic-resistant enterococci. Antimicrobial Agents and Chemotherapy, 2019; DOI: 10.1128/AAC.01454-19
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0