Таблетку, которая вводит мРНК в стенку желудка, создали в МТИ
Исследователи из Массачусетского технологического института разработали капсулы для проглатывания, которые доставляют в организм до 150 микрограммов матричной РНК через инъекцию в стенку желудка. РНК проникает в кровеносную систему и разносится по организму. Эффективность доставки проверили на мышах и свиньях.
MIT News | CC BY-NC-ND
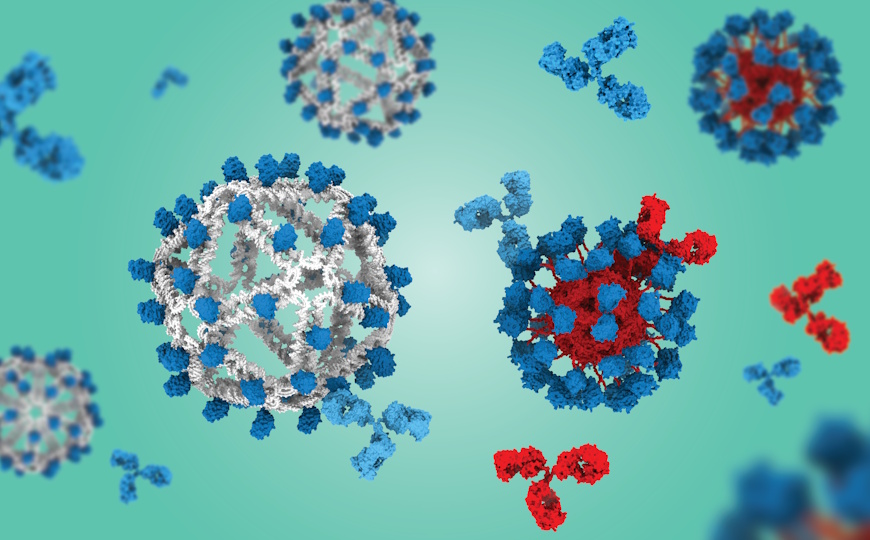
Терапевтические нуклеиновые кислоты (НК) и вакцины на их основе открывают новые возможности для лечения и профилактики болезней. В частности, вакцины против COVID-19 с матричной РНК оказались одними из самых эффективных в мире. Однако применение вакцин ограничивают дискомфорт от инъекций и сложность самостоятельной вакцинации без помощи специалиста. А при пероральном приеме нуклеиновые кислоты разрушаются.
Ученые из Массачусетского технологического института применили другой подход и разработали капсулу , которая доставляет НК в организм через стенку желудка. Такой подход может использоваться для доставки не только вакцин, но и терапевтических НК, например для лечения язвы желудка.
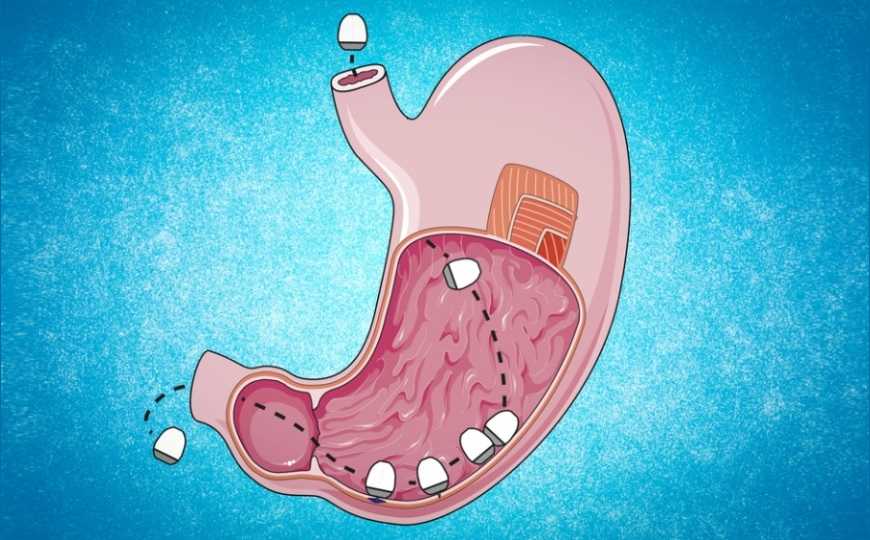
В течение нескольких лет лаборатории, которыми заведут последние авторы статьи Роберт Лангер и Джованни Траверсо, разрабатывали новые пути доставки препаратов в стенки желудочно-кишечного тракта. В 2019 году ученые создали капсулу, которая при попадании в желудок вводит в его стенку твердые лекарственные формы препаратов, например, прессованный лиофилизированный инсулин. Устройство получило название SOMA (self-orienting millimeter-scale applicator).
Капсула размером с небольшую ягоду спроектирована таким образом, что, подобно кукле-неваляшке или некоторым сухопутным черепахам, имеет единственную стабильную ориентацию. Инъекция всегда производится в стенку желудка, а не в просвет. После ориентирования капсулы гидратация активирует механизм на основе пружины (растворяется ступор, сделанный из сахара), а пружина вводит иглу в подслизистую основу стенки желудка. В 2021 году ученые показали, что таким образом можно доставлять маленькие молекулы, пептиды и моноклональные антитела в жидкой форме. Когда инъекция сделана, второй поршень втягивает иглу обратно в капсулу, чтобы ее можно было безопасно вывести через пищеварительный тракт.
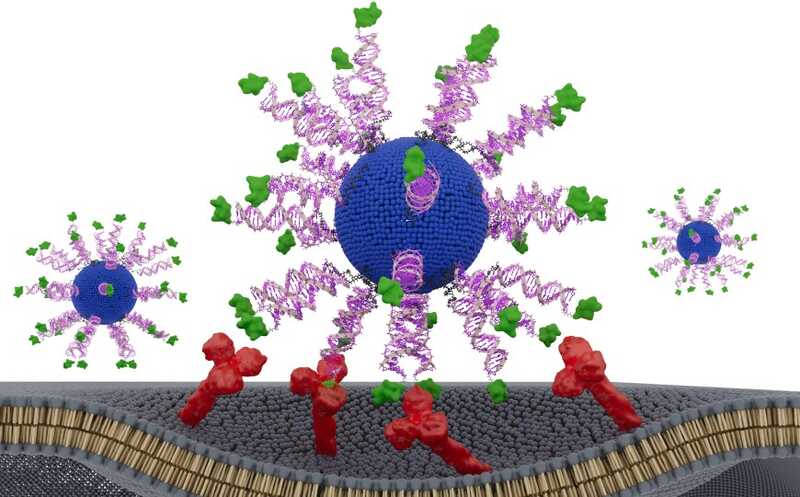
В настоящем исследовании ученые использовали капсулу для доставки других крупных молекул – НК. В отличие от белков, молекулы РНК проявляют активность только после того, как попадут в клетки. Чтобы спасти их от деградации во внутренней вреде организма, а также создать лекарственную форму, достаточно концентрированную для доставки в SOMA, ученые инкапсулировали мРНК в наночастицах из поли(бета-аминоэфиров). Эксперименты с различными клеточными линиями in vitro показали, что разветвленные полимеры лучше подходят для этого, чем линейные.
Эффективность доставки проверили на генетически модифицированных мышах, в организме которых производится флуоресцентный белок tdTomato в присутствии фермента Cre-рекомбиназы. Наночастицы, содержащие мРНК Cre-рекомбиназы, ввели мышам в хвостовую вену и в подслизистую основу стенки желудка. После введения комплексов в стенку желудка, но не в хвост репортерные белки обнаружили как в желудке, так и в печени.
Далее ученые лиофилизировали комплексы «мРНК-полимер» в присутствии сахарозы и поместили их в SOMA-капсулы. (Эта часть работы проводилась совместно с исследователями из компании Novo Nordisk.) В капсулу удалось поместить 50 мкг мРНК; свиньям давали по три капсулы, таким образом, суммарно вводили 150 мкг мРНК. Такое количество превосходит единичные дозы мРНК-вакцин Moderna и Pfizer (100 и 30 мкг соответственно). Вестерн-блоттинг выявил репортерный белок в желудке, но не в печени двух из трех свиней.
В дальнейшем ученые надеются увеличить эффективность доставки НК посредством оптимизации системы или введения большей дозы препарата.
Исследователи указывают на необходимость использования в последующих экспериментах терапевтических НК, таких как мРНК-вакцины, вместо модельных. Это позволит оценить, насколько хорошо развивается иммунный ответ при таком необычном способе доставки.
Источник
Alex Abramson, et al. Oral mRNA delivery using capsule-mediated gastrointestinal tissue injections // Matter, published online 31 January, 2022, DOI: 10.1016/j.matt.2021.12.022


 Меню
Меню





 Все темы
Все темы



 0
0