ДНК-оригами против ВИЧ
Эффективная вакцина против ВИЧ должна индуцировать выработку широконейтрализующих антител (ШНАт) к этому вирусу, однако их предшественники редки в иммунном репертуаре человека. Уже показано, что белковые наночастицы, несущие множество копий антигена, вызывают более сильный иммунный ответ, чем тот же антиген сам по себе. Однако белковый каркас наночастиц сам по себе может быть иммуногенен, и это, в свою очередь, может снижать выработку целевых ШНАт. Чтобы решить эту проблему, авторы статьи в Science предложили собирать такие наночастицы на основе ДНК вместо белка. Они применили метод ДНК-оригами, чтобы сконструировать наночастицы с эпитопом gp120 (поверхностного белка ВИЧ), и показали на мышах, что каркас из ДНК стабилен и неиммуногенен, а наночастицы стимулируют выработку ШНАт эффективнее, чем тот же антиген в виде мономеров.
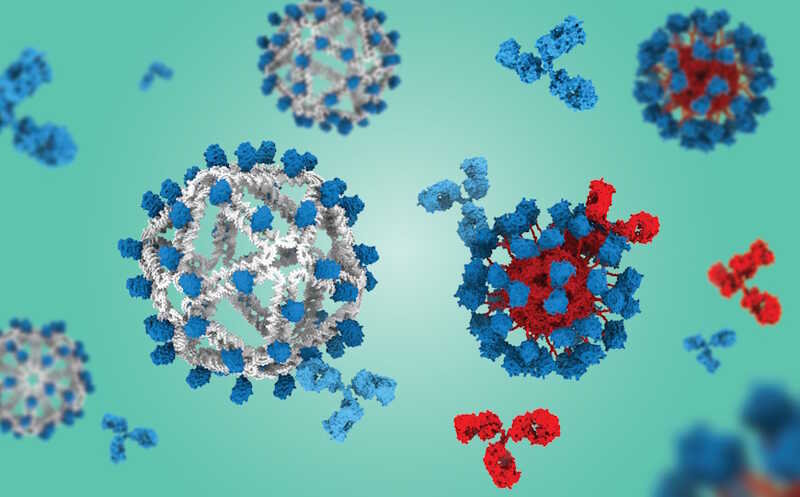
Наночастицы на основе ДНК (серого цвета), несущие эпитоп поверхностного белка ВИЧ, стимулируют выработку антител к нему, но, в отличие от белковых наночастиц, неиммуногенны сами по себе.
Credit:
MIT and Scripps Research |
пресс-релиз
Главная задача вакцины против ВИЧ, разработки которой продолжаются до сих пор, — это вызвать в организме продукцию широконейтрализующих антител (ШНАт) к вирусу. Однако их предшественники редко встречаются в иммунном репертуаре человека, поэтому стимулировать их выработку при первичной вакцинации сложно. Перспективный подход к тому, чтобы стимулировать размножение именно антигенспецифичных B-клеток, основан на применении белковых вирусоподобных частиц, содержащих много молекул иммуногена. Однако их структурные белки также способны вызывать иммунный ответ, который может ограничивать размножение целевых B-клеток, специфичных к антигенам ВИЧ. Авторы статьи в Science предложили создавать каркас вирусоподобных частиц на основе ДНК, а не белков, и применили для этого технику ДНК-оригами.
За основу ученые взяли ДНК-скаффолд, который ранее успешно применили для презентации антигенов SARS-CoV-2. Они встроили в него фрагмент поверхностного белка ВИЧ gp120 — eOD-GT8, — для которого подтверждена способность стимулировать выработку высокоаффинных антител. Сконструированные наночастицы диаметром около 40 нм содержали 30 таких фрагментов каждая и активировали B-клетки в культуре, тогда как растворимый eOD-GT8 в том же количестве (5 нмоль/л) не приводил к активации.
Исследователи предположили, что мультивалентные частицы вызовут у мышей более сильный иммунный ответ, чем мономеры eOD-GT8. Они вводили иммунокомпетентным мышам (C57BL/6) один из двух иммуногенов в сочетании с адъювантом, а затем отслеживали титры антител в крови животных. Как контрольные мономеры, так и вирусоподобные ДНК-частицы вызывали слабый иммунный ответ после первичной вакцинации, однако в случае наночастиц он значимо усиливался после введения бустерной дозы. «Голые» ДНК-наночастицы при этом не были иммуногенны.
Оценив состояние герминативных центров в лимфоузлах однократно иммунизированных мышей, авторы не обнаружили разницы между ДНК-наночастицами и контрольными мономерами. Из-за большого количества свободных ДНКаз, в норме присутствующих в крови, наночастицы на основе ДНК могли быть недостаточно стабильными. Однако это предположение не подтвердилось, когда ученые провели опыты на мышах с нокаутом ДНКаз. Авторы пришли к выводу, что конструкция наночастиц неоптимальна для того, чтобы вызвать ответ при первичной иммунизации, хотя это и на связано со стабильностью ДНК.
Дальнейший анализ показал, что ДНК-наночастицы слабо взаимодействуют с фолликулярными дендритными клетками. Авторы предположили, что это связано с недостаточной плотностью антигенов на их поверхности, и синтезировали частицы меньшего диаметра (23 или 34 нм), которые несли по 30 или 60 копий eOD-GT8. На полученном наборе они подтвердили, что плотность антигенов влияет на эффективность иммунизации; наиболее перспективными оказались частицы диаметром 34 нм, содержащие 60 копий антигена.
Затем ученые дополнили их универсальным T-хелперным эпитопом PADRE, который связывает широкий спектр HLA. Они предположили, что увеличенная из-за этого доля антигенспецифичных B-клеток в герминативных центрах обеспечит более «сфокусированный» иммунный ответ. Подтвердив влияние на B-клеточный состав, исследователи перешли к опытам на гуманизированных мышах.
Эксперименты проводили на трансгенных мышах, экспрессирующих сегмент человеческого гена IGHV1-2*02 в локусе мышиного иммуноглобулина. Такая модель отражает разнообразие B-клеток, потенциально способных вырабатывать ШНАт; как и у человека, их общая доля в репертуаре невелика. Мышам вводили ДНК-наночастицы с PADRE или белковые наночастицы в качестве контроля. Через 14 дней им проводили секвенирование отдельных B-клеток герминативных центров, чтобы охарактеризовать репертуар B-клеточных рецепторов (BCR). Сравнение представленности различных клонов показало, что вакцинация ДНК-наночастицами стимулировала размножение некоторых линий B-клеток, специфичных к антигену ВИЧ, причем эффективнее, чем наночастицы на основе белка.
Таким образом, замена белкового каркаса наночастиц на ДНК позволила сконструировать молекулы, которые лишены нецелевой иммуногенности и стимулируют выработку антител к эпитопу gp120 ВИЧ. По-видимому, это способно повысить эффективность иммунизации, и авторы надеются, что полученные ими результаты подтолкнут разработку вакцины против ВИЧ.
Эпитоп ВИЧ, лишенный ключевого гликана, может стать основой для вакцины
Источник
Anna Romanov, et al. DNA origami vaccines program antigen-focused germinal centers. // Science 391, eadx6291 (2026). DOI: 10.1126/science.adx6291


 Меню
Меню





 Все темы
Все темы




 0
0