Три модификации Fc-фрагмента антитела усилили привлечение иммунных клеток в опухоли молочной железы
Ученые из Великобритании разработали комбинированный подход к дизайну терапевтических антител против резистентного к химиотерапии HER2-положительного и трижды негативного рака молочной железы. Они взяли за основу антитела к HER2 и фолатному рецептору, подтвердив, что эти антигены сохраняются в опухолях после лечения, и оптимизировали их структуру одновременно двумя способами. Для модификации ученые прибегли к гликоинженерии, а также внесли две точечные мутации в Fc-фрагмент антитела. Такая трижды модифицированная молекула усиленно связывалась как с иммунными клетками, так и с раковыми клетками-мишенями. Она активнее, чем антитела дикого типа, привлекала эффекторные клетки в опухоль, в том числе активируя те, которые были супрессированы опухолевым микроокружением. Результаты подтвердились как в опытах in vitro, так и на мышиных моделях РМЖ.
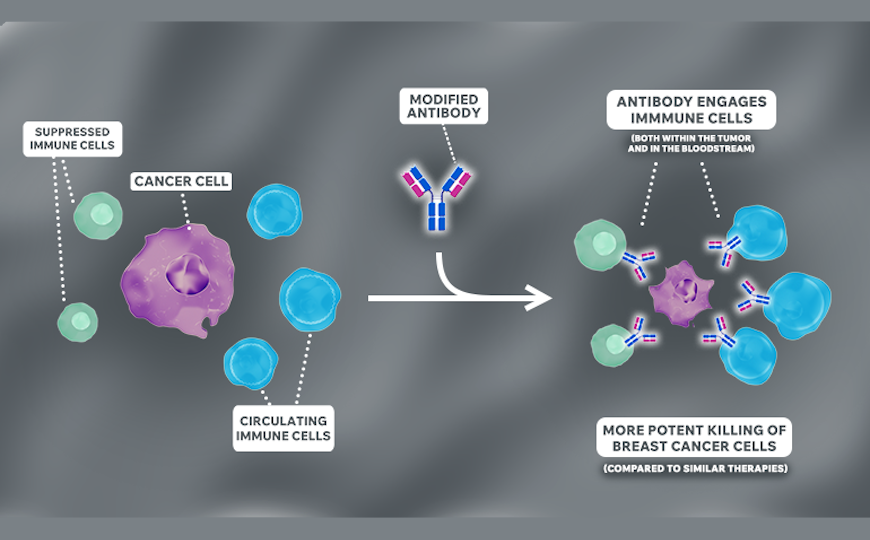
«Трижды модифицированное антитело» одним участком прикрепляется к раковым клеткам, а другим — к иммунным.
Credit:
King's College London |
пресс-релиз
Авторы проанализировали транскриптомные данные пациентов с HER2-положительным или трижды негативным РМЖ, в том числе устойчивом к неоадъювантной химиотерапии. Они сосредоточились на иммунных эффекторных клетки, экспрессирующих Fc-рецептор (FcR). С помощью секвенирования РНК единичных клеток (scRNA-seq) и пространственного профилирования ученые подтвердили сохранение популяции эффекторных клеток, экспрессирующих FcγRIIIa (подтип Fc-рецептора, который связывается с IgG-антителами), в HER2+ опухолях и ТНРМЖ.
Для того, чтобы разработать антитело к резистентным опухолям, уже подвергавшимся химио- и иммунотерапии, ученые искали гены, которые сохраняются в опухоли и ее микроокружении после лечения. Мишенями стали два антигена РМЖ — HER2 и фолатный рецептор α (FRα), экспрессия которого оставалась относительно стабильной в ТНРМЖ после терапии.
Опираясь на эти данные, исследователи сконструировали моноклональные антитела с повышенным сродством к FcγRIIIa, предполагая, что это может усилить их противоопухолевое действие. Антитела были нацелены на одну из выявленных мишеней, а их модификация сочетала два метода: внесение точечных аминокислотных замен и гликоинженерию N-связанного Fc-гликана. Эксперименты на клеточных моделях показали, что данные модификации значительно повышают аффинность антитела к FcγRIIIa, сохраняя при этом специфичное распознавание опухолевого антигена с помощью Fab-фрагмента, связывание и антипролиферативную активность.
Модифицированные антитела действовали активнее, чем специфичные к тем же антигенам варианты дикого типа. Они усиливали активность иммунных эффекторов против HER2+ РМЖ и ТНРМЖ, стимулируя выработку провоспалительных цитокинов NK-клетками и макрофагами.
На мышиных моделях ученые продемонстрировали, что модифицированные антитела сдерживали рост ортотопических ксенотрансплантатов HER2+ и FRα+ рака молочной железы и привлекали в опухоли FcγRIIIa-экспрессирующие иммунные клетки.
Первый автор исследования, доктор Алисия Ченовет (Alicia Chenoweth) из Королевского колледжа Лондона, прокомментировала: «Внеся несколько ключевых изменений в структуру антитела, мы обнаружили, что оно может активировать иммунную систему гораздо интенсивнее, чем немодифицированное антитело, которое в настоящее время применяют для терапии рака молочной железы. Многие иммунные клетки в опухолях молочной железы находятся в “супрессированном” состоянии, и их сложно активировать немодифицированными антителами. Мы обнаружили, что наши трижды модифицированные антитела способны не только активировать эти иммунные клетки для уничтожения раковых клеток, но и переводить их в более “активированное” состояние в целом».
Таким образом, модификация Fc-рецепторов позволила оптимизировать стратегию инженерии моноклональных антител, нацеленных на опухолевые клетки. Гликоинженерия и внесение точечных замен усилили взаимодействие антитела с рецепторами на эффекторных иммунных клетках. Это позволило активнее привлекать иммунные клетки к опухолям, что в итоге повысило иммуностимулирующие и противоопухолевые свойства терапии.
Инсулинрезистентные адипоциты повышают агрессивность рака молочной железы с помощью экзосом
Источник
Alicia M. Chenoweth et al. An Fc-Engineered Glycomodified Antibody Supports Proinflammatory Activation of Immune Effector Cells and Restricts Progression of Breast Cancer. //Cancer Research (2025), published online 23 October 2025. DOI:
10.1158/0008-5472.CAN-24-3174
Цитата по
пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0











