Туберкулезная микобактерия усиливает патогенный потенциал криптококка
Cryptococcus neoformans поражает легкие человека, как и Mycobacterium tuberculosis. При коинфекции риск смерти выше, чем при инфекции только Cryptococcus. Исследователи из Великобритании и Уганды показали, что под действием как живых, так и убитых нагревом микобактерий криптококк может увеличиваться в размерах и наращивать полисахаридную капсулу. Напротив, у некоторых изолятов растет доля мелких клеток. Крупные укрытые капсулой клетки хуже распознаются иммунитетом, а мелкие криптококки лучше распространяются по организму.
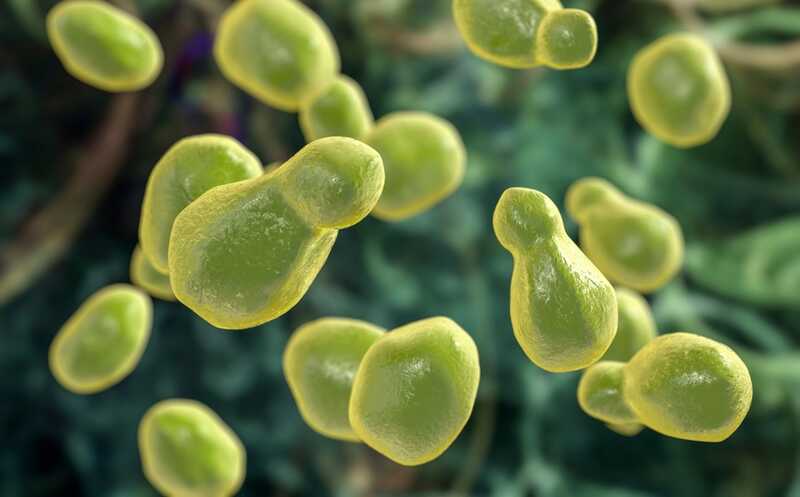
Грибок Cryptococcus neoformans поражает легкие при вдыхании спор. При этом образуются узелки, известные как гранулемы. Возбудитель туберкулеза Mycobacterium tuberculosis действует схожим образом — он попадет в легкие после вдыхания взвешенных частиц, после чего также образуются гранулемы. Нарушение работы иммунной системы из-за, например, ВИЧ, приводит к тому, что эти патогены распространяются на другие органы, включая центральную нервную систему, с развитием менингоэнцефалита.
Всемирная организация здравоохранения (ВОЗ) включила C. neoformans в список приоритетных грибковых патогенов. C. neoformans-ассоциированный менингит связывают с 118 тыс. смертей ежегодно. В странах с высоким уровнем дохода смертность достигает 20–30%, а в странах с низким уровнем дохода — 70%. По оценкам ВОЗ, только в 2021 году туберкулезом заболели 10,6 миллиона человек, а 1,6 миллиона умерли, при этом 11,7% смертей пришлись на ВИЧ-положительных пациентов. Появляются штаммы со множественной лекарственной устойчивостью. Коинфекция C. neoformans и M. tuberculosis вызывает повышенную обеспокоенность, особенно в странах Африки южнее Сахары и Азии. При коинфекции риски смерти выше, чем при инфекции только Cryptococcus. Однако неясно, взаимодействуют ли патогены и как воздействуют друг на друга. Этот вопрос прояснили исследователи из Великобритании и Уганды.
C. neoformans H99 культивировали в присутствии вакцинного штамма Mycobacterium bovis в условиях, имитирующих условия организма. Через 24 часа доля клеток-титанов (≥10 мкм) и клеток среднего размера (5–9 мкм) увеличилась примерно на 4,5 и 10% соответственно, а доля более мелких клеток (≤5 мкм) уменьшилась примерно на 14%. Предположительно, грибок распознает присутствие живой бактерии и реагирует на это, увеличивая разнообразие своей популяции. Те же закономерности наблюдались через 48 часов, но менее выражено.
Далее C. neoformans H99 культивировали в присутствии убитого нагреванием штамма M. tuberculosis. Грибки в этих условиях были больше, доля клеток-титанов через 24 часа выросла на 27,4%, а доли клеток среднего и маленького размера снизились на 13% и 14% соответственно. Закономерность сохранялась спустя 48 часов. Плотность грибковых клеток также выросла.
У клеток-титанов намного толще полисахаридная капсула, что позволяет им лучше избегать иммунного ответа и персистировать в тканях. В присутствии как живых M. bovis, так и убитых бактерий M. tuberculosis, толщина капсулы повышалась спустя 48 часов.
Исследователи проанализировали два высоковирулентных клинических изолята (SACl012 и UgCl387) и два низковирулентных изолята (UgCl223 и UgCl425) C. neoformans. SACl012 и UgCl387 вели себя так же, как и анализируемый до этого штамм H99. Изолят SACl012 не образовывал клеток-титанов, в этом случае увеличивалась доля клеток среднего размера.
Низковирулентные штаммы вели себя иначе. UgCl223 не менял размеры, но доля мелких клеток возрастала на 12%. Возможно, это происходит для лучшего распространения — мелки клетки грибков лучше преодолевают эндотелиальные барьеры. Размеры UgCl425 увеличивались, как это было показано для высокопатогенных изолятов, не образующих клеток-титанов.
Таким образом, изоляты с высокой вирулентностью преимущественно увеличиваются в размерах в присутствии микобактерий, что связано с уклонением от иммунитета и тканевой персистенцией, тогда как изоляты с низкой вирулентностью либо усиливают выработку мелких клеток, что способствует распространению, либо увеличиваются в размерах. То есть присутствие микобактерий действует как сигнал окружающей среды, который усиливает стратегии вирулентности, специфичные для штамма.
Высоковирулентный изолят SACl012 также наращивали толщину капсулы, как и H99. Однако второй изолят UgCl387, напротив, снижал размер капсулы. Оба низковирулентных штамма увеличивали толщину капсулы.
Легочные альвеолярные макрофаги входят в число первых иммунных клеток, которые сталкиваются с C. neoformans в легких. Макрофаги, похожие на альвеолярные (AM), получили из клеток косного мозга мышей. Их стимулировали убитой нагревом микобактерией и рекомбинантным IFN-γ, чтобы симулировать ответ на бактерию в легких. Такие AM значительно хуже сдерживали рост C. neoformans. То есть грибки, подвергшиеся воздействию микобактериальной среды, могут сохраняться и размножаться даже внутри активированных макрофагов.
Полученные результаты подтверждают модель, согласно которой чувствительность C. neoformans к микобактериям усиливает патогенный потенциал грибков, и это облегчает адаптацию, персистенцию и распространение криптококка.
Грибок, вызывающий менингит, устойчив к антибиотику за счет глюкозы из тканей мозга
Источник:
Orlando Ross, et al. Cryptococcus neoformans responds to presence of Mycobacterium by diversifying its morphologies and remodelling its capsular material // Journal of Medical Microbiology (2026), 23 February 2026, DOI: 10.1099/jmm.0.002128


 Меню
Меню





 Все темы
Все темы




 0
0










