Григорий Ениколопов: «Все плохое угнетает нейрогенез. А все хорошее усиливает»
«Не нервничай, нервные клетки не восстанавливаются» — это не просто обывательское представление. Долгое время и ученые-нейрофизиологи считали, что нейроны в мозге только убывают, но не прибавляются, потому что зрелые нервные клетки не делятся. Но оказалось, что в мозге есть запасные элементы — нейральные стволовые клетки, которые рождают новые нейроны. Однако делают они это не так, как другие стволовые клетки. О том, как происходит нейрогенез, мы говорим с Григорием Ениколоповым.

Григорий Ениколопов, профессор Университета Стони Брук (США)
Нейроны канарейки
Григорий Николаевич, открытие стволовых клеток, которые превращаются в нейроны, опровергло расхожее мнение о том, что «нервные клетки не восстанавливаются». Когда и как это произошло?
У стволовых клеток мозга довольно долгая история. В 1910–1911 годах испанский ученый Рамон-и-Кaхаль выдвинул очень определенную идею, что мы рождаемся со всеми нейронами, а в течение жизни их только теряем и ничего не приобретаем. Рамон-и-Кaхаль был ученым поразительного уровня и, можно сказать, создал науку нейробиологию такой, как бы ее сейчас понимаем, и на 99,9% то, что он говорил, было правильно. Но в то время, с тогдашними методами, он просто не мог увидеть других процессов. А в 1961–62 годах появились изотопные методы мечения делящихся ДНК, и стало возможным и модным смотреть, как клетки делятся в разных тканях. Джозеф Альтман из MIT опубликовал статью о том, что в мозге взрослой крысы видны делящиеся клетки и их довольно много. Но это открытие долго лежало без движения, поскольку слишком сильна была догма о том, что новые нейроны не появляются. Причем эта статья была в «Science», не в каком-то неизвестном журнале.
И все равно ей не сразу поверили?
Да. Даже не оттого, что люди косные или непонятливые. Просто это очень серьезное заявление и требует исключительно надежных подтверждений. Например, были вполне законные соображения, что нужно еще доказать, действительно ли эти делящиеся клетки — нейроны. Может быть, это клетки глии, может быть, это клетки кровеносных сосудов, может быть, вообще неизвестно что; откуда известно, что это нейроны?
Как ни странно, первые доказательства пришли не от мышей или крыс, а от птиц. Замечательный ученый Фернандо Ноттебом из Рокфеллеровского университета, который изучал птиц, обнаружил, в 80-х годах что у канареек во взрослом возрасте происходит смена нейронов — огромное их количество умирает, и новые появляются в определенных областях мозга, которые отвечают за обучение песне. И он смог при помощи антител показать, что эти новые клетки — действительно нейроны. Это был очень важный шаг. После этого люди начали серьезнее к этому относиться, разные лаборатории стали проверять это на крысах и мышах и уже намного более достоверно показывать, что так и есть: мозг взрослых животных содержит делящиеся клетки, которые превращаются в новые нейроны. А потом группа в Швеции показала, что можно взять мозг человека и там в гиппокампе увидеть делящиеся клетки — клетки, которые включили в себя БРДУ.
БРДУ, бромодезоксиуридин — это метка делящейся клетки? Они смотрели клетки на посмертных срезах мозга?
Это были посмертные срезы мозга людей, которым при жизни проводили онкотерапию и для разных клинических целей, в частности, для определения индекса пролиферации вводили БРДУ. Они разрешили использовать свой мозг после смерти. БРДУ — это аналог тимидина, который включается в ДНК, и потом его можно выявлять при помощи антител. Если этой метки много, значит, там дуплицировалась ДНК, а значит, клетки делились.
Так как это был именно человеческий мозг, эта находка сразу вывела гипотезу на другую орбиту. Стало ясно, что нейрогенез происходит не только у птиц или грызунов, но и у человека и что это может играть какую-то роль в работе мозга.
«Если не дать рождаться новым нейронам, то некоторые тонкие элементы памяти портятся»
Но есть отличия. У грызунов стволовых клеток и новых нейронов больше всего в обонятельной луковице, обоняние играет у них очень важную роль. У человека они там есть, но очень быстро истощаются, по-видимому, в раннем младенчестве (возможно, ольфакторные стимулы намного важнее для младенцев, чем мы думаем). А у взрослого человека нейральные стволовые клетки делятся в гиппокампе, главным образом в зубчатой фасции (небольшая структура, похожая на бахромку. — Н.М.). Уже было известно, что с гиппокампом связана память, и обнаружение новых нейронов в гиппокампе сразу интуитивно легло в эту концепцию. Легко представить себе, что новая память образуется в том числе и при помощи новых клеток. Но твердо доказать это очень трудно.
Тут несколько вопросов, которые сейчас бурно обсуждаются. Один вопрос: как может такое небольшое количество клеток влиять на память? Потому что и сам гиппокамп не очень велик, а зубчатая фасция еще меньше, у мыши в ней содержится около 0,1% всех нейронов. Видимо, ответ заключается в том, что гиппокамп и его зубчатая фасция действуют как воронка: они расположены в стратегически важных областях, и через них проходит огромное количество информации из коры, потом информация обрабатывается и идет обратно в кору и в другие области мозга. И на животных можно надежно показать, что это так; намного труднее это доказать для человека.
Хотя первые доказательства появляются, в том числе и в наших работах совместно с Институтом нейрохирургии имени Бурденко. Если не дать рождаться новым нейронам, то некоторые тонкие элементы памяти портятся. Например, человек легко запоминает последовательность предметов: яблоко, собачка, стол... Но если внести небольшие изменения — яблоко будет другого цвета, или собачка будет смотреть в другую сторону, или стол будет немного другой формы, люди, у которых подавлено появление новых нейронов, начинают сбиваться.
Эта грань памяти, связанная с системой зацепок и ориентиров, по которым мы различаем сходные предметы и контексты, — именно то, что особенно страдает, например, при болезни Альцгеймера. Нейроны гиппокампа особенно чувствительны к повреждениям и часто погибают первыми, это может объяснять, почему заболевание начинается именно с нарушения памяти. Люди теряются в городе, на улице, потому что их обычные ориентиры не работают. Мы обычно не задумываемся, какой наш подъезд или квартира, хотя все они внешне очень похожи, а для человека с Альцгеймером бывает трудно вспомнить те небольшие отличия, которые отделяют нужное от ненужного, и он может не суметь выбрать между похожими домами или подъездами.
А было показано, что при болезни Альцгеймере нейрогенез подавлен?
Появилось несколько статей из очень хорошей лаборатории, от очень точных и требовательных ученых, о том, что гиппокампальный нейрогенез очень сильно падает с возрастом. По их данным он очень бурно происходит у детей, меньше у подростков, а дальше все больше снижается, и даже в нормальном мозге взрослых людей трудно обнаружить те маркеры, которые обычно связывают с нейрогенезом. Эта статья взбудоражила всю область, и, как это часто бывает, противоречивые результаты заставили искать новые и более надежные доказательства того, что в мозге взрослого человека действительно рождаются новые нейроны. Так что теперь предположение о том, что нейрогенез у человека идет очень долго, в течение всей жизни, стоит на намного более твердой основе. И когда сравнивают мозг людей без Альцгеймера и с Альцгеймером, то с намного большей уверенностью можно утверждать, что при Альцгеймере нейрогенезез падает особенно сильно. Это важно, потому что сразу возникает вопрос - нельзя ли остановить или хотя бы замедлить развитие болезни Альцгеймера повышением уровня рождения новых нейронов.
Есть ли сегодня способы наблюдать прижизненный нейрогенез у человека?
Методы появляются, но весьма неэффективные. Я участвовал в работе, в которой его пытались обнаружить при помощи MRS — magnetic resonance spectroscopy, именно spectroscopy, а не imaging, это важная деталь. Там маркером был некий липид, про который сейчас мы знаем, что стволовые клетки им «набиты», так что, скорее всего, подход был правильный. Но все равно использовать это оказалось трудно, например, из-за того, что сигнал был очень сильным у детей, но резко падал у взрослых. Были и другие попытки. Но в целом это очень сложная задача — как найти маркеры, которые бы прижизненно фиксировали нейрогенез у человека. Над этой нерешенной задачей бьются много лабораторий, пытаются подойти к ней с разных сторон.
От молекулы NO до нейральных стволовых клеток
Григорий Николаевич, когда вы впервые занялись нейрогенезом?
Мы с моей женой Натальей Пеуновой работали в одной лаборатории, у Георгия Павловича Георгиева в Институте молекулярной биологии, а потом начали работать вместе в Лаборатории Колд-Спринг-Харбор. Занимались влиянием моноксида азота, NO, недавно открытой молекулой, на дифференцировку нейральных клеток. Мы опубликовали статью в Nature, и это была фактически первая работа, которая показала, что NO — важный фактор развития, в частности, развития нейронов.
В какую сторону он влияет?
NO тормозит деление клеток. Если какая-то клетка типа стволовой делится и делится, то для того, чтобы дифференцироваться, ей нужно остановить деление. Бурное деление и дифференцировка, за редкими исключениями, вещи почти всегда несовместимые. И NO помогает клетке приостановиться. Если программа нейрональной дифференцировки уже запущена, то эти клетки превращаются в нейроны. Если же подавить производство NO, то клетки продолжают делиться и не превращаются в нейроны, но их можно спасти, если добавить молекулы, производящие NO.
NO образуется в организме эндогенно, при каких-то окислительно-восстановительных реакциях?
У него несколько разных источников, главным образом, это ферментативные реакции, при помощи NO-синтаз. Например, огромное количество NO образуется при заражениях и воспалениях — организм с его помощью пытается убить заражающие микроорганизмы. В мозге главным источником NO является нейрональная изоформа NO-синтазы.
Нас интересовало — как клетки, которые делятся, решают перестать делиться и начать дифференцироваться? Мы получили такую линию мышей, у которых нокаутирован ген нейрональной NO синтазы, и увидели, что у них увеличивается мозг, так как появляется слишком много новых нейронов. Мы показали, что NO работает против пролиферации клеток во время развития, в частности, во время развития мозга. Из-за того, что мы занимались дифференцировкой, возник большой интерес к стволовым клеткам и к нейрогенезу. Меня эта тема очень заинтересовала, в ней удачно соединилось то, что я знал из нейробиологии и из молекулярной биологии.
Правда, сейчас большая часть нашей работы связана с другими вещами — нейрональными сетями, которые контролируют социальное поведение. Нас интересует, где располагаются центры, которые вовлечены в социальное поведение мышей, в частности, агрессию, и как они друг с другом «разговаривают». Наша модель — это агрессивное поведение, ее разработала для мышей Наталья Николаевна Кудрявцева в Новосибирске. Она была у нас здесь, в Америке, наладила модель, сейчас мы продолжаем с ней взаимодействовать, готовим большую статью по нейронным цепям, определяющим агрессивное поведение. А начали мы это направление, изучая возможную связь между агрессией и нейрогенезом.
А вы реально нашли эту связь?
Да. Если самец мыши раз за разом побеждает в драке с другими самцами, то у него усиливается нейрогенез; если же он раз за разом терпит поражение, то у него развивается хронический стресс.
И хронический стресс угнетает нейрогенез?
Совершенно верно. Вообще, все что обычно ассоциируется с чем-то плохим, его угнетает. А все хорошее усиливает.
Ваш брат Сергей Николаевич Ениколопов — ведущий специалист по психологии агрессивного поведения. Обсуждаете ли вы с ним научные проблемы и бывает ли, что какие-то идеи при этом рождаются?
Да, конечно. Он дает очень хорошие советы, потому что глубоко знает эту тему и концептуальные вопросы в области агрессии. Хочется понять общую модель агрессии, и как она преломляется у человека. И хотя мы потом работаем на мышках, но мне это очень помогает.
Нейрогенез «пессимистический» и «оптимистический»
Вы предложили свою схему деления нейральных стволовых клеток. Расскажите, пожалуйста, про нее.
Классические стволовые клетки — это клетки крови, и для них была известна схема деления. Клетка до поры до времени спит, потом пробуждается, производит «дочку», «дочка» размножается, а стволовая клетка идет назад спать, потом опять пробуждается и т.д. Это была классическая модель для кроветворных клеток, и она почти автоматические приклеилась к другим стволовым клеткам.
Но за несколько лет до этого мы сконструировали очень полезную линию трансгенных мышей, у которых стволовые клетки мозга высвечены зеленым флуоресцентным белком. Она позволила нам увидеть стволовые клетки мозга и их непосредственное потомство, и стало казаться, что их деление не укладывается в традиционную модель. Эти клетки много раз делятся, пока мозг развивается, но после рождения сценарий меняется. Клетки перестают делиться, но когда одна из них пробуждается, то быстро проходит через два-три деления, причем делится асимметрично — производит «дочку», которая совсем не похожа на нее. После такого залпа делений стволовая клетка постепенно меняет свою форму и превращается в обычный астроцит, клетку глии, и на этом ее жизненный цикл заканчивается. Дочерние клетки делятся уже симметрично, потом деление останавливается, и клетки начинают медленно превращаться в нейроны. Все деление занимает дня три-четыре, медленное превращение в нейроны может занимать до месяца, а функциональное созревание нейронов — три-четыре месяца.
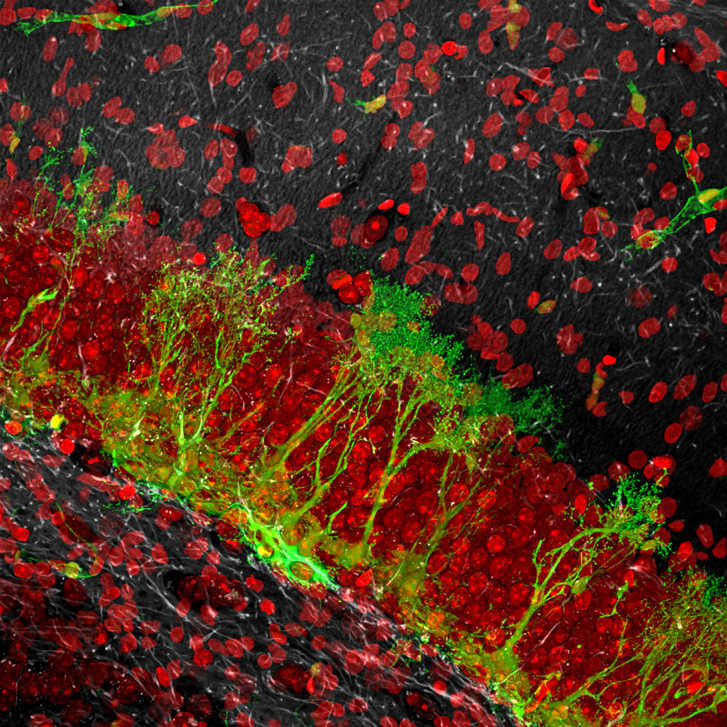 Стволовые клетки (зеленые клетки с радиальными отростками) в зубчатой фасции гиппокампа, ядра гранулярных нейронов окрашены красным. Репортерная линия мышей Nestin-GFP
Стволовые клетки (зеленые клетки с радиальными отростками) в зубчатой фасции гиппокампа, ядра гранулярных нейронов окрашены красным. Репортерная линия мышей Nestin-GFP
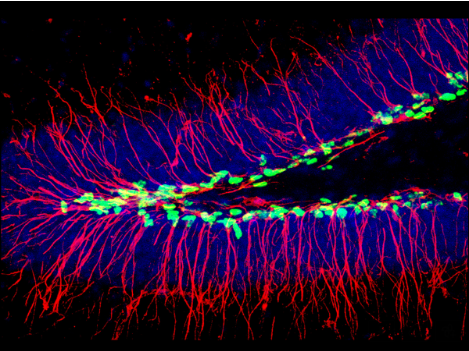 Ядра стволовых клеток (окрашены зеленым) и их радиальные отростки (красные) среди гранулярных нейронов (ядра окрашены синим) в зубчатой фасции гиппокампа. Репортерная линия мышей Nestin-CFPnuc
Ядра стволовых клеток (окрашены зеленым) и их радиальные отростки (красные) среди гранулярных нейронов (ядра окрашены синим) в зубчатой фасции гиппокампа. Репортерная линия мышей Nestin-CFPnuc
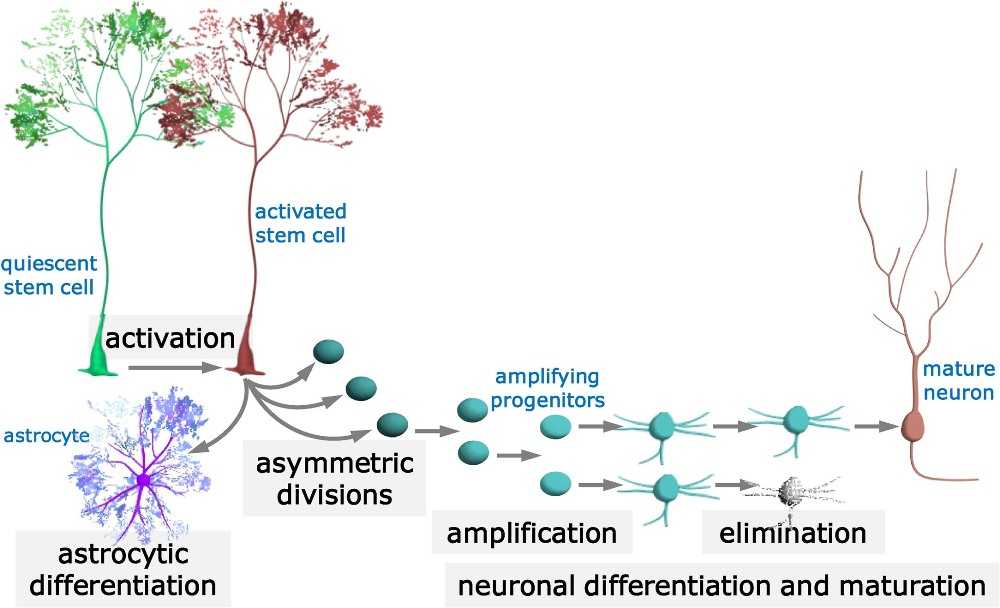 Схема деления и дифференцировки нейральной стволовой клетки. Зеленым показана спящая стволовая клетка, красным — активированная стволовая клетка, которая асимметрично делится с образованием «дочек» (круглые клеточки); «дочки» делятся симметрично, из их потомков развиваются новые нейроны, которые затем созревают. Cтволовая клетка, прошедшая через деление, превращается в астроцит (фиолетовый). | Behav Brain Res. 2019 DOI: 10.1016/j.bbr.2019.112118.
Схема деления и дифференцировки нейральной стволовой клетки. Зеленым показана спящая стволовая клетка, красным — активированная стволовая клетка, которая асимметрично делится с образованием «дочек» (круглые клеточки); «дочки» делятся симметрично, из их потомков развиваются новые нейроны, которые затем созревают. Cтволовая клетка, прошедшая через деление, превращается в астроцит (фиолетовый). | Behav Brain Res. 2019 DOI: 10.1016/j.bbr.2019.112118.
Мы довольно долго готовили публикацию, и когда вышла наша статья, одновременно вышла и другая работа, с иными выводами, и появилась редакционная статья в Cell под названием «Оптимистическая и пессимистическая модели деления клеток мозга». Наша была пессимистическая, потому что говорила, что во взрослом мозге стволовые клетки практически одноразовые — поделились и превратились в астроциты, и обратного пути нет, они уже не станут стволовыми и не станут производить новые нейроны.
Исходное число стволовых клеток не возобновляется?
Нет. В этом и состоит пессимистический момент. Получается, за счет того, что появляются новые нейроны, которые приносят пользу, их мать пропадает, и пул стволовых клеток постоянно истощается. Ранее уже было известно, что во взрослом мозге мыши постоянно снижается число рождающихся нейронов, но, как считалось, причина в том, что стволовые клетки становятся «плохими» и все хуже производят потомство. Это «оптимистическая модель», потому что, если стволовые клетки все же есть, то можно их как-то разбудить. А наша «пессимистическая» модель говорит о том, что число стволовых клеток падает, и именно поэтому становится меньше новых нейронов.
Хотя в реальности все немного сложнее. Чем старее мышь, тем меньше у нее стволовых клеток, но до нуля не доходит, так как скорость их исчезновения тоже уменьшается. Более того, мы обнаружили, что у старой стволовой клетки количество продуцируемого потомства на одну клетку увеличивается. То есть, мы пришли к довольно неинтуитивному выводу, что хотя общий пул стволовых клеток постоянно уменьшается, эффективность работы каждой стволовой клетки с возрастом увеличивается.
За счет чего это происходит, мы пока не знаем: то ли больше делений стволовых клеток, то ли больше делений их дочек и внучек, то ли меньше смерть потомства и т.д. Поэтому не исключено, что можно будет заставить имеющиеся стволовые клетки продуцировать еще больше нейронов. И второй вопрос: а нельзя ли как-то «разбудить» астроциты, которые совсем недавно были стволовыми клетками, и заставить их опять работать на производство новых нейронов? Есть разные потенциальные сценарии, каким образом можно это сделать, и мы этим сейчас занимаемся.
Интересная жизнь, больше движения и меньше стресса
Про факторы, которые стимулируют или подавляют нейрогенез. Насколько я понимаю, его стимулирует любое обучение, а также новые впечатления — все, что физиологи называют обогащенной средой?
Да. Когда мыши, из своей скучной жизни в клетке, попадают в какие-то новые условия, где больше новых предметов и больше возможностей побегать, полазать, зарыться, то у них резко подскакивает рождение новых нейронов. А при обучении всегда привносится что-то новое, так что в какой-то мере и обучение в процессе эксперимента можно считать обогащенной средой. Правда, люди всю жизнь не проводят в заключении, как мыши, в нашей жизни и так много разнообразия.
Но люди тоже могут его регулировать. Например, ребенка можно развивать, давать ему больше новых впечатлений. И в пожилом возрасте можно вести более активный образ жизни.
Да, это приходит на ум, но доказать, что у человека все это прямо воздействует на нейрогенез, не так просто. Потому что мы и так живем довольно разнообразной жизнью. Если вы пятилетнему ребенку еще что-то дадите, это в два раза увеличит у него нейрогенез или на 1%? Возможно, ребенок поглощает и запоминает такое огромное количество информации, что дополнительный выигрыш не так уж и велик, с точки зрения новых нейронов. Но не забывайте, что мы говорим именно о новых нейронах гиппокампа и связанных с этим функций; никто не поставит под сомнение, что безотносительно к этому ребенка нужно развивать и давать ему новые впечатления.
Наверное, это даже более актуально для пожилых людей.
Да, такое легче представить, хотя для людей все равно нет прямых доказательств. Но все, что мы знаем из опытов с животными, да и вообще по жизни, говорит о том, что чем более интересной и разнообразной жизнью в социальном смысле живет человек, тем дольше он сохраняет свои способности. Другой очень сильный стимул — физическая активность.
Да, физическая активность стимулирует нейрогенез, это убедительно показано на мышах. А известен ли механизм этого эффекта?
Их много. Это связано с метаболизмом, с тем, что ускоряется мозговой кровоток, появляются новые разные факторы роста, типа BDNF и т.д., которые, видимо, подстегивают потом деление новых клеток. Этим много занимаются и надеются, что смогут найти какой-то фактор, который поможет сделать лекарство, чтобы подстегивать деление стволовых клеток мозга, не истощая их. Это очень интересная область науки. Тонкий момент в том, что нет объективного способа у живого человека измерять нейрогенез. Иначе все было бы очень просто: помещаем человека в обогащенную среду и говорим, насколько повысился нейрогенез. Но реально такого метода нет, хотя многие лаборатории пробуют.
А факторы, которые подавляют нейрогенез? Мы уже поговорили про влияние возраста и болезни Альцгеймера. Что еще? Стресс?
Разные нейродегенеративные болезни – Альцгеймер в первую очередь, сильные воспаления (видимо, подавление происходит через NO), травмы головы, болезнь Паркинсона, судороги. Причем, при судорогах новые нейроны рождаются, но идут в неправильное место. Хронический стресс. В общем, все плохое коррелирует с падением нейрогенеза.
Если как-то получится поддерживать нейрогенез в пожилом возрасте, например, активным образом жизни, можно предотвратить развитие болезни Альцгеймера?
Есть такая надежда. При том, что остается большой вопросительный знак. Корреляция есть, интуитивно кажется, что да, так должно было бы быть, но доказать это сложно. Другая надежда на то, что если болезнь уже развивается, то можно замедлить ее развитие.
Почему антидепрессанты действуют не сразу
Поговорим теперь про то, как антидепрессанты связаны с нейрогенезом.
Есть такая идея, что депрессия связана со снижением нейрогенеза, а антидепрессанты его повышают. Эта идея появилась, в частности, потому, что нужно было объяснить, почему самые известные антидепрессанты, тот же прозак, начинают действовать не сразу, а через три-четыре недели. Если задуматься, то это довольно странно, ведь если вы выпьете бокал вина, вы тут же почувствуете его действие, а тут нужно несколько недель. Появилась идея, что антидепрессанты подстегивают рост новых нейронов, а пока они созреют — дойдут от стволовой клетки до нейрона — проходит три-четыре недели.
Эта идея сразу стала популярной, но доказать ее было довольно трудно. Считалось, что если появляется больше нейронов, значит должно быть больше стволовых клеток. Мы попытались в этом разобраться, имея в руках несколько линий трансгенных мышей, которые позволяли нам видеть подклассы нейральных стволовых клеток и их потомство. Наши опыты убедительно показали, что антидепрессанты увеличивают число новых нейронов, но пул стволовых клеток в этом не задействован, а увеличение числа нейронов происходит за счет клеток-«дочек». Обычно «дочка» проходит два-три деления, а под влиянием, например, прозака она проходит не два-три, а три-четыре деления, и нейронов становится больше. Мы предложили способ, которым можно проверить, на какой этап подействовал тот или иной агент — антидепрессант или физические упражнения. В этом была новизна. Эта статья стала очень популярной.
Почему это было важно? Как мы обсуждали раньше, если рождаются новые нейроны, когда ты бегаешь или принимаешь антидепрессанты, но при этом ты истощаешь свой пул стволовых клеток, то и нейрогенез у тебя закончится раньше. Но мы показали, что антидепрессанты, физические упражнения и другие хорошие стимулы действуют «ниже по течению» — на «дочек», и увеличивают число новых нейронов, не истощая при этом пул стволовых клеток, так что нет опасности опустошить его раньше времени. Хорошо. Есть еще другие лекарства, например мемантин, средство от болезни Альцгеймера, и мы знали, что оно подстегивает нейрогенез. Но оказалось, что оно действует именно на стволовые клетки и рекрутирует в деление те клетки, которые в норме не должны были бы делиться, и это может привести к их раннему исчезновению. Сейчас мы пишем статью, что при долгом введении мемантина сначала появляется очень много нейронов, но потом их количество падает, и пул клеток опустошается.
Но мемантин — это именно лекарство от болезни Альцгеймера. И если у пожилого пациента сейчас улучшается состояние, а лет через 20–30 ему станет хуже, то это не так уж важно. Другое дело, что это лекарство принимают не только пациенты с деменцией, но и молодые люди, которые используют его как стимулирующее средство. А это уже совсем другой вариант, и перспектива остаться без новых нейронов должна очень тревожить.
Я у вас видела статью , которая связывает нейрогенез, возраст и ограничение калорий. Может ли ограничение калорий, которое, как многие считают, тормозит возрастные изменения, стимулировать нейрогенез?
Да, ограничение калорий может стимулировать нейрогенез. Эта идея витала, потому что долгие голодания, ограничения калорий улучшают самые разные функции организма. Логично предположить, что и мозг — тоже. И мы показали, что если ограничивать калории мышам, то нейрогенез у старых мышей продолжается значительно дольше.
А еще стволовые клетки мозга участвуют в регенерации поврежденных зон мозга, так?
Эта идея появилась довольно давно. У животных есть очень много стволовых клеток, которые мигрируют в направлении обонятельной луковицы, производят новые нейроны. И когда в эксперименте животным наносили небольшое повреждение мозга, клетки отклонялись от своего пути и пытались пойти туда и залечить повреждения. Эти наблюдения породили большие надежды, что можно будет так лечить травмы, инсульты и т.д. Реально это оказалось более сложно, чем в теории: клетки туда идут, но из них получается мало нейронов: они начинают делиться, а потом или умирают, или превращаются в астроциты. И эффективного способа использовать это явление для лечения повреждений мозга, хотя бы на животных, пока нет. Хотя лаборатории все равно пробуют, потому что очень уж это привлекательная идея. В общем, какой-то регенеративный потенциал у взрослого мозга есть, безусловно. Вопрос, как его разбудить и улучшить когнитивные функции, не вызвав при этом бесконтрольный рост клеток и образование опухоли.
«Он видел свою миссию в поддержании духа новизны»
Я прочитала, что в Лабораторию Колд-Спринг-Харбор вас пригласил Джеймс Уотсон. Как это произошло?
Он пару раз приезжал в Москву. Вообще, ему все русское очень нравилось, и люди тоже. Он знал нескольких ученых в Москве, посетил их лаборатории, в том числе лабораторию моего учителя Георгия Павловича Георгиева в Институте молекулярной биологии. Мы, несколько человек, рассказали Уотсону о своей работе, и он предложил мне написать о том, что бы я хотел делать. Я написал — и он пригласил меня в Лабораторию Колд-Спринг-Харбор, которой он тогда руководил, это было в самом конце 1988 года. Я думал, что проработаю там года два-три и вернусь в Москву. Но потом все изменилось, наука стала разрушаться, и уже некуда было возвращаться.
В Лаборатории я долго работал как visiting scientist, не на постоянной позиции. Потом я сделал доклад по функциям NO, это была первая наша работа. Уотсону очень понравилось, и в перерыве после моего доклада он подошел и предложил мне «позицию». Я, конечно, согласился, и во время второго перерыва он сходил в отдел кадров, а на третьем ко мне подошли и сказали, что все сделано. Сработала такая вертикальная конструкция, которую он создал в лаборатории.
Вообще, он практически с нуля создал Лабораторию Колд-Спринг-Харбор, которая, хотя существует уже 150 лет, но знаменитой, настоящей меккой молекулярной биологии, стала после прихода Уотсона. Он приехал в Колд-Спринг-Харбор, маленький городок около Нью-Йорка, в 1968 году, после своей поздней женитьбы, и создал ее буквально так, как ему хотелось. Все его поручения тут же выполнялись, это была такая пирамидальная схема, идеально приспособленная для занятия наукой. К тому же Лаборатория тогда была маленькая, сейчас она стала намного больше.
По вашим словам можно понять, что Уотсон — человек авторитарный? Как было работать под его руководством? Какой он в личном общении?
Нет, он совсем не авторитарный, просто он хотел создать место, где ученые занимались бы наукой с полной отдачей, не отвлекаясь ни на что, и вся структура Лаборатории должна была работать на это. Он же организовал серию конференций и курсов в Лаборатории, которые скоро стали очень популярными. И результат — нобелевские открытия, вышедшие из стен Лаборатории и огромное число людей, которые ностальгически вспоминают свой первый доклад или годы работы в ней.
Уотсон не был руководителем в обычном понимании, он скорее видел свою миссию в поддержании духа новизны, нацеленности на важное, ощущения, что крупное открытие где-то совсем рядом, за углом. После его докладов хотелось быстрее бежать и начинать какой-то опыт или пересмотреть свои результаты — может, там было что-то важное, что сразу не заметил. Он все время придумывал новые модели, предлагал что-то проверить, и обычно интуиция его не обманывала. Общаться с ним очень легко, если ты тоже заточен на науку — можно было в любое время к нему подойти и сказать: «Джим, а что ты думаешь по поводу того-то?», и он сразу включался в обсуждение. У нас и сейчас с ним остались теплые отношения, и мы часто видимся.
Лаборатория стволовых клеток мозга в МФТИ образовалась по мегагранту в 2011 году. Ее работа была связана с Лабораторией в Колд-Спринг-Харбор?
Да, я построил московскую лабораторию так, чтобы было очень тесное сотрудничество с американской. В моей колд-спринг-харборовской группе побывало больше десятка человек, и все они потом возвращались в Москву и продолжали работать над проектами.
Когда мегагрант кончился, что произошло с лабораторией в МФТИ?
По правилам мегагранта тебе дают деньги на два с половиной года, потом можно немного его продлить, но предполагалось, что лаборатория перейдет на подножный корм и будет сама обеспечивать свою работу. Но это было не очень реально, потому что слаженная экспериментальная биологическая лаборатория формируется, конечно, намного дольше, и настоящий научный выход начинается позже. Мы сделали то, что смогли, но поддержка становилась все меньше. Но зато удалось создать сразу несколько независимых групп, а оставшиеся перешли в МГУ, в Институт перспективных исследований мозга, который возглавляет Константин Анохин, мой старый друг и соавтор.
Особенно тесно мы сотрудничаем с Александром Лазуткиным, очень талантливым ученым, который сейчас работает в Институте высшей нервной деятельности. У него там группа, которая потом, надеюсь, станет лабораторией; у нас идет сразу несколько совместных проектов. Саша у меня здесь был раза три, последний раз на два года застрял из-за ковида. Правда, сейчас вообще непонятно, что будет и как.
То, что сейчас происходит, сильно ударило по вашим контактам?
Во-первых, люди разъезжаются. Спрашиваешь: «Где Маша?» — «В Вильнюсе». — «Где Оля?» — «В Ереване». Хочется думать, что временно, но кто знает... Во-вторых, ничего не купишь. Для экспериментальной молекулярной биологии нужны тонкие реагенты, антитела и прочее, что нельзя просто заменить. У нас за годы работы накопились результаты, мы их будем описывать, но все это может прийти к завершению.
Гены, сети нейронов и мозг
Григорий Николаевич, напоследок еще один вопрос про науку. Есть ли в современной нейробиологии полное понимание работы мозга на генетическом уровне? Я лет двадцать назад впервые услышала от Константина Анохина о гене c-fos и других генах раннего ответа, которые экспрессируются в ответ на любой новый стимул, запускают другие гены, и таким образом геном участвует в обучении и памяти. Изменилась ли эта картина сейчас?
Сложный вопрос. По большому счету ясности нет, хотя, конечно, прогресс удивляющий. Сейчас появляется огромное количество работ, обычно от очень больших коллективов, которые делают полное описание, например, экспрессии генов во всех типах нейронов у мыши или у человека. Например, полный РНКовый или белковый профиль нейронов черной субстанции (скопление нейронов, богатых дофамином, в области среднего мозга. — Н.М.). Такие работы важны для создания огромных каталогов экспрессии генов в мозге, к которым можно при необходимости обратиться. Но по-прежнему лежит пропасть между нашим знанием генов и клеток в мозге и пониманием того, как же они взаимодействуют, чтобы вызвать какую-либо поведенческую реакцию.
Что касается гена c-fos, у Константина была отличная идея, которую он высказал давно и которая оказалась очень плодотворной. Он предположил, что экспрессию c-fos можно рассматривать как маркер активации нейрона. Это стало самым распространенным способом взглянуть, какие нейроны активируются при том или ином поведении. Например, когда пытаются понять какое-то поведение у мышей — подносят самку или детеныша, или заставляют драться, — то в первую очередь смотрят, где появились c-fos-положительные клетки. Значит, эта область мозга была задействована в ответ на этот стимул. И от этого можно начинать подробное исследование — манипулировать нейронами в этой области, активировать их или ингибировать и смотреть, как это скажется на поведении. Практически, это стало первым этапом для всех работ по изучению нейрональных сетей, которые управляют тем или иным поведением. Мы тоже пользуемся этим подходом для выявления нейрональных сетей, отвечающих за социальное поведение и агрессию, — регистрируем все нейроны во всем мозге мыши в 3D измерении, которые активировались при ее победе или поражении в драке. И потом пытаемся эти трехмерные карты сравнивать друг с другом и находить связи между участками мозга и группами нейронов, которые управляют этим поведением.
Вы используете зеленый флуоресцентный белок?
Можно и так. Но обычно мы просто смотрим на эндогенный белок, это оказалось легче, чем следить за флуоресцентным белком. Просто нужно, чтобы весь мозг равномерно пропитался антителами, и тогда можно увидеть, где экспрессируется c-fos. Методы для этого уже появились. Хотя можно было бы и к промотору гена c-fos привязать ген зеленого белка, и тогда смотреть за ним.
А оптическую регистрацию с оптоволокном вы не используете?
Используем, конечно, как и другие методы, для конкретных задач. Проблема такая — все нынешние методы очень мощные. Когда ты хочешь что-то наблюдать в конкретном участке мозга: ты вводишь стеклянный электрод с оптоволокном и рассматриваешь то, что тебе надо, или манипулируешь этим участком. Но ты не можешь смотреть за всем мозгом сразу. Наши главные усилия сейчас прилагаются к тому, чтобы увидеть распределение всех активированных участков в целом мозге в 3D и потом сравнивать полные наборы нейронов, которые активируются при разном поведении. Это уже вычислительный аспект работы, и здесь очень много зависит от тесного взаимодействия с математиками.
Я знаю, что у Константина Анохина есть концепция «когнитома» как модели сознания, но это отдельная история. Нейрональные сети, о которых вы говорили, — подход к этому, попытка понять работу целого мозга?
Да, да. Это нынешний этап развития нейробиологии. Сначала изучали области мозга, потом — гены, потом нейроны, а сейчас всех интересует, как одни нейроны мозга связаны с другими и как взаимодействие между нейрональными сетями определяет поведение. Вот главный вопрос, над которым сейчас стоит работать.


 Меню
Меню





 Все темы
Все темы




 0
0










