Нобелевская неделя 2025. Фред Рамсделл о регуляторных Т-клетках и лечении ревматоидного артрита
«Мы не хотим лечить заболевания. Мы хотим их вылечить, перезагрузив иммунную систему в нормальное состояние, в котором она находится у большинства из нас. Это наша цель. Амбициозная, но я не думаю, что недостижимая». — Лекция лауреата Нобелевской премии 2025 года по физиологии или медицине Фреда Рамсделла. Стокгольм, 7.12.2025.

Скриншот канала Нобелевского комитета
Перед началом лекции Фред Рамсделл рассказал о выставке в Нобелевском музее, на которой в этом году представлены платья, символически изображающие достижения лауреатов. Одно из платьев, посвященное исследованиям регуляторных Т-клеток, отражало в своем дизайне связывание Т-клеточного рецептора с молекулой MHC. «Видимо, даже дизайнеры платьев в Стокгольме много знают об иммунологии», — заметил нобелевский лауреат.
 Очевидно, пояс юбки — это рецептор
Очевидно, пояс юбки — это рецептор
В 1960 году Макфарлейн Бёрнет и Питер Брайан Медавар получили Нобелевскую премию по физиологии или медицине за открытие приобретенной иммунной толерантности и способности организма человека контролировать иммунный ответ на собственные ткани. «Так получилось, что это был год моего рождения. Шестьдесят пять лет спустя еще одна Нобелевская премия отмечает этот же феномен. Это потрясающе. Потрясающе быстро или потрясающе медленно. Я довольно нетерпелив, так что для меня скорее медленно».
Рамсделл немного рассказал о мышах линии scurfy, с которыми работали он и Мэри Брункоу. Одной из их особенностей была гиперреактивность — отобранным у них лимфоцитам требовался всего один внешний сигнал чтобы начать пролиферацию, в отличие от двух сигналов для обычных клеток. В то же время трансгенные мыши, несущие ген Scurfin (FOXP3), наоборот, демонстрировали гипоактивность Т-клеток.
В работе Симона Сакагути была описана небольшая популяция T-клеток, экспрессирующих поверхностные белки CD4 и CD25 — регуляторные Т-клетки (Treg). Роли Кхаттри изолировала эти клетки и показала, что это единственная группа клеток крови, экспрессирующая FoxP3. «Для меня это стало откровением, — сказал Фред Рамсделл. — Мы не только получили молекулярный маркер для этих клеток. Для меня это значило также, что именно этот ген ответственен за формирование этой конкретной линии и за ее функционал».
Так, стимуляция иммунных клеток обычно вызывает их ответ. Добавление в систему регуляторных Т-клеток подавляет этот ответ, а добавление Т-клеток, не относящихся к регуляторным, — наоборот, повышает. У Foxp3 трансгенных мышей иммунные клетки, которые обычно не обладали подавляющим эффектом (CD4+CD25– и CD8+), становились функционально аналогичными Treg. Таким образом, экспрессия Foxp3 в любых лимфоцитах активирует в них регуляторную программу.
Было известно, что регуляторные Т-клетки происходят из тимуса. Исследователи решили проверить, что будет, если у трансгенных мышей scurfy вызвать экспрессию Foxp3 только в тканях тимуса. Оказалось, что такой локализированной экспрессии недостаточно для восстановления нормального фенотипа, то есть для нормального развития организма необходима периферическая экспрессия Foxp3. В дальнейших опытах Александр Руденский создал линию мышей, у которых можно генетически «включать и выключать» экспрессию Foxp3. Эти исследования показали, что «включение» гена у Scurfy мышей в возрасте четырех недель обеспечивало почти полное восстановление нормального фенотипа и существенное снижение воспаления.
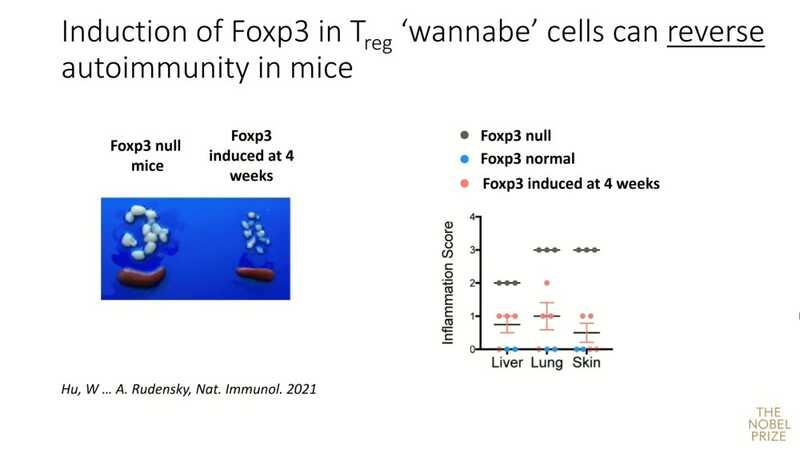 На фото, сверху вниз — лимфоузлы, селезенка и тимус мышей без Foxp3 и мышей с индуцируемым Foxp3 через 4 недели после введения индуктора
На фото, сверху вниз — лимфоузлы, селезенка и тимус мышей без Foxp3 и мышей с индуцируемым Foxp3 через 4 недели после введения индуктора
Таким образом, продукт этого гена необходим для иммунной толерантности и способности контролировать иммунный ответ на периферии — именно то, что нужно для лечения аутоиммунных заболеваний.
При всей своей важности как регулятора Foxp3 — ужасная терапевтическая мишень. Попытки разработать методы увеличения числа Treg клеток или улучшить их активность не увенчались успехом. (При этом параллельно велась и ведется работа в обратную сторону — по деактивации Treg клеток в тканях рака для повышения его уязвимости к иммунному ответу, отметил Рамсделл.)
«Мы решили, что раз мы не можем воздействовать на [Foxp3] классическими методами, нам надо наконец опубликовать эти данные, выпустить их в мир, чтобы все остальные могли над этим работать. Что мы и сделали. И множество людей помогло нам и в 2004–2010 годах мы узнали многое о том, как эти клетки работают… Мы также узнали, что эти клетки присутствуют во всех тканях нашего тела. На самом деле одной из причин, почему это был последний ген, который мы секвенировали, — были данные о том, что он экспрессировался во всех тканях на очень низком уровне. И я думал “Это глупо. [Этот ген] не может вызывать это заболевание”. Что, конечно, оказалось абсолютно неверным». [Область Х-хромосомы мыши, мутации в которой были ассоциированы с фенотипом scurfy, — симптомами тяжелого аутоиммунного заболевания у самцов, — содержала 20 генов, которые Рамсделл и Брункоу секвенировали по очереди, так как в 1990-е годы это было нетривиальной задачей. Ген Foxp3 оказался последним. — PCR.NEWS.]
Кроме модуляции иммунного ответа, Treg клетки поддерживают гомеостаз в тканях еще многими путей, включая влияние на регенерацию тканей. «Это как на месте происшествия одновременно полиция прекращает то, что пошло не так, и медики останавливают кровотечения и сохраняют людям жизни», — сказал Фред Рамсделл.
Также в процессе исследования Treg в 2000х годах были разработаны эффективные методы их идентификации и изоляции, сначала на мышах, а потом и на человеке. В том числе были проведены опыты по изоляции Treg клеток у пациентов, культивированию клеток в лаборатории и пересадке обратно пациенту с сохранением функционала клеток. Негативных последствий не было, однако особой клинической пользы от такой процедуры также не было, то есть простой подход «больше клеток» оказался неэффективным.
В 2019 году Джефф Блюстоун вместе с Цичжи Танг, Александром Руденским и Фредом Рамсделлом основали биотехнологическую компанию Sonoma Biotherapeutics, чтобы использовать природные механизмы контроля иммунного ответа для лечения заболеваний.
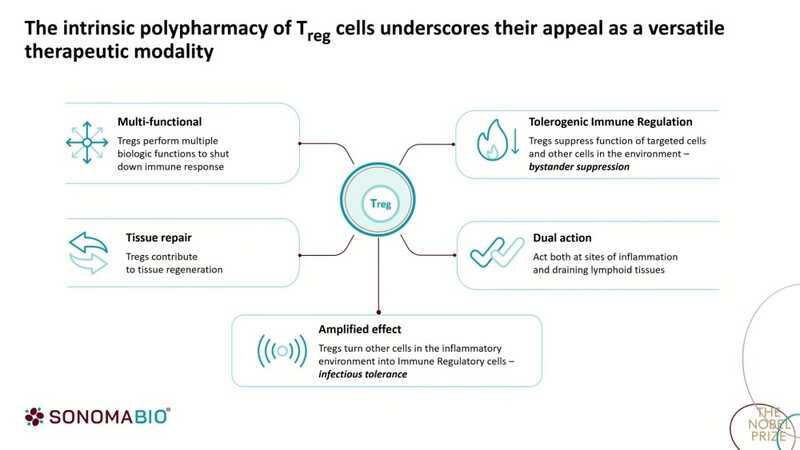
«По сути, мне не нужно быть умным. Мне просто надо использовать нужную клетку», — объяснил лектор принцип этого подхода. Использование Treg в качестве активного агента в лекарствах дает возможность извлекать преимущество из их многофункциональности, создавая препараты широкого спектра действия. Схожими исследованиями занималось и множество других компаний.
Работа SonomaBio началась с ревматоидного артрита (РА). По этому заболеванию имелось множество доклинических данных о способности Treg клеток восстанавливать нормальный фенотип и предотвращать развитие патологии. У пациентов с РА также снижена активность Treg клеток в сравнении со здоровыми контролями. Ученые решили проверить, можно ли взять эти дефектные Т-клетки от пациента и восстановить их активность в лабораторных условиях. И действительно, в культурах Treg клетки пациентов с РА показывали уровень активности и экспрессии FOXP3, близкий к нормальным.
Чтобы повысить эффективность Treg для лечения РА, их сделали специфичными к цитруллинированным белкам, которые образуются в процессе воспаления; их много в пораженных суставах при РА. В качестве метода обеспечения специфичности был выбран CAR — метод, хорошо разработанный в терапии онкологических заболеваний. При конструировании CAR узнающая антиген часть антитела соединяется с сигнальным доменом, и получившаяся система интегрируется в терапевтические клетки, в данном случае в Treg клетки.
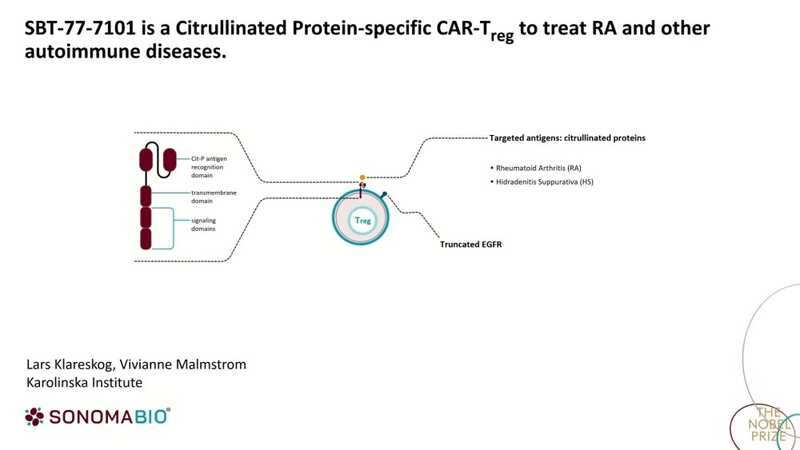
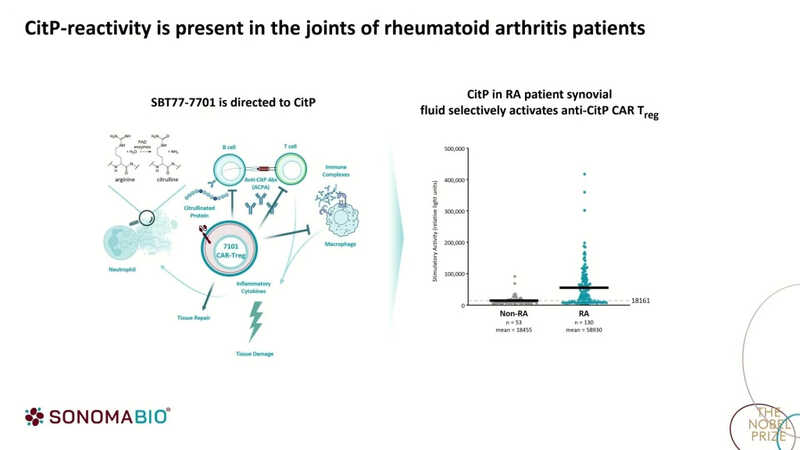
Эта работа была проведена в сотрудничестве с Ларсом Кларескогом и Вивианной Малстром из Каролинского института. Модифицированные Treg реагировали на изолированные цитруллинированные белки и синовиальную жидкость от пациентов с РА активнее, чем немодифицированные клетки. При этом не нарушались их функциональность и профиль экспрессии генов.
Для производства препарата у пациента берут кровь, из нее изолируют Treg клетки, которые затем культивируют и трансдуцируют вирусом, вносящим ген CAR. За 14 дней культивации удается получить миллиарды модифицированных клеток, которые затем вводят пациенту. При этом оказалось, что после выращивания в культуре клетки экспрессируют ключевые гены даже активнее, чем до модификации.
В настоящее время проводится клиническое исследование первой фазы, направленное в первую очередь на установление безопасности такого лечения. Уже были проведены тесты малой и средней дозы (по три пациента для каждого уровня). Рамсделл подчеркнул, что все шесть пациентов ранее получали как минимум четыре разных по механизму действия терапии, ни одна из которых не оказала эффекта.
В результате терапии модифицированными Treg клетками у пациентов, хотя и в разной степени и не у всех, наблюдался ответ на терапию — уменьшение числа пораженных суставов. Хотя у некоторых улучшение оказалось временным, у других ответ сохранялся до 24 недель. «У нас также есть анекдотичные свидетельства эффективности. Пациенты теперь могут открыть банку, что не могли сделать последние пять лет. У нас были пациенты, которые занялись бегом, чего не могли делать последние пять лет. Это немного, но я нахожу это очень обнадеживающим», — сказал Фред Рамсделл.
Некоторым пациентов выполнили ультразвуковые исследования и биопсию. Через 4–6 недель после инфузии клеток у ряда пациентов значительно снизились объемы воспаленной ткани. В некоторых случаях индекс воспаления снижался с 9 (максимально возможное значение) до 2. Результаты биопсии подтвердили присутствие модифицированных Treg клеток в синовиальной жидкости суставов.
Итак, спустя 65 лет после вручения Нобелевской премии за открытие периферической толерантности еще одна премия вручается за понимание и использование ее механизмов. По мнению Рамсделла, в ближайшие несколько лет наше понимание работы регуляторных Т-клеток станет глубже, что позволит разработать более эффективные методы терапии.
«Мы не хотим лечить заболевания. Мы хотим их вылечить, перезагрузив иммунную систему в нормальное состояние, в котором она находится у большинства из нас. Это наша цель. Амбициозная, но я не думаю, что недостижимая».
В конце лекции Рамсделл выразил благодарности множеству коллег. Отдельно он упомянул Дэвида Галаса, Мэри Брункоу, Стива Зиглера, Роли Кхаттри, сотрудников SonomaBio — Джеффа Блюстоуна, Джоша Билке, Мей-Лун Ванг, а также клинических исследователей, пациентов, своих наставников Сидни Голуба и Би Джей Фаулкс, лабораторных мышей и свою жену Флору.
В заключение Рамсделл вспомнил, как в 2002 году посетил Каролинский институт, и показал фотографию, где он стоит возле трейлера с логотипом нобелевского музея. «Я часто бываю неправ. И в 2002 году, когда была сделана эта фотография я сказал: “Смотрите, ближе к Нобелевской премии я никогда не буду”. Судя по всему, я был неправ».



 Меню
Меню





 Все темы
Все темы




 0
0











