Анализ клеток на новом уровне: путь к индивидуализированной терапии рака через технологии секвенирования
Анализ единичных клеток активно используется в онкологии как инструмент персонализированной медицины. Он предоставляет исследователям точные данные о генетических, эпигенетических, транскриптомных, протеомных и метаболических особенностях каждой клетки. Российские исследователи сравнили две технологии анализа транскриптома единичных клеток. Одна из них наиболее широко представлена на рынке — это 10x Genomics, варианты анализа 3’- и 5’-транскриптомов. И вторая технология, которая появилась достаточно недавно, в том числе и в России, — это технология компании SeekGene для анализа транскриптома полной длины.

Сергей Владимирович Попов, заведующий лабораторией общей, молекулярной и популяционной генетики ГНЦ ФГБУ «НМИЦ эндокринологии» Минздрава России, представил доклад «Сравнительный анализ технологий секвенирования единичных клеток в онкологии».
erid: 2VfnxxD1KhA
Сравнение технологий 10x Genomics и SeekGene в реальных условиях провели сотрудники лаборатории общей, молекулярной и популяционной генетики ФГБУ «НМИЦ эндокринологии» Минздрава России. Доклад на эту тему представил на конференции «Биохимия человека 2024» заведующий лабораторией Сергей Попов.
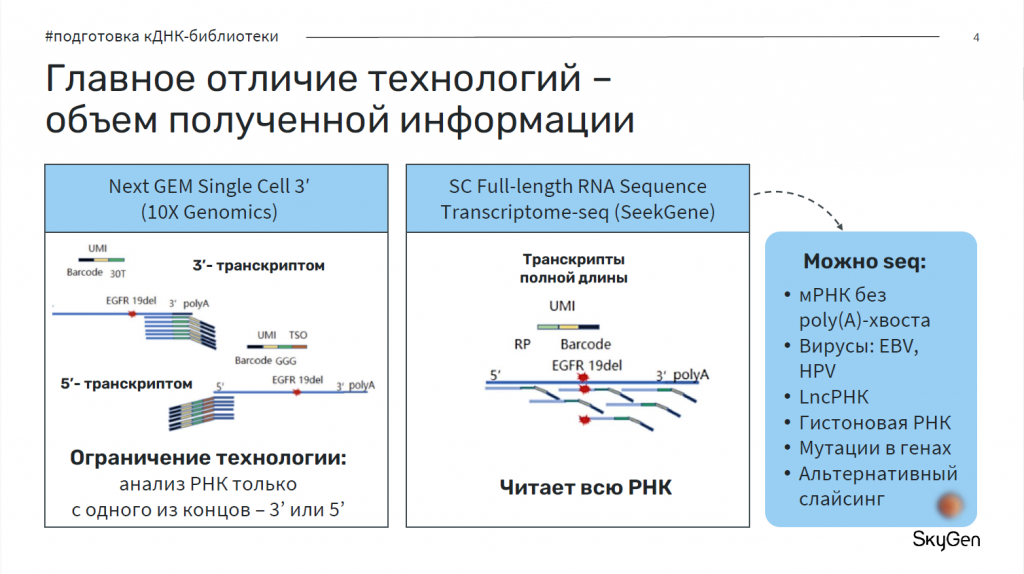
Исследователи отобрали образцы адренокортикальной опухоли, охарактеризовали их гистохимически и диссоциировали. Они подготовили кДНК-библиотеки с использованием технологии SC Full-length RNA Sequence Transcriptome-seq (SeekGene) и Next GEM Single Cell 3’ (10x Genomics). Секвенирование осуществили на платформе Illumina Novaseq 6000. Анализ данных включал фильтрацию, кластеризацию и интеграцию. Дальше анализировали данные с помощью специальных пакетов, в частности, широко известного пакета Seurat, провели анализ динамики РНК экспрессии (velocito.R), CNV-анализ (Numbat), анализ регулонов (SCENIC) и дифференциальной экспрессии (KEGG, Seurat).
В процессе секвенирования единичных клеток каждая клетка связывается с гелевой частицей, несущей молекулярные баркоды, которые метят саму клетку, и баркод UMI, который метит транскрипт. В ходе анализа можно оценить уровни экспрессии генов в индивидуальных клетках и их гетерогенность.
Технология 10x Genomics ограничена только одним концом мРНК — 3’ или 5’-концом. А технология SeekGene позволяет изучить мРНК без поли(A)-хвоста, экспрессию генов вирусов (EBV, HPV), длинные некодируемые РНК, гистоновые РНК, мутации в генах и альтернативный сплайсинг.
Первым этапом было ранжирование баркодов. У обеих технологий количество прочтений на клетку было сопоставимым. Однако распределение баркодов на SeekOne вышло на 10% больше 10х, что говорит о получении большего количества информации с клетки.
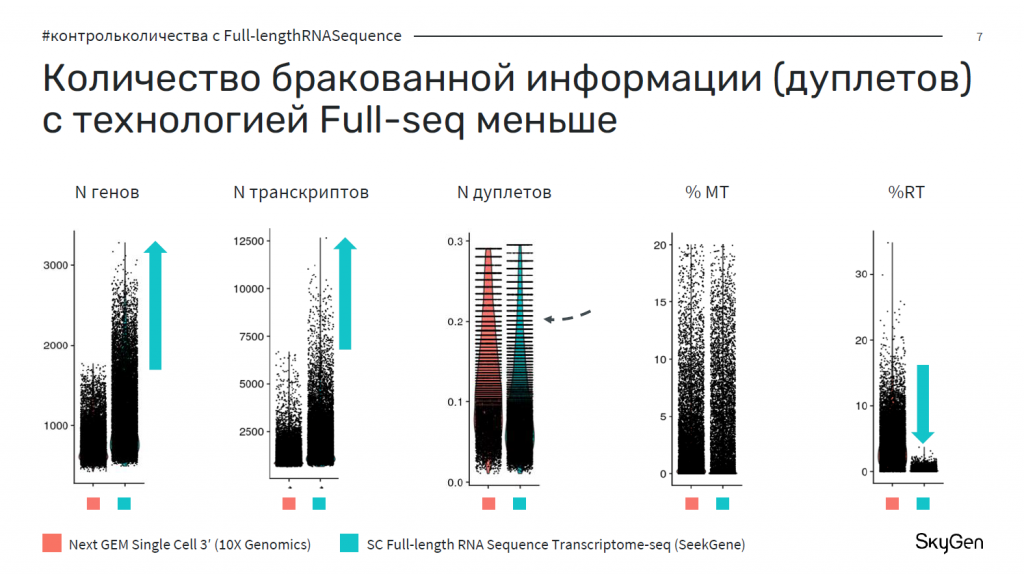
Следующий этап — контроль качества секвенирования. Прежде всего посмотрели соотношение общего количества генов и транскриптов, и соотношение количества митохондриальных генов и транскриптов получилось сопоставимым. Однако количество обработанной информации по SeekOne было больше, чем у 10х. С другой стороны, количество дуплетов — бракованной информации — по отношению к количеству генов было значительно выше у 10х. Особый интерес вызвало соотношение количества рибосомальных генов и транскриптов. В случае SeekGene оно получилось гораздо меньшим — не превышало 1%. Это происходит благодаря использованию в технологии SeekOne блокаторов рРНК, которые необходимы для снижения «спам»-информации.
Биотипирование транскриптов провели в сравнении с референсной базой данных. С технологией SeekGene картируется примерно такое же количество кодирующих белки транскриптов, что и с технологией 10x, это же касается количества митохондриальных РНК. А вот количество некодирующих РНК в SeekGene намного больше. Это объясняется тем, что SeekGene использует рандомные праймеры. Такой подход позволяет детектировать все неполиаденилированные фрагменты, в отличие от технологии 10x, которая нацелена на поли(А)-транскрипты.
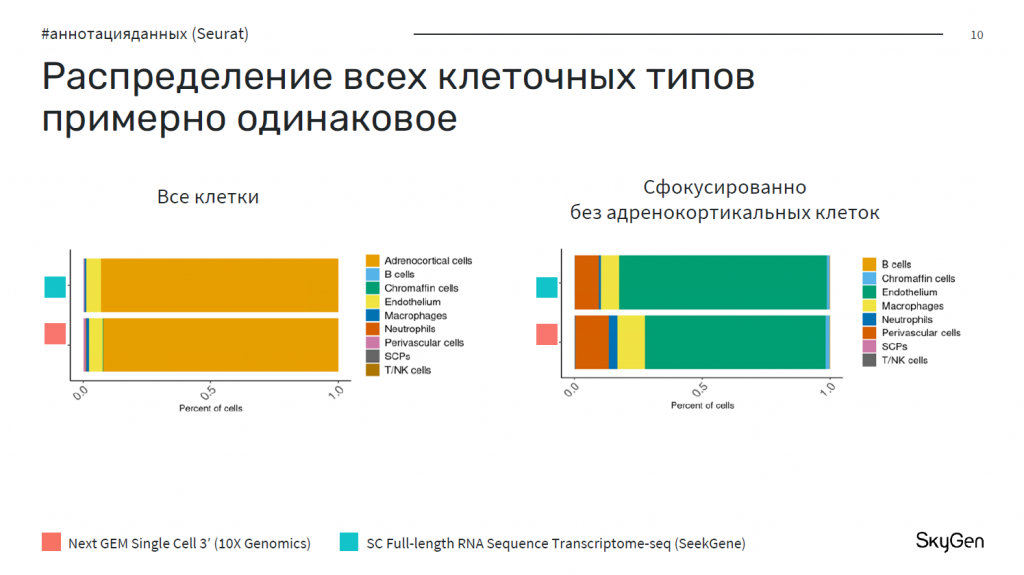
При анализе данных (Seurat) распределение всех клеточных типов было примерно примерно одинаковым. В качестве референса также взяли базовые данные. Все основные клеточные типы были представлены при использовании обеих технологий. И та, и другая технология показывают, что образец более чем на 90% состоит из аденокортикальных клеток. Если их убрать и сфокусироваться на остальных типах клеток, то распределение также не сильно отличается.
Анализ экспрессии основных маркеров выявил отличия технологий. С помощью той и другой технологии получили списки топ-500 маркеров. Они пересекались только на 23,2% (188 маркеров были общими).
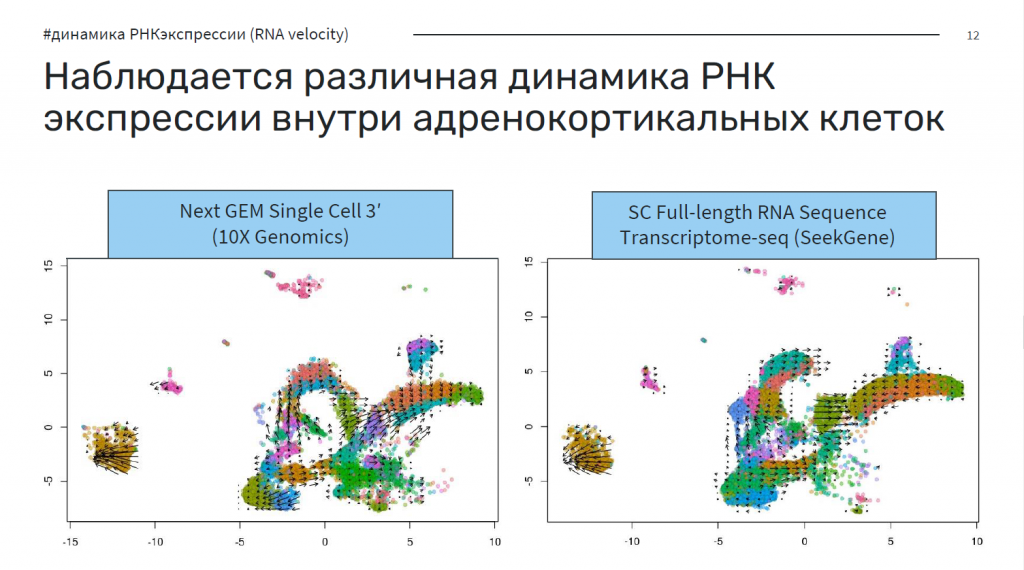
Анализ RNA velocity показал соотношение сплайсированных и несплайсированных вариантов в динамике. Если в образце больше сплайсированных вариантов, то клетка исчерпала свой потенциал для дальнейшего роста и развития. Обе технологии позволяют четко отслеживать наличие динамики РНК-экспрессии.
В ходе следующего анализа — анализа дифференциальной экспрессии (KEGG, Seurat) — были выявлены отличия в активации различных сигнальных путей. Например, активация пути синтеза и секреции кортизола видна при использовании обеих технологий, а дофаминергических синапсов – только на SeekGene.
С помощью анализа регулонов (SCENIC) изучили взаимосвязь между экспрессией ключевых генов и факторами транскрипции. Технология SeekGene позволила выявить ряд транскрипционных факторов, не обнаруженных с помощью 10 х, например, ZEP1, который играет важную роль при эпителиально-мезенхимальной трансформации.
Распределение CNV-мутаций (Numbat). Технология SeekGene выявила на первой хромосоме нейтральную потерю гетерозиготности, когда общее число транскриптов не менялось, и сбалансированную делецию. Все транскрипты объединили в псевдобалк, при его анализе видно, что в датасете SeekGene зарегистрировано больше вариантов CNV-событий.

Таким образом, технология full-seq позволила получить большее количество информации и точных данных по экспрессии генов, анализу CNV и сигнатуре сигнальных путей. Обе технологии применимы для анализа образцов адренокортикальной опухоли и позволяют получать данные по клеточным типам и динамике РНК-экспрессии.
В ответ на вопрос из зала докладчик пояснил, что в клинике технологии секвенирования единичных клеток пока не применяются. Сейчас в онкологии себестоимость одного подобного исследования — около 250 тыс. рублей. В то же время эти технологии позволяют увидеть переходные клеточные состояния, найти популяции клеток — предшественников развития рака. Можно построить траектории развития, клональные деревья, определить, в каких клетках происходят мутации, показать корреляцию мутирования со структурой органа, проверить гипотезу о том, что есть определенный клон клеток, который даст начало онкотрансформации. А дальше найденные маркеры помогут в персонализированной терапии онкологических заболеваний.
SkyGen — эксклюзивный дистрибьютор SeekOne в России. Напишите свой запрос на info@skygen.com
Реклама. Рекламодатель ООО «СКАЙДЖИН» ИНН 7705997147


 Меню
Меню





 Все темы
Все темы



 0
0