Антибиотик, отвергнутый из-за токсичности, показал хорошие результаты после очистки
Противомикробный препарат стрептотрицин, выделенный в 1942 году, оказывал токсическое действие на почки, в результате его исследования были заброшены. Сейчас нам известно, что тот стрептотрицин был смесью различных соединений. Американские ученые исследовали хроматографически очищенные стрептотрицины D и F и продемонстрировали их безопасность для мышей в клинически релевантных концентрациях. Они также показали, что механизм действия стрептотрицина отличается от других антибиотиков, взаимодействующих с рибосомами прокариот.
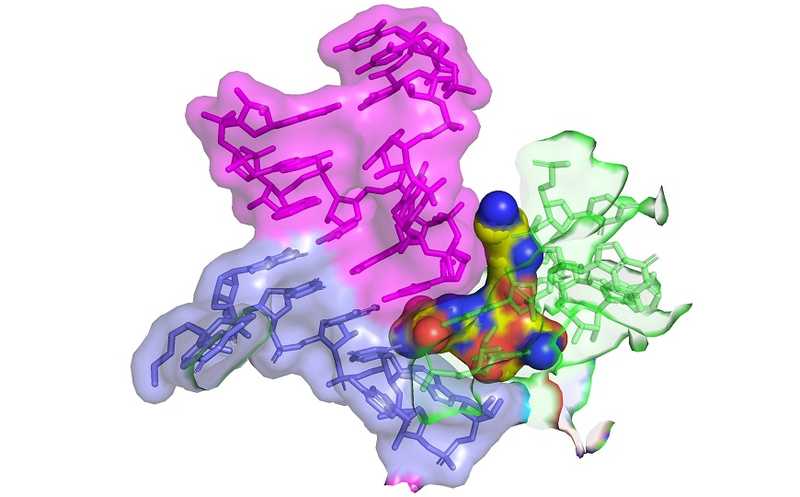
Стрептотрицин F (желтые сферы) связывает 16S рРНК (зеленая) бактериальной рибосомы. Розовым обозначена тРНК, а голубым — мРНК.
Credit:
James Kirby ( CC-BY 4.0; Zoe L Watson et al., 2023, eLife, CC-BY 4.0) | Пресс-релиз
Быстрое развитие устойчивости к антибиотикам — основная проблема терапии бактериальных инфекций. Особую сложность представляет лечение резистентных к карбапенемам Enterobacterales (CRE) и Acinetobacter baumannii. Есть необходимость в поиске новых антибактериальных препаратов. Американские исследователи обратили внимание на старый препарат стрептотрицин. Он был получен в 1942 году из почвенной бактерии Actinomyces и сначала вызвал всеобщее воодушевление благодаря своей способности селективно уничтожать грамотрицательные микроорганизмы и Mycobacterium tuberculosis. В опытах на животных препарат полностью излечил морских свинок от Brucella abortus, а мышей — от Salmonella paratyphi B. Но в испытаниях на людях он продемонстрировал токсичность для почек, после чего опыты с ним забросили.
Однако в настоящее время известно, что стрептотрицин на самом деле — это смесь, которую теперь называют норсеотрицин (nourseothricin), и что токсичность компонентов смеси варьирует. В новой работе авторы изучили активность, безопасность и механизм действия двух основных компонентов норсеотрицина — стрептотрицинов D и F, очищенных до гомогенности с помощью хроматографии.
Сначала исследователи определили минимальную ингибирующую концентрацию (minimum inhibiting concentration, MIC) стрептотрицинов F и D, а также норсеотрицина для большой группы CRE со множественной лекарственной устойчивостью. MIC50 и MIC90 составили 2 и 4 μM для стрептотрицина F, 0,25 и 0,5 μM для стрептотрицина D, 0,5 и 1 μM для норсеотрицина. Средняя MIC для стрептотрицина F была в 5,6 раза выше, чем для стрептотрицина D, и в 4,2 раза выше, чем для норсеотрицина. Анализ коммерчески доступного норсеотрицина показал, что смесь состоит из 65,5% стрептотрицина F, 29,6% стрептотрицина D и 4,9% стрептотрицина E.
В опытах на резистентном CRE изоляте K. pneumoniae Nevada (AR-0636) было показано, что бактерицидная активность стрептотрицина F и норсеотрицина проявлялась в течение двух часов в концентрации, в четыре раза превышающей MIC. Схожие результаты были показаны для изолята A. baumannii MSRN 1450, резистентного к карбапенемам.
На прокариотических и эукариотических in vitro системах для транскрипции-трансляции авторы показали, что стрептотрицины F и D присоединяются к рибосомам прокариот намного более селективно, чем к эукариотическим (приблизительно в 40 раз). Токсичность по отношению к эукариотическим клеткам определили на макрофагах J774A.1 и клетках почек LLC-PK1. Для этого противомикробные препараты инкубировали с клетками в течение пяти дней. Оказалось, что CC50 была более, чем в десять раз выше у стрептотрицина F по сравнению с стрептотрицином D. Цитотоксическое действие стрептотрицина F также было отложено по сравнению с стрептотрицином D, что стало очевидным уже через два дня инкубации. Важно, что цитотоксическое действие стрептотрицина F отмечалось только при концентрации 32 μM, что значительно выше, чем MIC99 для CRE (4 μM).
Исследователи также определили максимальную переносимую дозу (maximum tolerated dose, MTD) для стрептотрицина F и норсеотрицина. Для этого препарат вводили мышам в нескольких концентрациях. Норсеотрицин использовали в качестве суррогата стрептотрицина D, так как последний сложно выделить в количествах, достаточных для эксперимента. При введении до 200 мг/кг стрептотрицина F или 20 мг/кг норсеотрицина не было выявлено никаких признаков дискомфорта у мышей в течение 72 часов. Две мыши в группе 400 мг/кг стрептотрицина F и одна мышь в группе 50 мг/кг норсеотрицина умерли или были усыплены. Признаки токсичности для почек выявляли уже при дозе 100 мг/кг стрептотрицина F и 10 мг/кг норсеотрицина. Таким образом, авторы остановились на дозах 50 мг/кг стрептотрицина F и 5 мг/кг норсеотрицина. Одно введение стрептотрицина F в дозировке 50 или 100 мг/кг было эффективно для лечения мышей, зараженных изолятом K. pneumoniae Nevada.
В опытах на резистентных мутантных штаммах авторы изучили механизм действия норсеотрицина. Они показали, что он отличается от механизма действия тетрациклина, так как мутации, ассоциированные с резистентностью к норсеотрицину, не придавали штаммам устойчивости к тетрациклину, доксициклину, миноциклину, тигециклину или эравациклину. Также TetM не был связан с устойчивостью к норсеотрицину. Криоэлектронная микроскопия позволила выявить сайты связывания стрептотрицинов D и F. Один сайт связывания был общим для этих двух соединений. Он находился на спирали 34 16S рРНК.
Таким образом, авторы показали, что стрептотрицин F эффективен против современных резистентных штаммов. Он обладает уникальным механизмом действия, отличным от других ингибиторов трансляции. Авторы считают, что поиск аналогов этих молекул с высоким терапевтическим потенциалом оправдан.
Бактерии двигаются к источнику антибиотика в самоубийственной атаке
Источник:
Christopher E. Morgan, et al. Streptothricin F is a bactericidal antibiotic effective against highly drug-resistant gram-negative bacteria that interacts with the 30S subunit of the 70S ribosome // PLOS Biology (2023), published May 16, 2023, DOI: 10.1371/journal.pbio.3002091


 Меню
Меню





 Все темы
Все темы




 0
0