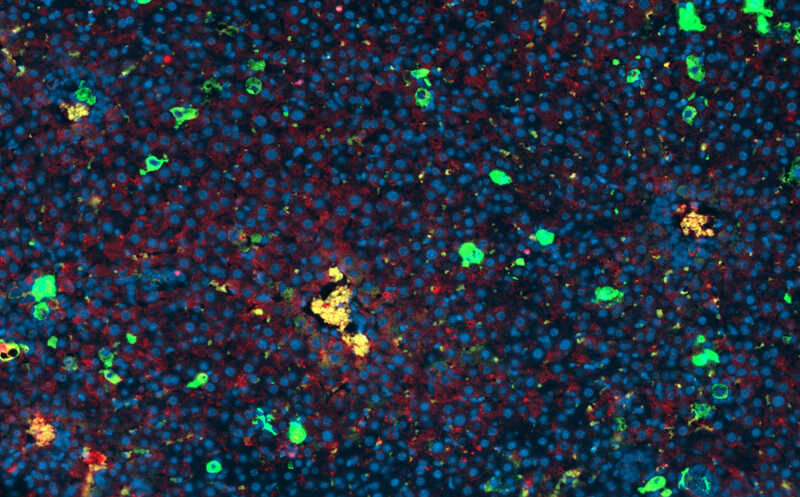
B-клеточная лимфома ускоряет старение иммунных клеток, особенно в молодом организме
Исследователи из США и Германии выяснили, как B-клеточная лимфома влияет на иммунные клетки. Оказалось, что и старение, и лимфома способствуют накоплению железа в Т-клетках. Это происходит из-за эпигенетических и транскрипционных изменений в сигнальных путях гема и железа и связано с приобретением клетками сенесцентного фенотипа. Однако в стареющем организме мыши и человека CD4+ T-клетки были более устойчивы к воздействию железа — их фенотип изменялся не так сильно, как у молодых клеток. Признаки ускоренного старения были выявлены и в других тканях мышей с лимфомой. После излечения некоторые изменения, связанные со старением, обращались вспять, но другие оставались неизменными.
Старение повышает риски развития рака и сильно влияет на работу и состав иммунной системы. Так, нарушается баланс провоспалительных цитокинов и хемокинов (инфламейджинг), гемопоэтические клетки начинают производить больше моноцитов и меньше лимфоидных клеток, поляризация макрофагов меняется на провоспалительную, снижается количество NK-клеток, CD8+ и CD4+ T-клеток и происходит смещение их фенотипа в сторону подавляющего иммунный ответ. T-клетки экспрессируют больше маркеров сенесценции, таких как KLRG1, ингибитор клеточного цикла p16INK4a/CDKN2A и некоторые провоспалительные цитокины.
Рак влияет на иммунитет, например, солидные опухоли подавляют CD8+ T-клетки, но поддерживают пролиферацию Treg. T-клетки также приобретают истощенный фенотип под действием постоянной стимуляции антигенами в микроокружении опухоли. Некоторые опухолевые клетки подавляют экспрессию MHC1, чтобы избежать распознавания Т-клетками и (или) экспрессируют PD-L1 и CD47, чтобы «отключить» функции Т-клеток и предотвратить фагоцитоз. Известно, что терапия рака ускоряет старение, особенно у молодых людей, но не так много известно про влияние самого рака на старение. Исследователи из США и Германии показали, как лимфома влияет на иммунную систему у молодых и старых людей и мышей.
B-клеточную лимфому (с незрелыми B-клетками) вызвали у мышей 6–12 недель и 78+ недель (примерно соответствует 16 и 56+ годам у человека). Через 12 недель анализировали иммунные клетки селезенки. Ранее было показано, что лимфома приводит к значительному снижению количества молодых Т-клеток. Однако количество старых CD4+ и CD8+ Т-клеток оставалось неизменным. То есть старение защищало иммунные клетки от вызванного лимфомой снижения их числа.
У молодых мышей с лимфомой фенотип CD4+ T-клеток изменялся значительно. В то же время количество клеток памяти CD62L/CD44 не менялось значительно среди T-клеток старых мышей с лимфомой. У старых CD4+ T-клеток не менялась экспрессия CD39, CD69, KLRG1 и PD-1 в отличие от молодых. Лимфома значительно не влияла а CD8+ T-клетки в любом возрасте. Схожие результаты были показаны для мышиной модели диффузной В-крупноклеточной лимфомы. Таким образом, стареющие CD4+ T-клетки по своей природе были устойчивы к фенотипическим изменениям, вызванным В-клеточной лимфомой, даже после перемещения в молодой организм.
Созревание молодых NK-клеток было нарушено у молодых мышей с лимфомой, у которых наблюдалось значительное увеличение незрелых популяций CD27−CD11b− и снижение более зрелых популяций CD27+CD11b+. Однако популяции старых NK-клеток CD27/CD11b не подверглись значительному влиянию лимфомы.
Авторы изолировали T- и NK-клетки у молодых мышей с лимфомой и секвенировали РНК единичных клеток. Все молодые T-клетки приобретали свойства стареющих клеток. Напротив, стареющие T-клетки значительно не меняли свой профиль экспрессии, как и NK-клетки мышей любого возраста. Молодые Т-клетки мышей с лимфомой демонстрировали повышенную транскрипционную активность сигнального пути IL-2-STAT5 по сравнению с молодыми контрольными Т-клетками. Многие гены этого пути перекрываются между старыми Т-клетками и молодыми Т-клетками из пораженного лимфомой организма.
Авторы отследили эпигенетические изменения CD4+ T-клеток, которые ассоциированы с различными ответами на болезнь. Молодые CD4+ Т-клетки мышей показали значительное увеличение экспрессии пути метаболизма гема, вызванное лимфомой. Лимфома также способствовала накоплению внутриклеточного железа в CD4+ и CD8+ Т-клетках независимо от возраста животных.
Примечательно, что наблюдалось повышение уровня внутриклеточного железа в Т-клетках у пожилых (≥65 лет) людей по сравнению с молодыми здоровыми донорами (≤37 лет). CD4+ Т-клетки у большинства пациентов с лимфомой содержали повышенные уровни внутриклеточного железа по сравнению с молодыми здоровыми контролями, но только у половины CD8+ Т-клеток этих пациентов возрастало количество железа.
Авторы предположили, что старение изменяет реакцию Т-клеток на железо. Обработка железом значительно снизила жизнеспособность активированных молодых CD4+ и CD8+ Т-клеток, но увеличила жизнеспособность активированных старых CD4+ и CD8+ Т-клеток. Старение способствовало повышению толерантности к железу как у мышей, так и у людей в Т-клетках.
Таким образом, старение и В-клеточная лимфома способствуют накоплению внутриклеточного железа в Т-клетках посредством эпигенетических и транскрипционных изменений в сигнальных путях гема и железа. Увеличение уровня железа в активированных молодых Т-клетках способствует снижению количества клеток, вызванному лимфомой; но в зависимости от возраста, увеличение уровня железа может способствовать и выживанию Т-клеток.
В-клеточная лимфома может вызывать увеличение экспрессии маркеров старения и в других тканях (аорта, почки, печень и толстый кишечник). После уничтожения клеток лимфомы число CD4+ и CD8+ T-клеток не повышалось. В них по-прежнему было много железа. Однако CD8+ T-клетки вырабатывали меньше TNFα, а CD4+ T-клетки — меньше IFNγ. Частично восстанавливалась популяция наивных T-клеток. То есть некоторые фенотипы, связанные со старением и вызванные лимфомой, фиксированы, другие — обратимыми. Некоторые воспалительные фенотипы в других тканях организма также могут быть обращены вспять.
Ускоренное старение органов предупреждает о развитии заболеваний в ближайшие десятилетия
Источник:
Rebecca S. Hesterberg, et al. Lymphoma accelerates T cell and tissue aging // Cancer Cell (2025), 21 August 2025, DOI: 10.1016/j.ccell.2025.07.023


 Меню
Меню





 Все темы
Все темы




 0
0