Белок с низкой экспрессией легче эволюционирует
Исследователи из Швейцарии изучили влияние уровня экспрессии белка на его способность эволюционировать на примере зеленого флуоресцентного белка. Они провели несколько циклов случайного мутагенеза и отбирали штаммы с голубым цветом флуоресценции. Выяснилось, что пониженная экспрессия помогает быстрее эволюционировать, так как не позволяет накапливаться мутациям с дестабилизирующим эффектом.
Credit:
123rf.com
Различные белки организма могут сильно отличаться по уровню экспрессии, причем чем сильнее белок экспрессируется, тем консервативнее его последовательность. В теории это можно объяснить тем, что белки с высоким уровнем экспрессии играют более важную роль, и их консервативность объясняется высоким давлением отбора. Однако в статье, опубликованной в Nature Ecology&Evolution, ученые из Швейцарии показали экспериментально и при помощи математического моделирования, что уровень экспрессии сам по себе является параметром, значительно влияющим на скорость эволюции белка.
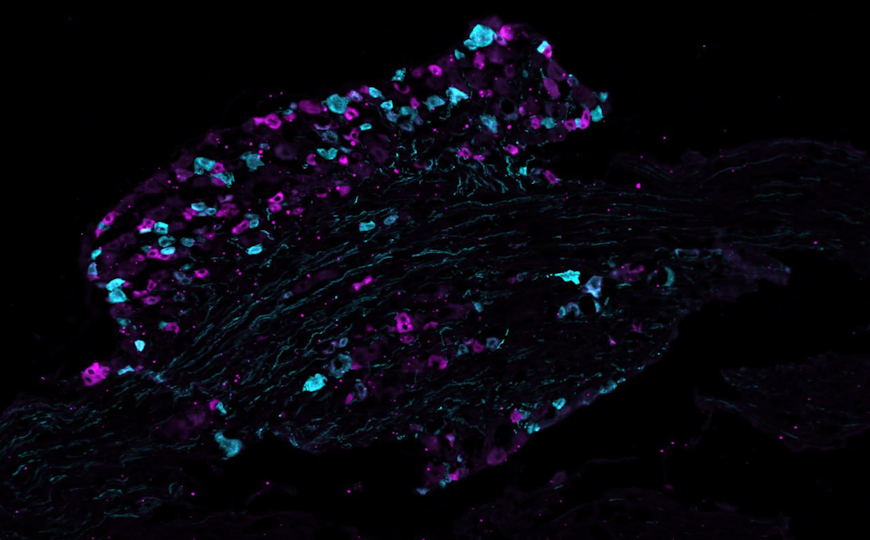
Авторы проводили направленный отбор библиотеки случайных мутантов зеленого флуоресцентного белка (GFP) на способность к эмиссии голубого (точнее, цианового) света. Библиотеку мутантов GFP экспрессировали в E. coli под двумя разными промоторами: сильным acp и слабым arg, и на проточном сортере отбирали 0,05% бактерий-победителей, экспрессирующих белки с голубой флуоресценцией. После сортинга последовательности мутантов GFP секвенировали при помощи одномолекулярного секвенирования в реальном времени (SMRT) на PacBio и повторяли мутагенез отобранных белков. Всего было проведено шесть раундов мутагенеза и отбора и по четыре реплики эксперимента для каждого из промоторов.
Выяснилось, что при низкой экспрессии белок эволюционировал значительно быстрее, чем при высокой. Однако в популяции слабо экспрессируемого белка обнаружилось меньше несинонимичных замен, а среди сильно экспрессируемых белков было больше неофункциональных мутаций, отвечающих за смену цвета флуоресценции. Значит, дело не в том, что слабо экспрессируемые белки быстрее накапливают неофункциональные мутации.
Чтобы объяснить этот феномен, ученые создали вычислительную модель, в которой приспособленность белка (то есть уровень его флуоресценции) зависит от трех факторов: квантового выхода, стабильности фолдинга (выраженной в изменении свободной энергии Гиббса, ΔG) и уровня экспрессии. Симуляция процесса показала, что отбор на фоне высокой экспрессии белка будет способствовать накоплению дестабилизирующих мутаций, так как потеря стабильности будет в какой-то мере компенсироваться высокой экспрессией. Это происходит из-за того, что разброс интенсивности флуоресценции больше именно при высокой экспрессии белка, и поэтому отобранные из этой популяции мутанты также будут сильнее отличаться по стабильности. А высокая интенсивность флуоресценции необязательно говорит о стабильности структуры белка.
Далее ученые проверили предсказание экспериментально, изменив дизайн эксперимента с мутагенезом: теперь раундам отбора на циановую флуоресценцию предшествовали три этапа отбора на стабильность. Отбор на стабильность был нестрогим и проводился лишь для того, чтобы отсеять 30% самых нестабильных вариантов. В результате такого эксперимента эффективность эволюции GFP никак не зависела от силы промотора, под которым он был экспрессирован.
Ученые пришли к выводу, что белки с низкой экспрессией подвергаются более сильному отбору на стабильность, что облегчает возможность быстрой эволюции. Это может быть распространенным механизмом, с помощью которого низкая экспрессия помогает белкам обретать новые свойства в меняющемся мире.
Источник
Karve S., et al. Low protein expression enhances phenotypic evolvability by intensifying selection on folding stability // Nat Ecol Evol (2022). 10.1038/s41559-022-01797-w


 Меню
Меню





 Все темы
Все темы




 0
0