Эндогенные ретровирусы человека ассоциированы с неврологическими заболеваниями
Немецкие ученые обобщили все, что сейчас известно об участии эндогенных ретровирусов в развитии рассеянного склероза, бокового амиотрофического склероза и шизофрении. Препарат против рассеянного склероза, нацеленный на белок эндогенного ретровируса, уже проходит клинические испытания.
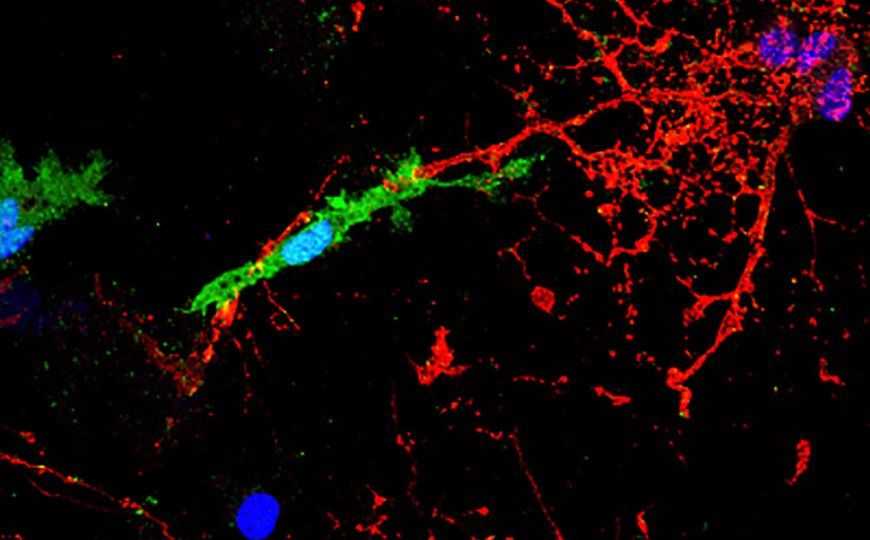
Клетка микроглии (зеленая) контактирует с миелинизированным аксоном (красный). В присутствии оболочечного белка pHERV-W это взаимодействие ведет к повреждению аксона. Синим показаны ядра клеток.
Credit: HHU / Joel Gruchot / Patrick Küry. Пресс-релиз
Около 8% нашего генома составляют эндогенные вирусы (human endogenous retroviruses, HERV) — ретровирусные элементы, встроившиеся в человеческий геном. Обычно HERV никак себя не проявляют, но под действием инфекции, гипоксии, некоторых лекарств, воспаления или мутаций может случиться их реактивация — начнется синтез вирусного белка или даже сборка вирусных частиц. Ранее было показано, что экспрессия HERV коррелирует с проявлением некоторых неврологических заболеваний: рассеянного склероза (РС), бокового амиотрофического склероза (БАС) и шизофрении.
При рассеянном склерозе поражается миелиновая оболочка нейронов в результате аутоиммунной реакции. Развитие этого заболевания ассоциировано с появлением в спинномозговой жидкости белка оболочки реактивированного вируса (ENV) и его РНК. Позже обнаружилось, что ENV способен вызывать иммунный ответ против миелина. По гистологическим данным, этот белок экспрессируется в основном миелоидными клетками.
Аутоиммунную реакцию белки HERV могут вызывать через «молекулярную мимикрию». «В дополнение к непосредственному воздействию HERV на миелинизирующие клетки, несколько групп сообщают о структурном сходстве между HERV и гликопротеином олигодендроцитов — молекулой, экспрессируемой на поверхности миелина, — говорит ведущий автор работы, профессор Патрик Кюри из Университета Генриха Гейне в Дюссельдорфе. — Это сходство может обмануть иммунную систему, так что она повредит миелин, усилив атаку на HERV».
При боковом амиотрофическом склерозе наблюдается прогрессирующая потеря моторных нейронов. Повышенный уровень ретровирусной обратной транскриптазы обнаруживается в крови и спинномозговой жидкости пациентов с БАС. С повышенной экспрессией вирусного фермента ассоциированы два локуса седьмой хромосомы— 7q34 и 7q36.1. Вирусные транскрипты экспрессируются в кортикальных и спинномозговых нейронах больных, в тканях же здоровых людей такого не наблюдалось. У трансгенных мышей, экспрессирующих белок оболочки вируса, развивалась моторная дисфункция. С другой стороны, некоторые исследования не подтвердили связь между повышенными уровнями вирусной РНК в коре и развитием БАС.
Шизофрения на патофизиологическом уровне характеризуется уменьшением объема мозга, потерей миелина и изменением функции астроцитов. Для шизофрении недавно было показано снижение метилирования районов некоторых HERV, что должно вести к росту их экспрессии. Однако экспрессия других HERV при шизофрении уменьшается.
Таким образом, HERV напрямую или через иммунную систему повреждают нейроны и глиальные клетки. Возможно, антитела, нейтрализующие вирусные белки, подобные ENV, и воздействие через эпигенетические механизмы позволят ослабить симптомы этих тяжелых заболеваний.
«Следует отметить, что была проведена фаза IIb клинического исследования с использованием нейтрализующего антитела против HERV — Темелимаба, в котором участвовали пациенты с рецидивирующим РС. Сейчас мы ждем, чтобы увидеть, окажет ли лечение благотворное влияние на ремиелинизацию, ослабит ли нейродегенерацию», — заключает Кюри. Темелимаб, разработанный швейцарской компанией GeNeuro, содержит антитела против оболочечного белка эндогенного ретровируса pHERV-W. Результаты фазы I испытаний препарата были многообещающими. Кстати, недавно вышло еще одно исследование, посвященное безопасности этого препарата.
Источники
Gruchot J., Kremer, D. and Küry P. // Neural Cell Responses Upon Exposure to Human Endogenous Retroviruses. // Frontiers in Genetics, 2019. DOI: 10.3389/fgene.2019.00655
D. Kremer, et al. // pHERV-W envelope protein fuels microglial cell-dependent damage of myelinated axons in multiple sclerosis. // PNAS, first published June 18, 2019; DOI: 10.1073/pnas.1901283116
Цитаты по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0