Фаги микобактерий с полностью синтетическими геномами оказались жизнеспособными
Исследователи из США разработали технологию конструирования микобактериофагов, включающую синтез фрагментов ДНК, сборку геномов и электропорацию в клетки Mycobacterium smegmatis. Таким способом они «перезапустили» два фага микобактерий — BPs и Bxb1. Метод позволяет быстро создавать мутантные и рекомбинантные варианты с расширенным спектром хозяев, встроенными генами-репортерами или удаленными элементами лизогении. Он открывает путь к созданию новых терапевтических фагов и инструментов для исследований в области генетики микобактерий, а также может сделать ненужным хранение бактериофагов в коллекциях.
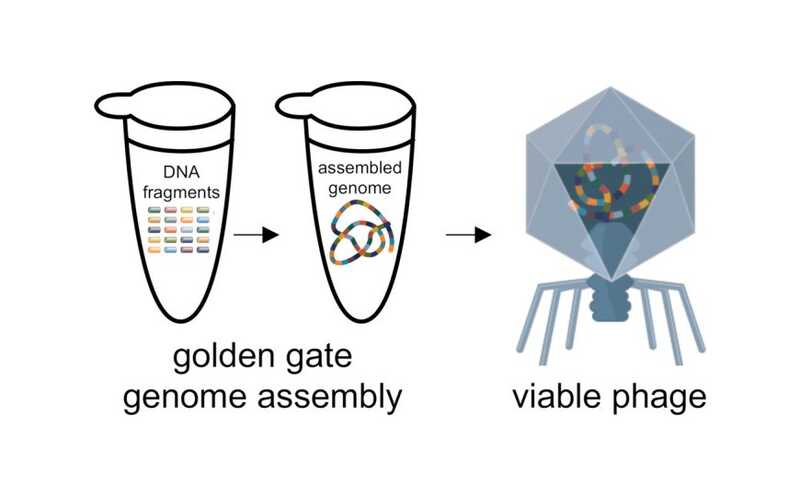
Получение синтетического бактериофага (здесь изображен упомянутый в тексте фаг Т4)
Credit:
ACS Synth Biol. 2022. DOI: 10.1021/acssynbio.1c00525 | CC BY-NC-ND 4.0
Исследователи из Питсбургского университета и компании Ansa Biotechnologies (США) собрали «с нуля» большие и GC-богатые геномы фагов микобактерий и получили жизнеспособные фаги.
В последние десятилетия бактериофаги вновь привлекают внимание как альтернатива антимикробным препаратам. Предполагается, что они могут найти применение при инфекциях, вызванных лекарственно-устойчивыми патогенами, включая нетуберкулезную микобактерию Mycobacterium abscessus и бактерии комплекса M. tuberculosis. Фаги обладают высокой специфичностью к хозяину и поэтому не нарушают микробиом пациента. Однако их использование ограничено несколькими ключевыми проблемами, такими как узкий спектр фагов, специфичных к клинически значимым штаммам, и недостаточно высокая эффективность. Кроме того, геномы микобактериофагов плохо охарактеризованы, функция многих генов не определена, что вызывает опасения при терапевтическом применении.
Создание фагов, не имеющих генов с неизвестными функциями, представляется очевидным решением. Для этого могут применяться челночные фазмиды либо электропорация геномной ДНК фага и фрагментов ДНК, содержащие желаемую модификацию, в рекомбинирующие бактериальные штаммы с последующим скринингом. Альтернативный подход — прямая сборка генома бактериофага из фрагментов ДНК. ТехнологияHigh-Complexity Golden Gate Assembly (HC-GGA) позволяет с помощью ферментов рестрикции и лигаз конструировать геном из малых фрагментов, которые можно получить синтетически или с помощью стандартной ПЦР. При этом не нужна промежуточная сборка в живых клетках. Например, геном фага Escherichia coli T7 размером 40 т. п. н. был собран таким способом из 52 фрагментов, и после трансформации этого генома в E. coli удалось получить жизнеспособный фаг.
Однако геномы микобактериофагов богаты GC-парами (до 70%), что осложняет синтез из фосфорамидитов, и велики по размеру (40–150 т.п.н.). Авторы статьи в PNAS предложили эффективную технологию синтетического создания и «перезапуска» таких фагов. Она включает ферментативный синтез ДНК, сборку Golden Gate и электропорацию в Mycobacterium smegmatis.
Авторы использовали альтернативный метод синтеза ДНК с помощью терминальной дезоксинуклеотидилтрансферазы (TdT) — с ее помощью можно получать участки ДНК длиной 2–5 т.п.н. даже при высоком содержании GC-пар. Для сборки целых геномов использовалась модифицированная HC-GGA, где десятки фрагментов соединяются в одном реакционном объеме. В качестве моделей были выбраны два микобактериофага: BPs (41,9 т.п.н., 66,6% GC) и Bxb1 (50,5 т.п.н., 63,6% GC).
Геном BPs собирали из 12 фрагментов. Из их последовательностей с помощью синонимичных замен были удалены сайты, распознаваемые рестриктазой BsaI, за исключением концевых (эта рестриктаза используется при сборке методом HC-GGA для получения липких концов, и присутствие ее сайта внутри фрагмента привело бы к его разрезанию). Также авторы удалили сайты рестрикции PaqCI, хотя эта рестриктаза не вовлечена в сборку, «чтобы обеспечить дополнительную гибкость в будущем применении синтетической системы». Модифицированные последовательности авторы называют «одомашненными».
Синтезированные фрагменты клонировали в E. coli, затем плазмиды, содержащие 12 фрагментов, смешивали и проводили сборку методом HC-GGA. Получившуюся кольцевую ДНК вводили с помощью электропорации в клетки M. smegmatis и высеяли их на твердую среду. На чашке Петри появились сотни бляшек — свидетельство успешной «перезагрузки» синтетического фага. Полученный штамм phCCK1 оказался полностью идентичен исходному BPs и демонстрировал сходную эффективность репликации, на которую не повлияли синонимические замены.
Используя тот же модульный подход, авторы создали серию производных фагов с целевыми изменениями: удаляли гены интегразы и репрессора для получения облигатно литических вариантов, не способных к лизогении; вводили точечные мутации, расширяющие спектр хозяев; добавляли репортерные или антирестрикционные гены из других фагов и M. abscessus. Все эти варианты успешно собирались и вызывали образование бляшек на газоне M. smegmatis. Однако некоторые конструкции, например, с геном 80 фага Cuco и геном 91 фага Expelliarmus (оба они сходны с геном антирестрикционного белка ArdA плазмиды ColIb-P9) оказались токсичными для фага, и формирования бляшек не происходило, возможно, из-за чрезмерной экспрессии продуктов.
Чтобы проверить применимость метода к более крупным и сложным геномам, исследователи синтезировали и собрали фаг Bxb1. Его геном (50,5 т.п.н.) также разделили на 12 фрагментов, из которых удалили 41 сайт BsmBI и 9 сайтов PaqCI. После первичной неудачи (вызванной заменой аминокислоты в перекрывающихся генах 50 и 51) исправленная версия успешно перезапустилась в M. smegmatis, формируя нормальные бляшки. Этот случай продемонстрировал, что изменение кодонов в областях с неизвестными функциями следует с осторожностьюб.
Далее было создано несколько производных Bxb1. Мутант phCCK18 без гена gp30 (участвующего в формировании хвостовой структуры) формировал жизнеспособные частицы, но без характерных «гало» вокруг бляшек — что позволило идентифицировать gp30 как фермент D-Ala-D-Ala-карбоксипептидазу, который разрушает покоящиеся клетки. Другой вариант, phCCK20, лишенный гена репрессора, оказался полностью литическим и эффективно уничтожал M. smegmatis. Третий, phCCK16, без интегразы, показал возникновение компенсаторных мутаций в репрессоре, что указывает на тесную связь между этими генами в контроле лизогении. По информации авторов, Bxb1 — самый большой фаг созданный с помощью данного подхода.
Таким образом, комбинация TdT-синтеза, сборки HC-GGA и прямой электропорационной «перезагрузки» в M. smegmatis дает возможность получать фаги с синтетическим геномом, несмотря на высокое содержание GC-пар. Метод работает быстро (в одной реакции соединяются десятки фрагментов) и позволяет проектировать терапевтически полезные варианты фагов с заданными свойствами — от расширенного спектра хозяев до встроенных генов-репортеров. Эта стратегия открывает путь к библиотекам синтетических микобактериофагов для фаготерапии, диагностики и молекулярных инструментов исследований в области микобактериологии.
Предложенный подход «значительно улучшат наше понимание микобактериофагов, включая функции их генов, структуру, жизненные циклы, экспрессию генов и регуляцию», — пишут авторы. Они признают существенное ограничение — высокую стоимость синтеза генома фага в настоящее время (~$10 000 для генома размером 50 т.п.н.). Но она будет снижаться, так что, возможно, необходимость хранения жизнеспособных фагов в коллекциях через какое-то время исчезнет — нужный фаг будут просто синтезировать заново.
Источник
Ko C., et. al. Genome synthesis, assembly, and rebooting of therapeutically useful high G+C% mycobacteriophages // PNAS (2025), published online 10 November 2025. DOI: 10.1073/pnas.2523871122


 Меню
Меню





 Все темы
Все темы




 0
0