Грибок Candida albicans колонизирует кишечник здоровых мышей с помощью токсина кандидализина и адгезинов
Candida albicans может длительное время находиться в кишечнике млекопитающих, но он же становится причиной серьезных системных инфекций. Кандидозы в основном изучают на мышах, получающих антибиотики, находящихся в стерильных условиях, а также без иммунитета. Ученые из США, Великобритании и Германии показали, что клинический штамм C. albicans колонизирует кишечник здоровых мышей в обычных условиях и даже на фоне противогрибковой терапии. Устойчивое заселение кишечника требовало экспрессии грибковых факторов вирулентности — токсина кандидализина (ECE1) и адгезинов Als3 и Hwp1.
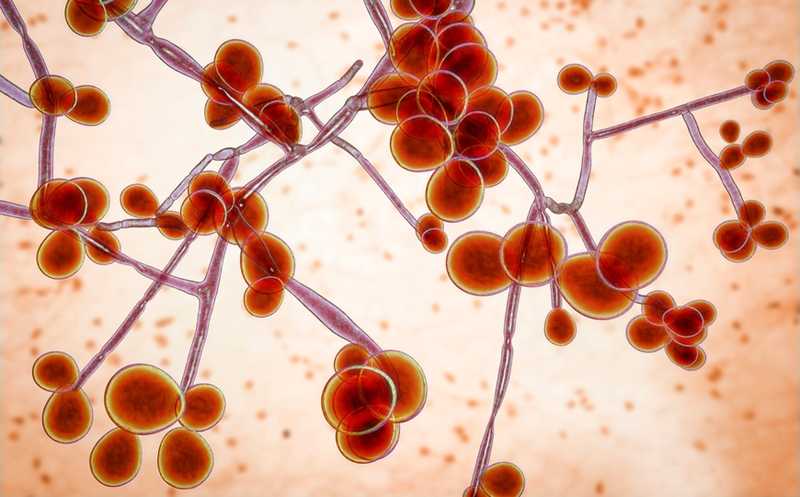
Candida albicans — широко распространенный грибок, заселяющий слизистые оболочки желудочно-кишечного тракта (ЖКТ), мочеполовой системы, а также дыхательные пути и кожу человека. Колонизация C. albicans может протекать без симптомов, но этот грибок способен становиться причиной местных инфекций и серьезных инвазивных заболеваний. Его присутствие связывают с хроническими заболеваниями кишечника, дыхательных путей, печени и мозга. При этом причиной системной инфекции обычно являются штаммы, заселяющие ЖКТ. Более 80% здоровых людей имеют C. albicans в составе микробиома кишечника. Чтобы выяснить, как C. albicans инициирует системные инфекции и способствует развитию хронических заболеваний, важно понять, как этот грибок заселяет кишечник и задерживается в нем на долгое время.
Большая часть данных о колонизации ЖКТ была получена на мышиных моделях, получавших антибиотики или живущих в стерильных условиях, а также на животных с подавленным иммунитетом, что искажает картину естественного поведения грибка. Ученые из США, Великобритании и Германии провели исследование, чтобы понять, как C. albicans колонизирует ЖКТ здоровых мышей с нормальной микробиотой в естественных условиях, и какие грибковые факторы необходимы для этой колонизации.
В качестве инокулята ученые использовали клинический изолят CLCA10, выделенный из дыхательной системы пациента с астмой. После однократного введения CLCA10 в ЖКТ мышей C. albicans стабильно сохранялся в организме в течение по крайней мере 58 дней без признаков болезни или изменения веса у животных. Грибок локализовался преимущественно в просвете кишечника. Колонизация не нарушала бактериальный микробиом и была устойчивой — численность грибка снижалась под действием амфотерицина B, но он не исчезал полностью.
Интересно, что штамм C. albicans SC5314, ранее считавшийся неспособным к долгосрочной колонизации, также устойчиво заселял кишечник мышей. Факторы среды (тип диеты, температура и способ культивирования до введения) почти не влияли на колонизацию. Мыши одной линии разного пола или от разных поставщиков одинаково реагировали на колонизацию, но некоторые генетические линии мышей (BALB/c, 129S1) показывали меньшую восприимчивость.
В контрольных экспериментах другие виды грибков, включая Candida auris, C. tropicalis, Nakaseomyces glabratus и даже безопасные для человека дрожжи Saccharomyces cerevisiae, не смогли колонизировать ЖКТ более чем на 14 дней. Это подчеркивает уникальную способность C. albicans к долговременной асимптоматической колонизации кишечника.
Исследователи удаляли гены C. albicans, связанные с вирулентностью: ECE1 (кодирует токсин кандидализин), als3 и hwp1 (адгезины). Оказалось, что штаммы без ECE1 полностью теряли способность к колонизации, особенно в присутствии нормальной микробиоты (способность восстанавливалась при добавлении антибиотиков). Удаление ALS3 и HWP1 частично подавляло колонизацию, особенно на слизистой. Другие мутации (например, в SAP2, CAT1, ICL1) не влияли на результат. Эти данные подтверждают, что для успешного удержания на слизистой кишечника C. albicans необходимы как адгезивные свойства, так и локальная активность кандидализина.
Таким образом, авторы показали, что C. albicans способен устойчиво колонизировать ЖКТ мышей в естественных условиях, и что эта колонизация зависит от экспрессии определенных факторов вирулентности, в первую очередь кандидализина и адгезинов. Грибок не вызывает воспаления и не нарушает микробиоту, но при этом устойчив к системной терапии. Эти данные позволяют лучше понять, как грибок переходит от комменсального состояния к патогенному, и какие мишени можно использовать для разработки средств для его контроля.
Новое противогрибковое средство выделили из патогена картофеля
Источник:
Mauk K.E., et. al. Commensal colonization of Candida albicans in the mouse gastrointestinal tract is mediated via expression of candidalysin and adhesins. // Microbiology Spectrum (2025), published online 30 July 2025. DOI: 10.1128/spectrum.00567-25


 Меню
Меню





 Все темы
Все темы




 0
0











