Иммунные клетки наследуют искусственно созданное гиперметилирование и становятся «агрессивней»
Миелоидные патологии часто ассоциированы с нарушениями в метилировании ДНК. Эпигенетическое редактирование промотора p15 в гемопоэтических стволовых клетках (ГСК) показало, что гиперметилирование не только наследуется иммунными клетками, которые образуются из таких ГСК, но и изменяет их транскриптомный профиль в сторону провоспалительной активности.
Credit:
123rf.com
Гиперметилирование ДНК промоторных последовательностей — одна из черт старения клеток человека. Оно наблюдается, в частности, в гемопоэтических стволовых клетках (ГСК), где также ассоциировано с заболеваниями крови, например, острой миелоидной лейкемией. Недавнее исследование показало, что редактирование этой эпигенетической метки в ГСК при помощи системы CRISPR не только наследуется при дифференцировке, но и эффективно регулирует дальнейший гемопоэз, меняя характеристики популяций лимфоцитов.
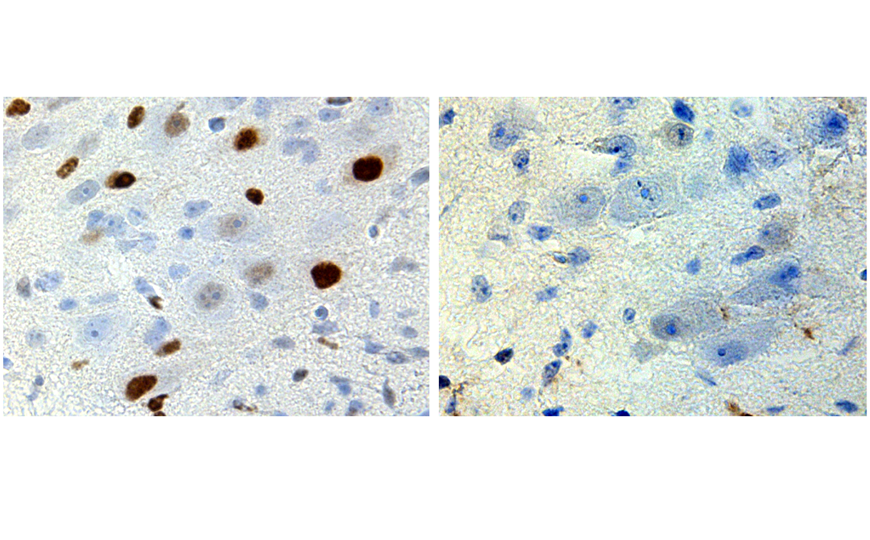
Сперва ученые установили, что один из ключевых эпигенетических регуляторов гемопоэза — это метилирование промотора CDKN2B, также известного как p15. Для этого они использовали dCas9, слитую с ДНК-метилтрансферазой (DNMT). Такой гибридный белок не обладает каталитической активностью Cas9, однако его можно нацелить на нужный участок с помощью гидовых РНК, куда DNMT навесит метильную метку. Исследователи попробовали отредактировать человеческие CD34+ ГСК с помощью нескольких вариантов гидовых РНК: нацеленных на промоторы p14 (ARF), p15 (CDKN2B) и p16 (CDKN2A), однако в последнем случае изменить уровень метилирования им не удалось. Дальнейшие опыты на CD34+ ГСК показали, что гиперметилирование промотора p15 существенно снижает уровень его экспрессии, однако на колониеобразующей активности это не сказывается. Интересно, что сам паттерн гиперметилирования наследовался при дифференцировке ГСК в миелоидные клетки.
Помимо экспериментов in vitro ученые также проанализировали паттерны метилирования в клетках периферической крови пациентов, у которых был выявлен клональный гемопоэз с неопределенным потенциалом (CHIP). По-видимому, гиперметилирование промотора p15 может иметь клиническое значение — авторы обнаружили его у некоторых пациентов с CHIP. В частности, большая вариабельность метилирования отмечалась у пациентов с предлейкозом.
Влияние гиперметилирования p15 на гемопоэз исследователи проверили in vivo. Они вводили отредактированные человеческие ГСК иммунодефицитным мышам, а 19 недель спустя анализировали результат. Человеческие ГСК с гиперметилированием промотора p15 успешно приживались у модельных животных, причем пропорции миелоидных (CD33+), лимфоидных (CD19+) и прогениторных (CD34+) клеток в костном мозге практически не отличались от контроля. Различия встречались в популяции миелоидных клеток: при гиперметилировании p15 моноцитов (CD14+) было существенно меньше, а гранулоцитов (CD66b+) больше, чем у контрольных мышей. Среди прогениторных клеток ученые также выявили изменения — в их популяции снизилось количество мультипотентных и лимфоидных предшественников, а доля предшественников гранулоцитов и моноцитов, наоборот, возросла.
Авторы работы отдельно обращают внимание на наследуемость искусственно созданного гиперметилирования. С помощью бисульфитного секвенирования они показали, что паттерн метилирования сохраняется во всех линиях, дифференцировавшихся из отредактированных ГСК, спустя 19 недель после пересадки. Уровень гиперметилирования в некоторых CpG-островках промотора p15 достигал 76%, а его характер согласовался с полученными in vitro данными.
Дальнейший транскриптомный анализ показал, что гиперметилирование p15 влияет также на активность унаследовавших его иммунных клеток. Ученые отсеквенировали РНК моноцитов и гранулоцитов, полученных от модельных мышей. В обоих типах клеток они выявили нарушение регуляции транскриптов, связанных с эффекторной функцией клеток.
Так, в моноцитах активней экспрессировались гены HLA, связанные с презентацией антигенов, и провоспалительные цитокины (IL1B и TNF). Анализ дифференциальной экспрессии в гранулоцитах выявил прежде всего факторы, участвующие в распознавании патогенов и интерфероновом ответе I типа (JUN, NFAT5). Это указывает на то, что клетки врожденного иммунитета, унаследовавшие метилирование p15 от ГСК in vivo, могут способствовать развитию патологических воспалительных процессов.
«Результаты нашего исследования демонстрируют возможность отредактировать метилирование ДНК в гемопоэтических стволовых клетках человека при помощи CRISPR/dCas9, а также указывают на то, что такое de novo метилирования поддерживается в процессе кроветворения in vitro и in vivo» — заключают ученые. Предложенный ими подход поможет углубить понимание того, какую роль в развитии заболеваний играет такой эпигенетический механизм, как метилирование ДНК.
Цитата по пресс-релизу
Источник
Saunderson, E.A. et al. CRISPR/dCas9 DNA methylation editing is heritable during human hematopoiesis and shapes immune progeny. // PNAS (2023). DOI: 10.1073/pnas.230022412


 Меню
Меню





 Все темы
Все темы




 0
0