Химерные молекулы стабилизируют белок CFTR в модели муковисцидоза
При муковисцидозе происходит деградация мутантного белка CFTR. Новые молекулы DUBTAC привлекают к белку деубиквитиназу, стабилизируя его и предотвращая деградацию, что должно улучшить состояние больного. Эксперименты проводились на клеточной модели.
Многие из известных на сегодняшний день заболеваний, в том числе онкологических, метаболических и нейродегенертивных, вызваны аберрантным убиквитинированием и протеосомной деградацией белков. В таких случаях разрушающиеся белки считаются недоступными для терапии (undruggable).
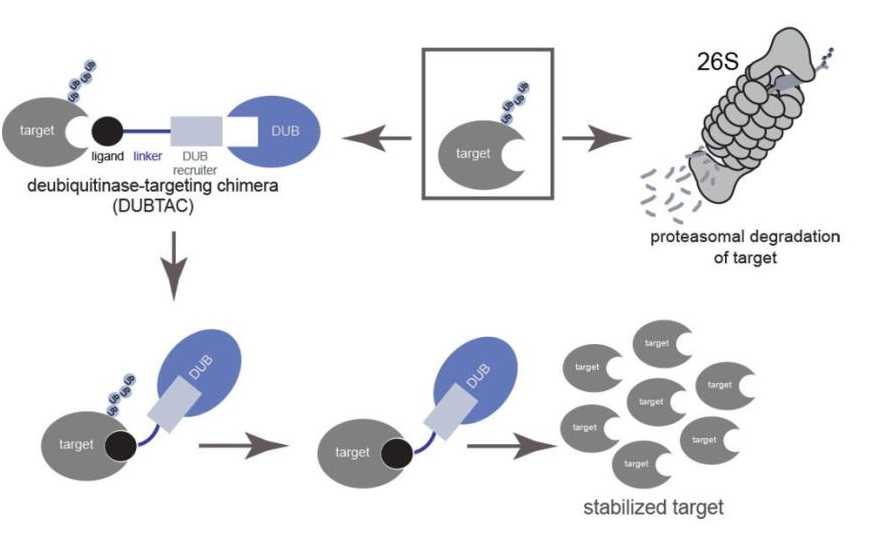
Авторы нового исследования предложили способ избежать аберрантной деградации, основанный на стабилизации белка. Они разработали химерные молекулы, привлекающие деубиквитиназу к белку-мишени, деградация которого происходит убиквитин-зависимым образом. Платформа получила название DUBTAC (deubiquitinase-targeting chimeras).
DUBTAC представляют собой молекулы в форме гантели, которые содержат рекрутер фермента деубиквитиназы с одной стороны и лиганд к белку с другой, соединенные линкером. Рекрутер DUB — это малая молекула, подобранная таким образом, чтобы не нарушать функцию фермента. Деубиквитиназа удаляет убиквитиновую метку с белка-мишени, предотвращая его разрушение.
DUBTAC проверили на модели муковисцидоза — клетках эпителия бронхов, экспрессирующих мутантную форму хлоридного канала CFTR. Мутация приводит к конформационной нестабильности белка. Препарат лумакафтор, который используется для терапии муковисцидоза, работает как шаперон для мутантного CFTR, корректируя его фолдинг. Однако даже при использовании лумакафтора белок активно убиквитинируется и деградирует.
Ученые сконструировали DUBTAC, несущий рекрутер деубиквитиназы OTUB1 на одном конце и лумакафтор на другом. Они показали, что молекула надежно стабилизирует белок CFTR. В результате проводимость хлоридных каналов в клетках улучшается.
Также ученые разработали DUBTAC для стабилизации супрессора опухолей — киназы WEE1. Киназа фосфорилирует комплекс циклин-зависимой киназы CDK1 с циклином B1, ингибируя таким образом прогрессию клеточного цикла. DUBTAC, нацеленная на WEE1, стабилизировала уровень белка в клетках гепатомы, но терапевтическая эффективность молекулы пока неясна.
Работа служит доказательством концепции стабилизации белков с помощью DUBTAC. Авторы надеются, что платформа станет основой для разработки нового класса препаратов против множества заболеваний.
Источник
Henning, N.J. et al. Deubiquitinase-targeting chimeras for targeted protein stabilization // Nature Chemical Biology (2022). DOI: 10.1038/s41589-022-00971-2


 Меню
Меню





 Все темы
Все темы




 0
0











