Хламидии обманывают иммунную защиту клетки с помощью белка GarD
Исследователи из Университета Дьюка выяснили, что позволяет возбудителю хламидиоза — широко распространенной передаваемой половым путем инфекции, избегать иммунного ответа хозяина. Бактерия Chlamydia trachomatis — облигатный внутриклеточный паразит — живет и размножается под защитой мембранного пузырька, который образуется при проникновении хламидии в клетку. Ученые провели генетический скрининг и идентифицировали на поверхности этого пузырька белковый фактор (GarD), который маскирует хламидий от иммунной системы хозяина.
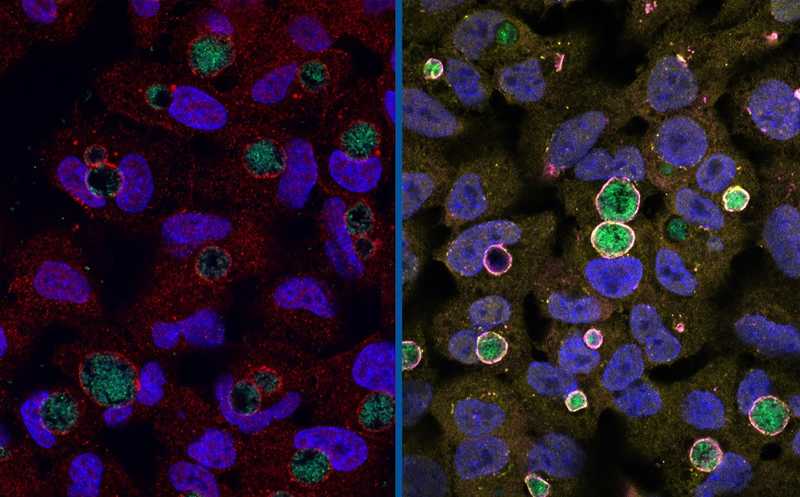
Слева: Chlamydia trachomatis дикого типа (зеленый цвет), окруженные белком GarD (красный), который скрывает бактерии от иммунного ответа клеток человека.
Справа: хламидии с нокаутом garD (зеленый), которые окружены антимикробными белками — убиквитином (желтый) и RNF213 (пурпурный).
Credit:
Stephen C. Walsh, Duke University
Хламидиоз — одна из самых распространенных инфекций, передающихся половым путем. Только в США ежегодно регистрируют порядка 200 тысяч человек, причем у многих из них заболевание протекает без клинических проявлений. Особенно опасен хламидиоз для женщин: без лечения он может привести к хроническому воспалению органов малого таза, внематочной беременности и даже бесплодию.
Возбудитель инфекции — бактерия Chlamydia trachomatis — облигатный внутриклеточный паразит. Проникать в клетку и скрываться от автономного внутриклеточного иммунитета (autonomous intracellular immunity) хламидиям помогает вакуоль из клеточной мембраны, называемая патологическим включением. Такая маскировка позволяет патогену успешно размножаться, а вызванная им инфекция может бессимптомно длиться месяцами.
Однако было неясно, почему включения с хламидиями не вызывают иммунный ответ клетки, индуцированный интерфероном гамма (IFNγ, lymphocyte-derived cytokine gamma-interferon).
Авторы новой публикации в Cell Host & Microbe пролили свет на механизмы этого явления. С помощью генетического скрининга они выделили белковый фактор, защищающий бактерию от распознавания клеткой, убиквитинилирования и уничтожения. Им оказался мембранный белок GarD (от англ. Gamma resistance Determinant), называемый также мистерином. Ученые показали, что праймированные IFNγ клетки человека, имеющие на поверхности линейные формы адаптерных белков убиквитина (OPTN, NDP52, TAX1BP1), опознают хламидии, несущие мутации гена garD, которые нарушают функции фермента (мистерина), и те быстро устраняются клеткой.
Полногеномное секвенирование геномов отдельных клеток с анализом ассоциаций установило, что активной в отношении белков хламидии является конкретная молекула — E3-лигаза, а именно белок RNF213. Этот крупный фермент участвует в одном из путей уничтожения клеткой патологических белков. Авторы исследования сравнивают RNF213 с «глазами» иммунитета, которые хламидия «научилась ослеплять». Активируемая в присутствии IFNγ молекула RNF213 способна убиквитинилировать и тем самым запустить деградацию мембранных включений с бактериями, не имеющих GarD.
Выходит, что GarD играет роль своеобразного стелс-фактора (фактора «невидимости»), позволяющего хламидиям маскироваться от иммунного ответа и успешно размножаться. В то же время RNF213 является молекулой-антагонистом GarD.
Авторы отмечают, что многие детали механизма патогенности Chlamydia им все еще не известны. «Внутри клетки присутствует такое многообразие различных мембран и вакуолей» — отмечает Йорн Коерс, один из авторов — «Как же иммунная система оказывается способна отличить редкую вакуоль с патогеном внутри? В случае Chlamydia это пока непонятно. Но что бы это ни было, мы убеждены, что мистерин его видит».
Авторы работы также провели эксперименты с близким родственником C. trachomatis — патогеном грызунов C. muridarum. Зараженные им человеческие клетки легко распознавали и удаляли не имеющий GarD патоген. Это указывает на узкую специализацию и избирательность двух видов хламидий, некогда произошедших от единого предка.
Источник
Walsh S.C., et al. The bacterial effector GarD shields Chlamydia trachomatis inclusions from RNF213-mediated ubiquitylation and destruction // Cell Host Microbe. Published: September 08, 2022. DOI: 10.1016/j.chom.2022.08.008


 Меню
Меню





 Все темы
Все темы




 0
0










