Конъюгат пептида и пептидонуклеиновой кислоты избирательно убивает связанную с раком бактерию
Международная команда исследователей, разрабатывающая антимикробные средства против Fusobacterium nucleatum — бактерии, связанной с ростом опухолей и химиорезистентностью, — сделала неожиданное открытие. Авторы создавали конъюгаты пептида и пептидонуклеиновой кислоты, которые могли бы проникать в клетку и подавлять экспрессию важных бактериальных генов через антисмысловое воздействие. Однако вместо исследуемых соединений эффективным оказался только контроль (FUS79), который избирательно уничтожал F. nucleatum. По-видимому, эффект FUS79 связан со стрессом бактериальной оболочки.
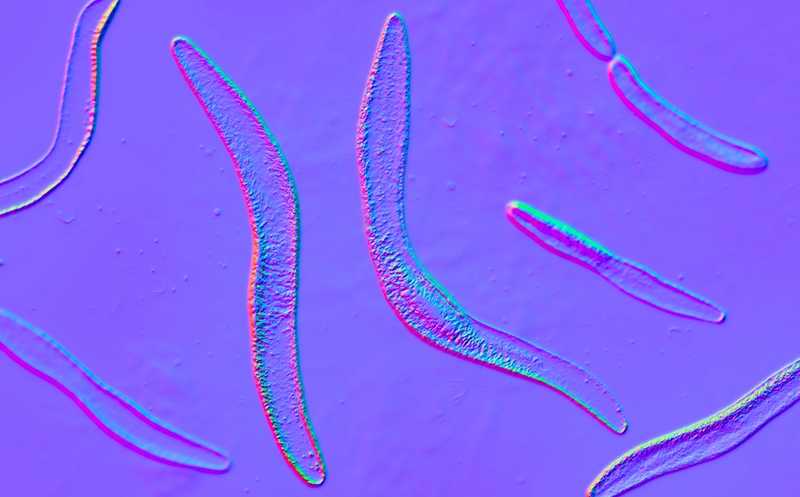
Fusobacterium nucleatum — комменсальная бактерия полости рта, чью способность колонизировать опухолевые ткани связывают с прогрессированием рака, метастазированием и химиорезистентностью. Ее накопление в опухоли коррелирует с ухудшением прогноза. Хотя антибиотики широкого спектра действия могут снижать бактериальную нагрузку и замедлять развитие опухоли, их применение сопряжено с побочными эффектами — от расстройств ЖКТ и дисбиоза до воспалительных реакций и риска рецидива, что ограничивает их клиническое применение.
Авторы статьи в mBio разработали видоспецифичные программируемые антибиотики нового поколения. Ключевой компонент этих средств — антисмысловые олигомеры на основе пептидонуклеиновых кислот (ПНК). ПНК — синтетические аналоги нуклеиновых кислот с устойчивой пептидоподобной структурой, которая обеспечивает прочность и стабильность в биологических средах. Благодаря азотистым основаниям они способны связываться с комплементарной мРНК, блокируя синтез жизненно важных белков бактерии. Для эффективной доставки в клетку ПНК конъюгируют с клеточно-проникающими пептидами (КПП).
Ученые протестировали несколько КПП и выбрали (RXR)4XB за его высокую способность проникать в клетки F. nucleatum. Далее были созданы ПНК с этим пептидом, направленные на области начала трансляции предполагаемых жизненно важных генов бактерии (acpP, ftsZ, gyrA, dnaB, rpoA, rpoB, rpoD, clpB, groEL, fomA). Для проверки специфичности эффекта разработали и контрольные соединения с ПНК, не комплементарными ключевым регионам мРНК.
Ожидалось, что таргетные конъюгаты замедлят рост бактерии, однако ни один из них не продемонстрировал выраженного антимикробного действия. Некоторые соединения лишь незначительно задерживали рост, причем эффект был сопоставим с контрольными препаратами. То есть экзогенно доставленные антисмысловые олигомеры не проявляют ожидаемой активности против F. nucleatum. Это может быть связано с недостаточной эффективностью доставки в цитоплазму, ограниченными знаниями о жизненно важных генах или проблемами с дизайном самой ПНК.
Неожиданный результат дал один из контрольных конъюгатов — (RXR)4XB с ПНК последовательности GACATAATTGT, получивший название FUS79. Несмотря на отсутствие комплементарности к ключевым генам, он полностью подавил рост бактерии. Дальнейший анализ подтвердил, что FUS79 обладает бактерицидным действием, а не просто подавляет рост. Причем эффект оказался избирательным: препарат эффективно уничтожал различные штаммы F. nucleatum, включая клинические изоляты (FNN23, FNN25, FNA, FNP, FPE), но не действовал на подвид F. nucleatum subsp. vincentii (FNV), несмотря на его близкое родство с чувствительным штаммом FNN23. Это подчеркивает специфичность FUS79 даже внутри одного вида. Другие грамотрицательные бактерии, такие как P. gingivalis и E. coli, остались нечувствительны, тогда как у Salmonella enterica отмечался дефект роста — эффект, характерный для конъюгатов этого типа, но не связанный с целенаправленным действием FUS79.
Ученые выяснили, что бактерицидный эффект FUS79 не связан с антисмысловой активностью, а определяется сочетанием пептида (RXR)4XB и нуклеотидной последовательности ПНК. Без пептида или с другим пептидом (KFF)3K препарат не проявлял активности. Интересно, что замена ПНК на фосфородиамидатный морфолиновый олигомер с той же последовательностью при конъюгации с (RXR)4XB сохраняла эффект, что подтверждает важность структуры пептида и последовательности, а не механизма антисмыслового действия. Активность FUS79 зависела от плотности культуры и состава среды, что характерно для мембранных агентов.
Анализ транскриптома (РНК-секвенирование) чувствительного штамма FNN23 и устойчивого FNV после обработки FUS79 показал ключевые различия в активации функциональных путей. В FNN23 препарат индуцировал пути, связанные с рибосомами, метаболизмом аминокислот, бактериальными секреторными системами, синтезом пептидогликана и деградацией РНК. Также наблюдалась активация генов, ассоциированных с реакцией на стресс клеточной оболочки, включая значительное повышение активности генов σE-регулона. Этот регулон критически важен для поддержания целостности клеточной оболочки в ответ на стресс. В штамме FNV такие реакции не наблюдались, что указывает на отсутствие выраженной стрессовой активации. Авторы предполагают, что FUS79 взаимодействует с бактериальной оболочкой, вызывая стресс и клеточную гибель.
Открытие FUS79 имеет большое значение. Хотя изначальная цель создания антисмыслового антибиотика не была достигнута, это соединение представляет новый мощный инструмент для избирательного воздействия на F. nucleatum. Такой подход может стать альтернативой или дополнением к традиционным антибиотикам для целевого удаления этой бактерии у пациентов с онкологическими заболеваниями.
Механизм действия FUS79, основанный на индукции мембранного стресса, отличается от предполагаемого антисмыслового эффекта, что открывает новые возможности для разработки антимикробных средств против F. nucleatum. Для полноценного использования потенциала FUS79 необходимы дальнейшие исследования, чтобы точно определить молекулярный механизм действия и возможные пути оптимизации.
Микробиом ротовой полости влияет на когнитивные функции
Источник:
Cosi V., et al. An antisense oligomer conjugate with unpredicted bactericidal activity against Fusobacterium nucleatum. // mBio0, e00524-25, published online 29 April 2025. DOI: 10.1128/mbio.00524-25


 Меню
Меню





 Все темы
Все темы




 0
0











