Кожный трансплантат светится в ответ на воспаление
Японские ученые получили «живой сенсорный дисплей» — искусственную кожу с модифицированными стволовыми клетками кератиноцитов для мониторинга биомаркеров. Клетки были изменены так, что в ответ на фактор некроза опухоли альфа (TNF-α) запускалась экспрессия флуоресцентного белка. Искусственную кожу пересадили мышам и после приживления вызывали у них воспаление. Флуоресценцию регистрировали уже через несколько часов. Подобные дисплеи можно использовать для долговременного мониторинга заболеваний.
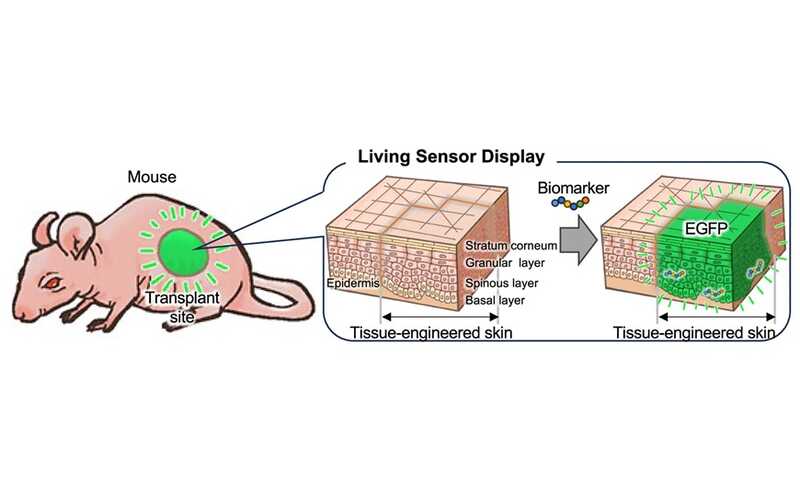
Исследователи из Японии предложили новый метод долговременного измерения уровня глюкозы, воспалительных цитокинов или других биомаркеров — модифицированные стволовые клетки кератиноцитов кожи (KSC).
Кожа выполняет барьерную функцию, но также является сенсором многих биомаркеров in vivo. KSC находятся в базальном слое эпидермиса и поддерживают его структуру. Благодаря их позиции и особенностям дифференцировки, изменения в KSC и их дочерних клетках легко детектируются. Исследователи модифицировали живые клетки таким образом, чтобы те вырабатывали флуоресцентные белки в ответ на внешние сигналы. Кожу с такими клетками трансплантировали для длительного мониторинга биомаркера. Такой сенсор назвали «живым сенсорным дисплеем». В качестве биомаркера выбрали фактор некроза опухоли альфа (TNF-α). Кератиноциты эпидермиса (NHEK) и KSC экспрессировали NF-κB-EGFP под действием TNF-α. Систему опробовали на мышах.
Сигнальный путь NF-κB вовлечен во многие биологические процессы, включая иммунитет, воспаление, ответ на стресс. Несколько лигандов, включая TNF-α, связывают рецепторы, в результате белковый комплекс NF-κB активируется и распознает специфические нуклеотидные последовательности (RE, responsible element), запуская транскрипцию генов. Для создания живого сенсорного дисплея авторы получили KSC, в которых трансген слит с RE и EGFP.
Работу системы проверили in vitro. Под действием TNF-α появлялся флуоресцентный сигнал уже через 12 часов, а через 24 часа он еще усиливался. IL-1β также вызывал появление флуоресценции, так как он вовлечен в сигнальный путь TNF-α, а IL-1 или LPS — нет.
Исследователи культивировали модифицированные NHEK и нормальные человеческие дермальные фибробласты для моделирования кожи. При добавлении TNF-α была видна флуоресценция. Интенсивность зависела от концентрации. Пик был достигнут примерно через 17 часов.
Искусственную кожу пересадили мышам. Низкий уровень флуоресценции был отмечен сразу после пересадки, что можно объяснить иммунным ответом на трансплантацию. Действительно, воспалительные клетки проникали в трансплантат, но через несколько недель их количество снизилось, после чего провели дальнейшие испытания. Пересаженная кожа реагировала на TNF-α флуоресценцией. Пик приходился на 1–2 день. Флуоресценцию можно вызвать повторно после затухания.
Мышам с пересаженным участком кожи давали вызывающие воспаление вещества, такие как LPS, которые сами не индуцируют флуоресценцию. Действительно, была отмечена флуоресценция, хотя и через больший промежуток времени. В месте трансплантата и в нормальных частях ткани наблюдались многочисленные нейтрофилы и зрелые макрофаги.
Таким образом, живой сенсорный дисплей использует характеристики рецепторов для обнаружения нестабильных биомаркеров in vivo с высокой чувствительностью. После анализа безопасности сконструированные клетки могут быть имплантированы в организм для выявления и долгосрочного мониторинга заболеваний.
Создан сверхчувствительный биосенсор для ранней диагностики рака молочной железы
Источник:
Jun Sawayama, et al. Living sensor display implanted on skin for long-term biomarker monitoring // Nature Communications (2026), 12 January 2026, DOI: 10.1038/s41467-025-67384-2


 Меню
Меню





 Все темы
Все темы




 0
0











