Круговые пермутанты Cas9 — новый инструмент модификации генома
Исследователи из Калифорнии, известные своими работами в области CRISPR и конструирования белков, объединились для создания нового поколения нуклеаз Cas9 — круговых пермутантов, обладающих принципиально новыми свойствами. Активность этих конструктов можно регулировать внешними факторами, а возможности их использования для создания новых регуляторов активности генома могут оказаться очень широкими.
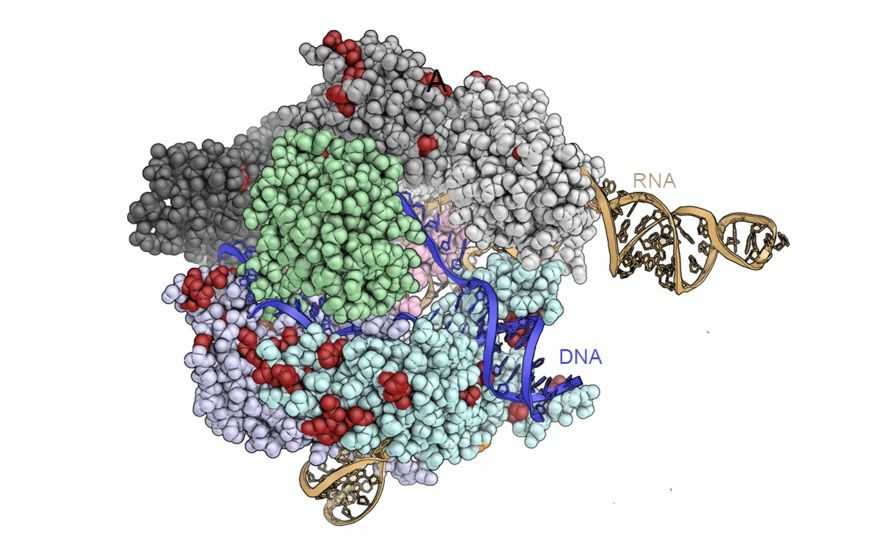
Нуклеаза Cas9 — один из главных генераторов новостей в молекулярной биологии, постоянно появляются новые технологии на ее основе. Однако и недостатков у них пока хватает, и возможности далеко не исчерпаны. Что если попытаться поменять местами части Cas9? – задались вопросом исследователи из Калифорнийского университета в Беркли и Институтов Гладстона в Сан-Франциско.
На страницах средневековых книг часто можно видеть животных с переставленными частями тела. Конечно, такие животные не могут существовать в реальности, иллюстраторы развлекались или создавали символы, но почему бы не представить, что змея с головой посредине туловища имеет некоторые преимущества по сравнению с обычной гадюкой? По такой логике работает круговая пермутация белков — создается молекула, у которого «голова» присоединена к «хвосту», а «туловище» разделено на две части; итоговый белок состоит из тех же доменов, что исходный, но они переставлены «по кругу». С белком это проделать проще, чем с животным, но и тут есть свои сложности: вручную, разрезая и склеивая ДНК белка нуклеазами и лигазами, качественную библиотеку пермутантов создать практически невозможно. Выход нашли не тик давно, приспособив для конструирования пермутантов транспозоны. Похожая технология, с годами претерпевшая ряд модификаций, была использована и для конструирования библиотеки пермутантов Cas9.
По свидетельству экспериментаторов, они не ожидали такого уровня устойчивости Cas9 к пермутациям. Было выявлено 77 точек, пермутация в которых не инактивировала нуклеазу. Эти точки объединялись в три группы, по расположению в том или ином домене белка: RuvC, Helical-II, и С-концевом (CTD). Поскольку активный фермент невозможно скринировать в E. coli, анализу подвергалась мутантная нуклеаза, неспособная расщеплять ДНК. Это, впрочем, не мешало ей супрессировать продукцию красного флуоресцентного белка. Супрессия и стала индикатором успешной пермутации. Зеленый флуоресцентный белок выступал в роли свидетеля: его экспрессия говорила об отсутствии других вариантов инактивации сигнала от красного белка.
Зачем нужна пермутированная нуклеаза? Прежде всего, такой фермент можно гораздо жестче контролировать, например, давать ему дополнительный сигнал активации. В процессе исследования выяснилось, что если длина линкера, который связывает пермутированные фрагменты нуклеазы, менее 15 аминокислот, активность фермента блокируется. (В исходном Cas9, при правильной трехмерной укладке N- и C-концы находятся на расстоянии 40–60 ангстрем друг от друга, эта «змея», хотя и свернулась клубком, свой хвост в зубах не держит.) Вот такой заблокированный фермент можно включать, расщепляя линкер специфической протеазой. Пермутант Cas9 вначале сконструировали под активацию протеазой TEV, а затем, добившись результата, создали пермутанты, активируемые вирусными протеазами. «Альтруистическая защита», как обозначили полученную систему авторы, блокировала распространение вирусной инфекции: если в эукариотическую клетку, содержавшую ген «протеолитического» пермутанта, попадал вирус, то его протеаза активировала заблокированную Cas9, нацеленную на жизненно важный ген. Клетка погибала, блокируя распространение вируса. В отсутствие вирусной протеазы пермутант Cas9 был на 100% неактивен.
Для чего может понадобиться такая система? Для человека — вряд ли (хотя, учитывая ВИЧ и его способность бессимптомно жить в геноме некоторых клеток иммунной системы, и в медицине система на сходной основе может найти применение). А вот для защиты растений от вирусных инфекций — вполне вероятно. Авторы также предполагают, что база найденных пермутантов и инактивированной Cas9 расширит возможности для конструирования регуляторных белков – активаторов транскрипции, сайтспецифических инструментов для репарации ДНК, и многого другого. От пермутантов недалеко и до сплит-белков, а это еще одно большое окно возможностей для Cas9, которая постепенно превращающется в «универсального солдата» молекулярной биологии и медицины.
Источник
Oakes et al.. //CRISPR-Cas9 Circular Permutants as Programmable Scaffolds for Genome Modification//, Cell, 176, 254–267 (2019); DOI: 10.1016/j.cell.2018.11.052


 Меню
Меню





 Все темы
Все темы




 0
0











