Малые молекулы помогают доставить антисмысловые олигонуклеотиды через гематоэнцефалический барьер
Гематоэнцефалический барьер (ГЭБ) препятствует проникновению в мозг из крови не только патогенов и токсинов, но и лекарств. Ученые из США получили конъюгаты малых молекул с антисмысловыми олигонуклеотидами (АСО), которые могут проникать через ГЭБ и доставлять АСО во все основные типы клеток мозга. Успешную доставку АСО для терапии рака и бокового амиотрофического склероза продемонстрировали на мышах и на изолированной ткани мозга человека.
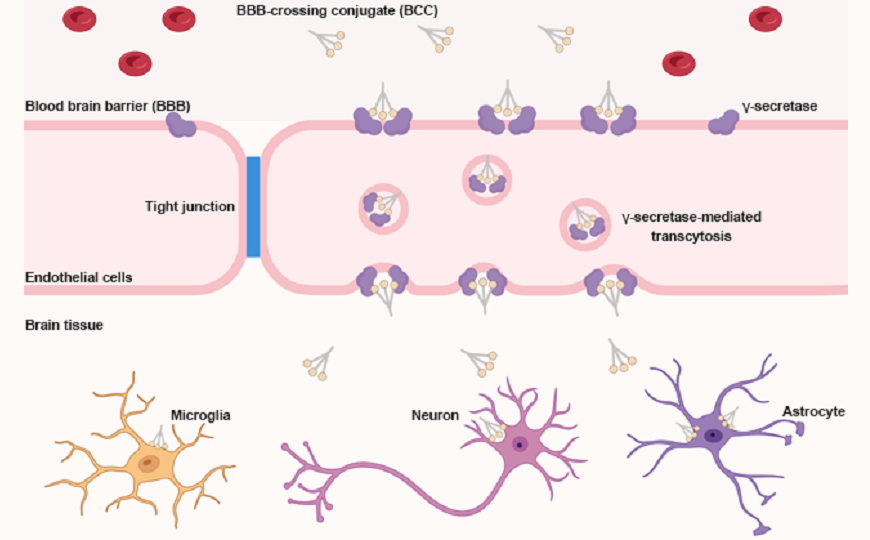
Гематоэнцефалический барьер (ГЭБ) защищает центральную нервную систему (ЦНС) от циркулирующих в крови патогенов и токсичных веществ. В то же время ГЭБ препятствует попаданию в мозг лекарств, особенно терапевтических биомакромолкул, что затрудняет лечение болезней ЦНС. Ученые из США разработали конъюгаты антисмысловых олигонуклеотидов с малыми молекулами, которые могут пересекать ГЭБ, и продемонстрировали эффективность их доставки в мозг.
В качестве основы для конъюгатов авторы изначально рассматривали несколько малых молекул: производные коричной кислоты, триптамина, MK-0752 и SR-57227. Коричная кислота способна пересекать ГЭБ, триптамин проникает в мозг с помощью ионов магния и АТФ, MK-0752 является ингибитором γ-секретазы, а SR-57227 проникает в мозг за счет связывания с 5-HT3 серотониновыми рецепторами. Для первых тестов ученые присоединили две или три копии малых молекул к флуорофору Cy5 через алкановый или этиленгликолевый спейсер.
Полученную панель конъюгатов малых молекул с Cy5 ввели внутривенно мышам. По сравнению со свободным флуорофором все конъюгаты лучше попадали в мозг. Так, уровни конъюгатов с тремя копиями производных коричной кислоты, триптамина и SR-57227 в мозге были в 62,5, 97 и 141,8 раз выше, чем уровень свободного Cy5. Но наилучший результат показал конъюгат с тремя копиями MK-0752: его в мозге было в 220,5 раз больше, чем свободного флуорофора. Этот конъюгат обозначили BCC10 и использовали в последующих экспериментах.
Новое исследование впервые показало, что γ-секретаза может опосредовать трансцитоз веществ через ГЭБ. Обычно этот фермент рассматривается только в контексте процессинга APP — белка-предшественника амилоида. Чтобы подробнее изучить процесс трансцитоза, ученые использовали модель ГЭБ: на вкладышах выращивали эндотелиальные клетки, а в лунках планшета под ними — астроциты и нейроны. Свободный Cy5 практически не проникал через такой барьер к нейронам, в то время как конъюгат BCC10-Cy5 справлялся с этой задачей. Если клетки эндотелия предварительно обрабатывали нирогацестатом или MK-0752 — ингибиторами γ-секретазы, то трансцитоз через ГЭБ ухудшался. Так ученые подтвердили роль γ-секретазы в пересечении ГЭБ конъюгатами.
Далее исследователи получили конъюгаты с биомолекулами — олигонуклеотидами. Сначала они проверили только возможность доставки олигонуклеотидов через ГЭБ, сравнивая свободные олигонуклеотиды, а также конъюгаты с BCC10 и холестерином. При внутривенном введении препаратов мышам конъюгат BCC10-олигонуклеотид накапливался в мозге в 66 и 7,3 раз интенсивнее, чем свободный олигонуклеотид и его конъюгат с холестерином. Помимо мозга, конъюгат BCC10-олигонуклеотид также накапливался в печени, почках и легких. В мозге же он попадал во все основные типы клеток. Так, при дозировке 25 мг/кг конъюгат удавалось доставить в 26,1% клеток микроглии, 23,9% нейронов, 19,8% эндотелиальных клеток, а также в 43,9% астроцитов.
Чтобы показать перспективность такого подхода к доставке биомолекул, ученые получили несколько конъюгатов с терапевтическими антисмысловыми олигонуклеотидами (АСО). Сначала исследователи конъюгировали с BCC10 АСО против мРНК Malat1, которые ассоциированы с метастазирующей аденокарциномой легких. Если мышам внутривенно вводили только АСО, то нокдауна Malat1 не наблюдалось. При введении конъюгата экспрессия этой мРНК снижалась в диапазоне от 26% до 62,6% в зависимости от дозировки. При дозе 25 мг/кг экспрессия Malat1 снизилась на 45,3% в нейронах, на 62,1% в астроцитах и на 56,5% в микроглиальных клетках.
Полученные результаты ученые также подтвердили на изолированной ткани мозга человека. В этом случае при инкубации ткани мозга с BCC10-ASOMalat1 экспрессия Malat1 снижалась на 81,3%.
Помимо этого, ученые показали возможность доставки АСО для лечения бокового амиотрофического склероза (БАС). Применялись АСО, способные подавлять экспрессию мРНК мутантного гена SOD1. В эксперименте ученые использовали трансгенных мышей, несущих мутацию G93A в этом гене. После внутривенного введения мышам BCC10-ASOSod1 исследователи добились снижения экспрессии мРНК Sod1 на 44,2%.
Авторы также продемонстрировали безопасность предлагаемых конъюгатов. Их введение не нарушало работу печени и почек, не повреждало органы и не приводило к воспалению. После инъекции конъюгатов практически не изменялся цитокиновый профиль крови. Исследователи заключили, что конъюгаты, способные пересекать ГЭБ, имеют терапевтический потенциал.
Ультразвук делает более эффективной доставку ингибиторов контрольных точек и доксорубицина в мозг
Источник:
Wang C. et al. Intravenous administration of blood–brain barrier-crossing conjugates facilitate biomacromolecule transport into central nervous system. // Nature Biotechnology (2024). DOI: 10.1038/s41587-024-02487-7


 Меню
Меню





 Все темы
Все темы




 0
0










