Микрофлюидный чип ускорил и упростил сборку наночастиц для доставки противораковых препаратов
Наночастицы — перспективный метод доставки противоопухолевых препаратов, однако их получение требует существенных затрат времени и реагентов. Ученые из Массачусетского технологического института разработали высокопроизводительный метод для масштабируемого синтеза многослойных наночастиц — они применили микрофлюидику. В отличие от классических способов, такая технология не требует дополнительных стадий очистки, поэтому снижает потери материала и ускоряет производство. Для демонстрации возможностей метода авторы собрали липосомы, несущие IL-12, а затем подтвердили их противоопухолевую эффективность на клетках и на мышах.
Наночастицы, загруженные противоопухолевыми препаратами, перспективны для лечения многих видов рака, включая рак яичников. Их можно специфично нацелить на опухоль, в тканях которой они будут накапливаться и высвобождать лекарство — это позволяет существенно снизить системные побочные эффекты по сравнению с традиционной химиотерапией.
Один из наиболее универсальных способов получения наночастиц — метод послойной сборки (Layer-by-Layer, LbL), позволяющий точно контролировать высвобождение лекарства, его фармакокинетические параметры и адресную доставку. Однако классические LbL-подходы требуют поэтапной очистки после каждого цикла покрытия, масштабировать их затруднительно, а производительность обычно невелика.
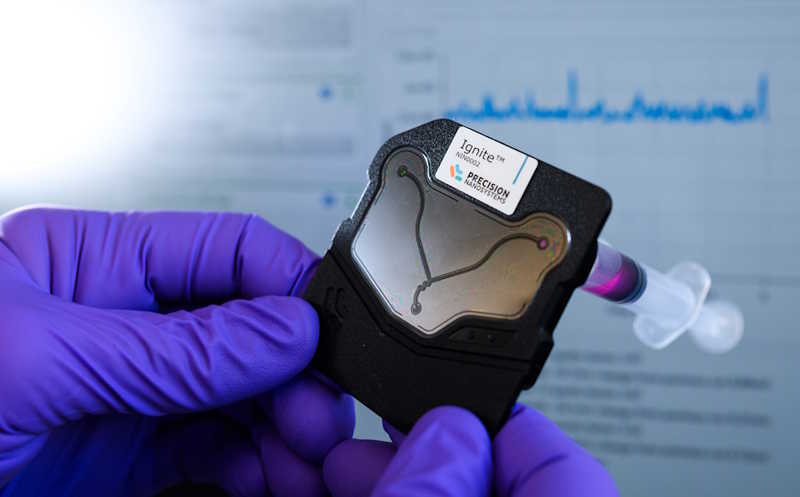
Ученые из США разработали метод получения многослойных наночастиц (LbL-NP) при помощи микрофлюидной технологии. Он позволяет собирать наночастицы без использования большого объема полимеров и стадий очистки, что упрощает и ускоряет процесс производства. За последнее десятилетие коллектив исследователей создал варианты LbL-наночастиц для доставки терапевтических молекул, которые доказали свою эффективность в доклинических исследованиях. Их изготовление оставалось ресурсоемким: после нанесения каждого слоя требовалось центрифугирование для удаления остаточного полимера, что ограничивало скорость и масштаб производства. Позднее для упрощения очистки ученые дополнили метод тангенциальной проточной фильтрацией (TFF), однако и она не обеспечивала необходимую производственную эффективность. Для преодоления этих ограничений исследователи предложили использовать микрофлюидную технологию, которая позволяет формировать LbL-NP в непрерывном потоке без промежуточных стадий очистки.
В предлагаемом подходе наночастицы последовательно проходят через микроканалы устройства, где к ним добавляются точно отмеренные объемы полимеров в растворе. Такая система исключает избыток реагентов, минимизирует потери материала и обеспечивает однородность покрытия. Она позволила получить около 15 мг наночастиц (что эквивалентно примерно 50 дозам) всего за несколько минут, тогда как ранее на это уходил почти час.
Для проверки подхода авторы синтезировали наночастицы, состоящие из анионных липосом, конъюгированных с интерлейкином-12 (IL-12), поли-L-аргинина (PLR) для создания положительного заряда и поли-L-глутамата (PLE) для того, чтобы усилить связывание наночастиц с клетками рака яичников и позволить им удержаться на клеточной мембране. Они выбрали IL-12 как цитокин, обладающий выраженным противоопухолевым действием.
Физико-химические параметры наночастиц оценивали с помощью динамического светорассеяния и измерения дзета-потенциала. Выяснилось, что для предотвращения агрегации необходимо использовать избыточное количество полимера по отношению к изоэлектрической точке — состоянию, при котором суммарный заряд частиц равен нулю. Это не приводило к дополнительной адсорбции полимера на поверхности частиц, но обеспечивало коллоидную стабильность. Сборка LbL-наночастиц при оптимальном соотношении компонентов позволила избежать агрегации и устранить этапы очистки. Полученные наночастицы отличались высокой однородностью и стабильностью.
Липосомальные наночастицы с IL-12, собранные новым методом, не уступали по свойствам аналогам, полученным традиционными способами. Они связывались с клетками рака яичников, оставались на их поверхности и сохраняли активность как в клеточных культурах, так и в мышиной модели метастатического рака (животным подсаживали клетки линии HM-1). Примечательно, что IL-12-NP не проникали в клетки, а оставались на их мембране, обеспечивая локальную активацию иммунного ответа. Лечение значительно увеличило выживаемость, часть мышей из экспериментальной группы дожила до окончания эксперимента, в отличие от остальных случаев.
Кроме того, микрофлюидная платформа позволяла собирать LbL-структуры из различных полимеров, включая гиалуроновую, поли-L-аспарагиновую и полиакриловую кислоты, а также наночастицы с разной природой ядра и размером — от липосом до латексных микросфер. Авторы отметили, что более мелкие частицы обеспечивают лучшее связывание с опухолевыми клетками, что, вероятно, связано с увеличенной площадью поверхности.
Технология позволяет работать с различными средами в качестве растворителей — собирать частицы можно не только в деионизированной воде, но и в физиологических буферах, что расширяет возможности управления толщиной и свойствами полимерных слоев. Более того, микрофлюидный картридж с бифуркационным смесителем, примененный в этой разработке, уже используется в производстве других нанопрепаратов, включая мРНК-вакцины, и соответствует стандартам GMP.
Предложенный микрофлюидный метод открывает путь к промышленному производству многослойных наночастиц для доставки лекарств. Он обеспечивает высокую воспроизводимость, сокращает производственные затраты и соответствует требованиям GMP. Благодаря своей универсальности подход может применяться для создания библиотек LbL-NP с заданными свойствами, что делает его перспективным как для фундаментальных исследований, так и для клинического применения.
Липидные наночастицы на основе тиофена доставляют мРНК в легкие и сетчатку
Источник
Pires, I. S. et al. High-Throughput Microfluidic-Mediated Assembly of Layer-By-Layer Nanoparticles. // Adv. Funct. Mater. 2503965 (2025). DOI: 10.1002/adfm.202503965


 Меню
Меню





 Все темы
Все темы




 0
0