Микрогель улучшает свертываемость крови у младенцев
У самых маленьких детей высока опасность кровопотери при хирургических вмешательствах или патологиях из-за незрелости системы гемостаза и рыхлой структуры тромба. Переливание продуктов крови от взрослых доноров, напротив, может вызвать тромбозы. Исследователи из США создали гемостатический микрогель для внутривенного введения, который улучшает структуру фибринового сгустка в крови младенцев. Эксперименты на мышах с неонатальным человеческим фибриногеном подтвердили, что микрогель снижает острую кровопотерю на 50–60%.
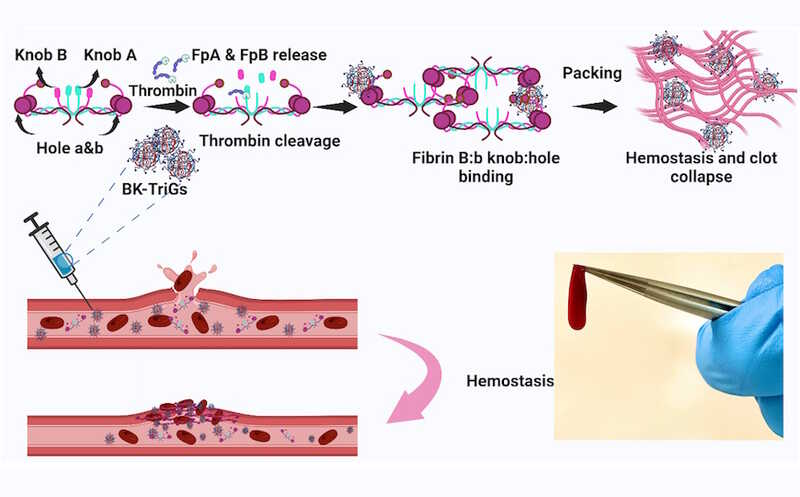
Принцип работы микрогелевых частиц BK-TriG: они улучшают структуру тромба, взаимодействуя с участком b фибриногена
Credit:
Science Advances. 2026. DOI: 10.1126/sciadv.ady7698 | CC BY-NC
У новорожденных могут возникнуть серьезные кровотечения в жизненно важных органах во время операций либо при различных патологиях, например в ЖКТ при некротизирующем колите или в головном мозге. Поэтому необходимы препараты, улучшающие свертываемость крови именно у этой группы пациентов. Исследователи из Университета Северной Каролины (США) разработали кровоостанавливающий препарат для младенцев — микрогель для внутривенного введения.
При повреждении кровеносного сосуда остановку кровотечения запускает многоступенчатый процесс, называемый гемостазом. Он включает сосудисто-тромбоцитарный механизм (спазм сосуда и закупорку агрегатами тромбоцитов — образование так называемого белого тромба) и коагуляционный — собственно свертывание крови. Коагуляционный гемостаз регулируется многочисленными факторами свертывания, и в результате образуется фибриновый сгусток, или красный тромб — сеть из волокон белка фибрина, в которой находятся эритроциты.
У младенцев гемостаз отличается от «взрослого»: фибриновые сгустки мягче, состоят из менее разветвленных молекул и быстрее деградируют. Чтобы компенсировать кровопотерю, детям переливают препараты крови, полученные от взрослых доноров, но разница в работе механизмов гемостаза может стать причиной тромбоза.
В настоящее время разрабатываются разные методы лечения неонатальных кровотечений, в том числе создание искусственных микрочастиц, имитирующих тромбоциты и несущих функциональные белки. Ранее авторы новой статьи в Science Advances выявили возрастные различия в динамике образования фибринового сгустка на молекулярном уровне, которые можно использовать в разработке препаратов..
От N-концевых участков цепей Аα и Вβ фибриногена тромбин отщепляет фибринопептиды А и В — на молекуле образуются участки А и В, которые взаимодействуют с участками а и b на соседних молекулах фибрина (фибриногена). А и В называются «выступами» (knobs), а и b — «отверстиями». У взрослых фибринопептид А отщепляется быстрее, чем фибринопептид В, и быстро образуются протофибриллы со связями А:а. Роль связей B:b в полимеризации фибрина нуждается в дальнейшем исследовании, однако считается, что они способствуют агрегации параллельных протофибрилл и образованию волокон из них.
Авторы ранее установили, что фибриноген новорожденных медленнее высвобождает фибринопептид А и быстрее — фибринопептид В. Но при этом миметики А мало влияют на структуру сгустка в детской крови, в отличие от миметиков В. Исследователи предположили, что эту структуру у новорожденных улучшат тромбоцитоподобные микрочастицы с пришитыми к ним фибринопептидами В — «выступами», взаимодействующими с «отверстиями» b. Такое связывание вызывает благоприятные конформационные изменения фибриногена и может способствовать латеральной агрегации фибрилл. Частицы назвали BK-TriG (B-knob triggered microgel). Поглощая воду, они превращаются в мягкие гидрогели, имитирующие механические свойства тромбоцитов, и тем самым дополнительно укрепляют сгусток.
Сначала исследователи протестировали BK-TriG in vitro с использованием микроКТ и конфокальной микроскопии для анализа структуры сгустков. BK-TriG достигали наилучшего результата в крови младенцев, тогда как в крови взрослых людей были эффективнее частицы, конъюгированные с фибринопептидом А. Кроме того, BK-TriG повышали стабильность фибринового сгустка, замедляя его деградацию, в том числе в потоке крови — на микрофлюидной платформе.
Для проверки действия препарата in vivo исследователи получили генномодифицированных мышей, в организме которых не вырабатывался фибриноген. Этим мышам вводили «младенческий» фибриноген пуповинной крови, так что характеристики их гемостаза были аналогичны тем, что наблюдаются у новорожденных детей. Кровопотерю моделировали повреждением печени. BK-TriG при внутривенном введении превзошли все другие протестированные варианты, снизив кровопотерю у мышей в течение 10 минут на 50–60% по сравнению с контрольной группой. Однако при введении самых высоких доз кровопотери вновь увеличились, возможно, потому, что микрочастицы начали конкурировать с участками фибрина за сайты связывания или создавать стерические препятствия
Авторы планируют сравнить BK-TriG с другими гемостатическими препаратами, представленными на рынке, как при их самостоятельном применении, так и в сочетании с BK-TriG. Необходимо проверить их безопасность, отмечает один из руководителей работы Эшли Браун. Так или иначе препарат представляется перспективным, в том числе потому, что производство частиц BK-TriG будет относительно недорогим по сравнению с препаратами крови.
Моноклональное антитело уменьшает риск кровотечений у пациентов с мерцательной аритмией
Источник
Nooshin Zandi, et al. Hemostatic B-knob–triggered microgels (BK-TriGs) to address bleeding in neonates // Science Advances. 3 Apr 2026. Vol 12, Issue 14. DOI: 10.1126/sciadv.ady7698
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0










