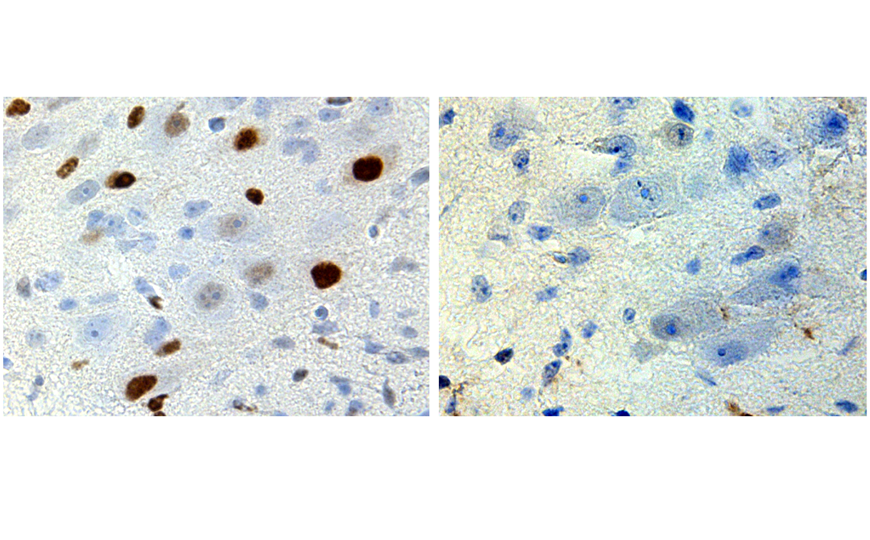
МикроРНК подавляют экспрессию терапевтической мРНК в клетках сердца
Исследователи из США работали над соматическим перепрограммированием клеток сердца для создания биологического кардиостимулятора. Они доставляли в кардиомиоциты химически модифицированную мРНК человеческого эмбрионального фактора транскрипции TBX18. Оказалось, что клетки сопротивлялись такому воздействию с помощью супрессорных микроРНК. Ученые разработали контрстратегии, которые привели к устойчивой экспрессии необходимого белка, используя антагонисты микроРНК.
За установку частоты, с которой бьется сердце человека, отвечает основной водитель ритма, который находится в синоатриальном узле (sinoatrial node, SAN). Специализированные клетки SAN экспрессируют гиперполяризационно-активируемые каналы HCN4, которые обеспечивают ток водителя ритма. Неспособность SAN генерировать электрические импульсы или нарушения системы проводимости, препятствующие их нормальному распространению, приводят к замедлению сердечного ритма, или брадикардии. За последние шесть десятилетий основой терапевтического вмешательства при таких заболеваниях стали электрические кардиостимуляторы. Однако существуют проблемы, ассоциированные с их использованием, такие как ограниченный срок службы батареи, инфекции, связанные с устройством, или возможность системного сбоя, что требует разработки альтернативных стратегий. Одним из таких подходов стала разработка биологического кардиостимулятора — создание области автоматизма, которая может функционировать как суррогат SAN. Для этого применяют соматическое перепрограммирование с помощью переноса генов, кодирующих факторы транскрипции, которые создают реплики настоящих клеток-водителей ритма.
Для доставки трансгенов in vitro и in vivo часто используют вирусные векторы. Их можно адаптировать для переноса генов в сердце. Тем не менее, вирусные векторы имеют такие недостатки, как стимулирование иммунного ответа хозяина и инсерционный мутагенез. Одной из альтернатив является прямая доставка трансгенной мРНК, которая позволяет избежать риска инсерционного мутагенеза и способствует быстрой экспрессии белка. Чтобы избежать иммунной активации, такая мРНК может быть химически модифицирована (chemically modified mRNA, CMmRNA) с использованием нуклеозидов, таких как псевдоуридин, 5-метилцитидин или 2-тиуридин.
Исследователи из Института сердца Седарс-Синайского медицинского центра в Лос-Анджелесе, США, работали над соматическим перепрограммированием клеток сердца. Ранее они уже показали, что вирусная доставка человеческого эмбрионального фактора транскрипции T-box 18 (TBX18) в сердце вызывает образование индуцированных клеток SAN (iSAN), которые биохимически и функционально напоминают клетки водителя ритма. В новой работе ученые перепрограммировали кардиомиоциты с помощью модифицированной мРНК человеческого TBX18 (CMmTBX18). Статья с результатами работы опубликована в журнале Cell Reports Medicine.
Сначала ученые модифицировали остатки уридина в мРНК TBX18 (CMmTBX18) с помощью 1-метилпсевдоуридин-5'-трифосфата. Они трансфицировали такую CMmRNA в желудочковые миоциты новорожденных крыс (NRVM) in vitro. Однократная трансфекция CMmTBX18 вызывала экспрессию белка TBX18 в желудочковых миоцитах, однако она была слабая и не могла поддерживаться более 24 часов даже при многократном введении. При этом акрифлавин, ингибитор Argonaute 2, повышал уровень экспрессии TBX18. Белки Argonaute связывают микроРНК (miR) и имеют эндонуклеазную активность по отношению к мРНК, находящимся в комплексе с ними, при реализации РНК-интерференции.
В ходе дальнейшей работы исследователи подтвердили, что трансляцию CMmTBX18 подавляют именно микроРНК. Секвенирование выявило две таких микроРНК (miR-1-3p и miR-1b), которые имели повышенную экспрессию в клетках, трансфицированных CMmTBX18, и несли комплементарную ей последовательность. Различные супрессивные miR также ограничивали экспрессию CMmRNA фактора роста эндотелия сосудов А (VEGF-A).
Исследователи разработали контрстратегии, которые привели к устойчивой экспрессии необходимых белков. Совместное введение антагонистов miR-1-3p и miR-1b с CMmTBX18 продлевало экспрессию белка TBX18. Клетки NRVM имели морфологию iSAN через 72 часа после трансфекции, которая была связана с экспрессией белков HCN4 и HCN2, что соответствовало соматическому перепрограммированию; оно оставалось устойчивым в течение как минимум одной недели. Эффективность такого подхода in vivo была подтверждена в экспериментах на крысах с атриовентрикулярной блокадой.
Таким образом, ученые выяснили, что клетки сердца сопротивлялись трансляции терапевтической CMmRNA за счет усиления экспрессии супрессорных miR. Подавление экспрессии трансгена с помощью miR не зависело ни от выбора химической модификации мРНК, ни от трансгена. Результаты работы имеют важное значение для общего использования CMmRNA. По мнению ученых, предложенные ими контрстратегии помогут повысить эффективность и результативность терапии с помощью CMmRNA.
Источник:
Sanchez L., et al. MicroRNA-dependent suppression of biological pacemaker activity induced by TBX18 // Cell Reports Medicine. 2022. 3, 100871 December 20. DOI: 10.1016/j.xcrm.2022.100871


 Меню
Меню





 Все темы
Все темы




 0
0