Мышечные столовые клетки жертвуют функциональностью ради выживания
В мышечных столовых клетках (MuSC) старых мышей на высоком уровне экспрессируется NDRG1 — ген-супрессор опухолей, подавляющий сигнальные пути многих факторов роста. Такие клетки не так активно участвуют в регенерации мышц после повреждения, как молодые с низким уровнем NDRG1. Однако MuSC с высоким уровнем экспрессии NDRG1 более устойчивы при стрессе. Исследователи предполагают, что мышечные столовые клетки с высоким уровнем экспрессии NDRG1 чаще сохраняются в организме мыши до старости, и, хотя они хуже способствует регенерации, это предпочтительнее ситуации, когда стволовых клеток не остается вовсе.
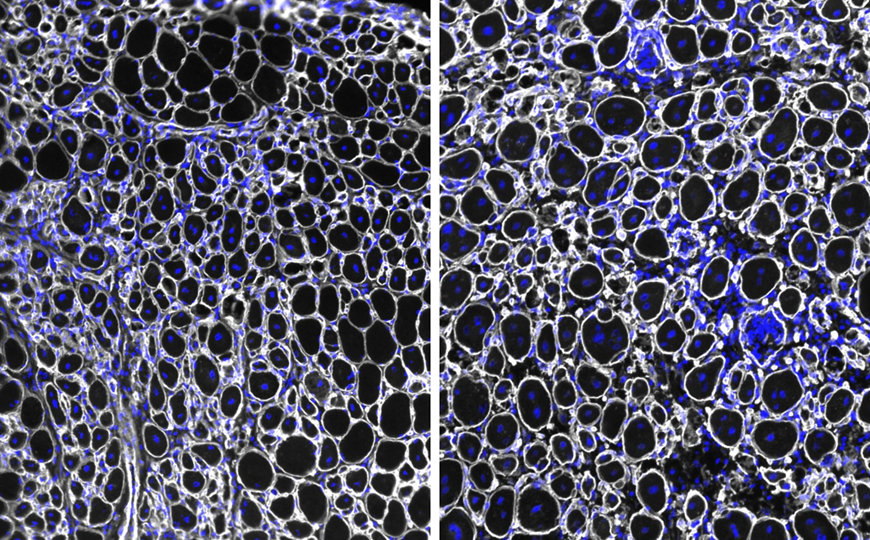
Мышечная ткань старых мышей через семь дней после травмы. Слева: у старых мышей с нормальным уровнем NDRG1 наблюдается более медленная регенерация с меньшими мышечными волокнами. Справа: у старых мышей с нокаутом NDRG1 наблюдается более быстрая регенерация с более крупными волокнами.
Credit:
Jengmin Kang, Rando Lab | Пресс-релиз
Стареющие ткани хуже восстанавливаются и регенерируют после повреждения. В скелетных мышцах это обусловлено снижением функции мышечных столовых клеток (MuSC) — они медленнее активируются и входят в клеточный цикл. Транскриптомный анализ MuSC подтвердил, что возраст в первую очередь влияет на клеточный цикл и пролиферацию. Однако механизм этих процессов плохо изучен.
Исследователи из США проанализировали транскриптомы MuSC молодых и старых мышей, которые различались значительно. Среди генов, кодирующих факторы роста и белки, вовлеченные в клеточный цикл, наибольшая разница в уровне экспрессии была у Ndrg1 (уровень экспрессии вырос в 3,5 раза в MuSC старых мышей). NDRG1 действует как ген-супрессор опухолей в различных типах клеток, подавляя сигнальные пути многих факторов роста.
Авторы работы получили мышей, у которых нокаут NDRG1 в MuSC можно индуцировать тамоксифеном, что и проделали в возрасте 20 месяцев. Через две недели MuSC изолировали из мышц генетически модифицированных мышей и мышей дикого типа. После нокаута NDRG1 MuSC чаще входили в S-фазу и накапливали митохондрии при активации, чем у контрольных мышей, так что эти показатели были сравнимы с молодыми мышами. При оценке регенерации после повреждения у старых мышей с нокаутом мышца восстанавливалась быстрее (у молодых разницы не было).
MuSC после нокаута NDRG1 чаще активировались, но и хуже выживали — покоящихся MuSC у таких мышей было меньше через 21 день после повреждения. И при двух последовательных повреждениях мышц у мышей с нокаутом второе повреждение заживало значительно хуже. Число MuSC снижалось после каждого повреждения.
Таким образом, NDRG1 мешает MuSC быстро активироваться и регенерировать мышцу, но одновременно способствует выживанию этих клеток. Если провести нокаут NDRG1 у молодых мышей, то у старых мышей будет меньший пул MuSC, а мышцы у них будут восстанавливаться хуже. Делеция NDRG1 не делала MuSC молодыми — были и другие факторы, негативно влияющие на их функцию.
Авторы задались вопросом — почему NDRG1 не был утрачен в ходе эволюции, если он не дает преимуществ в молодости, когда естественный отбор сильнее всего. Хотя нокаут NDRG1 не оказал существенного влияния на регенерацию молодых мышц после одной травмы, общее число MuSC снижалось. И в ответ на последующие травмы наблюдалось еще большее снижение общего числа мышечных стволовых клеток, а теперь — еще и нарушение регенерации.
Ученые изолировали молодые MuSC с наибольшим уровнем NDRG1 и сравнили их с MuSC с наименьшим уровнем NDRG1 тех же молодых мышей. NDRG1high MuSC хуже активировались, чем NDRG1low, в нескольких тестах. Оверэкспрессия NDRG1 не повлияла на выживаемость MuSC при нормальных условиях, но в экспрессирующие NDRG1 клетки лучше выживали при окислительном стрессе.
Последствия накопления NDRG1 в стареющих мышечных стволовых клетках для фенотипа опосредуются подавлением пути PI3K-AKT-mTOR. При нокауте NDRG1 в MuSC повышаются уровни экспрессии нескольких генов этого пути — PIK3CA, AKT1, PTEN и CXCR4.
Исследователи предположили, что со временем MuSC с низким уровнем NDRG1 элиминируются, как менее устойчивые, и остаются клетки с высоким уровнем экспрессии NDRG1, которые не могут поддерживать быструю регенерацию.
Таким образом, молекулярные изменения, связанные с клеточным старением, могут представлять собой положительные компенсаторные реакции. Снижение способности к регенерации кажется отрицательным последствием старения, но это повышает устойчивость стволовых клеток и позволяет избежать гораздо худшего результата — истощения пула стволовых клеток, что сделает регенерацию невозможной.
При миодистрофии нарушается регенерация мышечных волокон
Источник:
Jengmin Kang, et al. Cellular survivorship bias as a mechanistic driver of muscle stem cell aging // Science (2026), published 29 January 2026, DOI: 10.1126/science.ads9175


 Меню
Меню





 Все темы
Все темы




 0
0











