Немецкие ученые случайно усилили действие метронидазола против бактерии, вызывающей язвенную болезнь
Метронидазол — препарат первой линии для лечения инфекций, вызванных Helicobacter pylori. Однако он эффективен лишь в высоких концентрациях и в составе комбинированной терапии. Чтобы выяснить, с какими белками хеликобактера преимущественно взаимодействует метронидазол, ученые из Германии создали его алкиновые производные — белки, с которыми связана такая молекула, удобно детектировать. К их удивлению, эти молекулы-зонды для анализа белков лучше уничтожали H. pylori, чем сам метронидазол. Возможно, на их основе будут созданы новые препараты для лечения этой инфекции, повышающей риск язвенной болезни и рака желудка.
Helicobacter pylori — грамотрицательная бактерия, колонизирующая желудок человека. Хеликобактером инфицировано 43% населения мира, и хотя инфекция часто протекает бессимптомно, она может способствовать развитию гастрита и язвенной болезни, а постоянное воспаление увеличивает вероятность развития рака желудка и лимфомы слизистой оболочки. Для уничтожения хеликобактера назначается 7-дневная комбинированная терапия, включающая два противомикробных компонента — метронидазол и кларитромицин — и ингибитор протонной помпы, например омепразол. Однако в последнее время начали распространяться лекарственно-устойчивые штаммы хеликобактера. Кроме того, даже против чувствительных штаммов эффективны лишь достаточно высокие дозы метронидазола, что повышает вероятность побочных эффектов и нарушает состав микробиома кишечника. При этом механизм действия метронидазола и его клеточные мишени изучены недостаточно, чтобы разработать его улучшенный вариант.
Исследователи из Мюнхенского технического университета и Центра инфекционных заболеваний Гельмгольца (Германия) выполнили профилирование белков хеликобактера, с которыми взаимодействует метронидазол. Для этого они разработали специальные зонды — производные метронидазола, которые взаимодействовали с белками так же, как он, и легко детектировались. Неожиданно зонды оказались лучшими антимикробными препаратами, чем сам метронидазол.
Известно, что метронидазол вызывает окислительный стресс в клетках — восстановление нитрогруппы в его составе приводит к образованию реактивных радикалов, повреждающих ДНК и белки. Эту реакцию могут проводить бактериальные НАДФ Н-нитроредуктазы (мутации в их генах часто ассоциированы с устойчивостью). В присутствии кислорода токсичные радикалы снова превращаются в нетоксичную окисленную форму, что делает препарат более безопасным.
При этом оставалось неясным, повреждение каких именно белков критично для хеликобактера. Чтобы выяснить это, исследователи синтезировали зонды на основе метронидазола с алкиновой меткой (-C≡CH), присоединенной в различных положениях через эфирную или С-С связь. Мечение белков выполняли методом клик-химии: бактерии, выращенные в культуре, обрабатывали зондом, белки с присоединенным зондом помечали родаминазидом, затем меченые белки визуализировали на гель-электрофорезе и идентифицировали методом масс-спектрометрии.
Перед экспериментами зонды проверили на активность против хеликобактера, и неожиданно два эфира метронидазола (авторы назвали их Metro-P1 и Metro-P3) проявили активность в значительно меньших количествах, чем сам метронидазол. Их минимальные ингибирующие концентрации были ниже соответственно в 30 и 60 раз. Увеличение активности продемонстрировали все зонды с эфирной связью, тогда как зонды с алифатическими боковыми цепями были, напротив, менее активными, чем метронидазол.
Основными мишенями метронидазола оказались шаперон HpGroEL и тиолпероксидаза HpTpx. Шаперон — это белок, необходимый для правильного сворачивания других белков, что важно при появлении большого количества поврежденных молекул. Тиолпероксидаза необходима для выживания H. pylori в агрессивной среде желудка; этот фермент восстанавливает токсичные пероксиды до воды или спиртов.
Конечно, авторов заинтересовала повышенная антибактериальная активность эфирных производных метронидазола. Они исследовали их взаимодействие с мишенями и подтвердили, что производные прочнее связываются с HpTpx. Также проанализировали действие Metro-P1, Metro-P3 и еще нескольких похожих по строению эфирных производных метронидазола на клетки и мышей, зараженных хеликобактером. Новые соединения продемонстрировали благоприятные фармакологические профили и низкую цитотоксичность. Один из эфирных аналогов метронидазола, обозначенный MF-01, полностью уничтожил хеликобактер в желудке инфицированных мышей даже при очень низкой дозировке — 0,3 мг на килограмм веса в день.
Согласно гипотезе, выдвинутой авторами статьи, метронидазол и особенно его нитроимидазоловые эфиры вызывают окислительный стресс в бактериальной клетке и одновременно подавляют защитную реакцию на него. «Хотя для любой новой молекулы потребуются полные исследования безопасности и дозировок, тот факт, что 5-нитроимидазольные эфиры получены из клинически одобренного препарата, обеспечивает прочную основу для доклинической разработки», — говорится в заключении. Низкая токсичность, стабильность в плазме крове и фармакокинетические показатели уже полученных соединений практически не требуют оптимизации. Возможно, это шаг к безопасной и эффективной терапии инфекции H. pylori.
Источник
Fiedler, M.K., et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition // Nature Microbiology (2026). DOI: 10.1038/s41564-026-02291-w


 Меню
Меню





 Все темы
Все темы
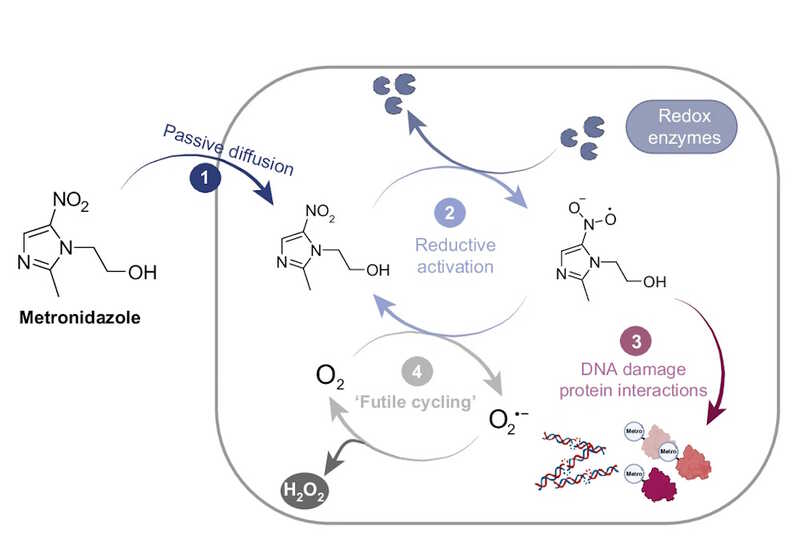 Credit: Nature Microbiology (2026). DOI:
Credit: Nature Microbiology (2026). DOI:




 0
0











