Новая флуоресцентная система показала, как онкогенные клетки вредят своим соседям
Ученые разработали репортерную систему Red2Onco, основанную на Cre-рекомбиназе, для наблюдения за влиянием онкогенных клеток на их соседей в криптах кишечника модельных мышей. Выяснилось, что даже на начальных этапах канцерогенеза стволовые клетки, экспрессирующие онкогены, подавляют пролиферацию соседних стволовых клеток.
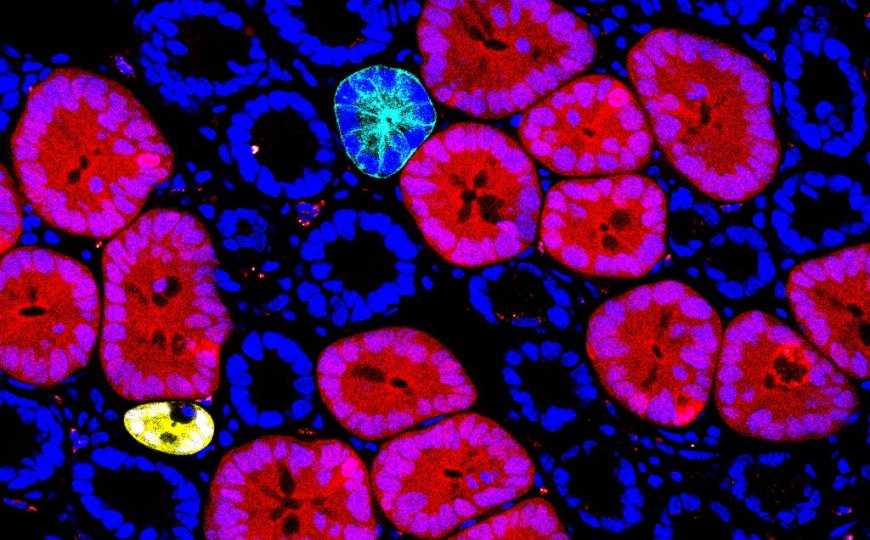
Credit: Yum/IMBA | Пресс-релиз
Начальные этапы канцерогенеза невозможно определить гистологически, поскольку изменения начинаются с мутации в единственной клетке. После того, как первая клетка мутирует и становится онкогенной, она по-прежнему полностью окружена нормальной тканью, и точно определить фенотип и дальнейшую судьбу этой клетки до сих пор не представлялось возможным. Чтобы преодолеть этот барьер, исследователи из Венского биоцентра и Кембриджа разработали систему для анализа предраковых стадий крипт кишечника мышей, основанную на флуоресцентных репортерах рекомбинации.
Система использует технологию многоцветной маркировки, которая позволяет отслеживать начало онкогенеза от одной мутантной клетки. Ученые создали новые репортеры на основе системы Confetti, которая, в свою очередь, является модификацией известной технологии многоцветного окрашивания популяции клеток Brainbow 2.1. Репортерная конструкция содержала loxP-сайты для Cre-рекомбиназы, ограничивающие стоп-кодоны перед генами четырех различных флуоресцентных белков. Экспрессия Cre-рекомбиназы индуцировалась тамоксифеном. После этого из конструкции вырезался стоп-кодон, и стохастически под промотор вставали последовательности, содержащие один из флуоресцентных белков. Из всех четырех только ген красного белка (RFP) был соединен с одним из трех исследованных онкогенов, NotchICD, Kras-G12D или PIK3CA-H1047R, с помощью саморазрушающегося пептида 2A. Полученную систему ученые назвали Red2Onco, так как она обеспечивает эффективную коэкспрессию RFP с белком, запускающим канцерогенез.
В качестве модели ученые использовали мышей, экспрессирующих Red2Onco в клетках тонкого кишечника. Они обнаружили, что мутантные клетки создают враждебную среду для своих соседей и в значительной степени нарушают регуляцию нормальных стволовых клеток в кишечных криптах. Авторы удивились, обнаружив, что клеточные клоны, экспрессирующие онкогены, со временем занимают все большую долю пространства в крипте. Чтобы понять механизм этого явления, они провели РНК-секвенирование единичных клеток. Выяснилось, что клетки, которые экспрессируют мутантные гены KRAS и PI3K, секретируют в окружающую среду лиганды BMP (костного морфогенетического белка). Это приводит к подавлению активности соседних с ними стволовых клеток.
Полученные результаты говорят о том, что экспрессия онкогенных белков создает среду, которая пагубно сказывается на нормальных клетках, находящихся рядом с потенциально канцерогенными. Однако авторы также показали, что теперь, зная о подобных эффектах, мы можем на них воздействовать. Ингибирование избыточного сигналинга BMP снижало влияние онкогенных клеток на нормальные.
Источник
Yum, M. K., et al. // Tracing oncogene-driven remodelling of the intestinal stem cell niche. // Nature (2021); DOI: 10.1038/s41586-021-03605-0


 Меню
Меню





 Все темы
Все темы




 0
0











