Новые линии мышей для редактирования эпигенома на основе системы CRISPR-Cas9
Ученые из университета Дюка в США создали две мышиные линии — Rosa26:LSL-dCas9-p300 и Rosa26:LSL-dCas9-KRAB — для таргетированных и органоспецифичных активации и подавления экспрессии генов. В геном мышей встроили последовательность белка dCas9, сшитого с эпигенетическими регуляторами p300 или KRAB. Экспрессия гибридного белка активировалась Cre-рекомбиназой. Авторы повысили уровень экспрессии гена Pdx1 в печени и Fos в мозге, а также снизили экспрессию гена Pcsk9 в печени.
Система CRISPR-Cas9 играет все большую роль в науке. Один из новых вариантов ее применения — редактирование эпигенома. Для этих целей белок Cas9, лишенный нуклеазной активности (dCas9), сшивают с белками, ремоделирующими хроматин. Однако такая конструкция довольно громоздка, ее доставка в ткани затруднительна и поэтому область ее применения in vivo ограничена. Одно из решений — создание линий мышей, в генах которых уже закодирована подобная конструкция, активируемая по сигналу.
Ученые из США создали две мышиные линии, в которых гены гибридного белка dCas9 и хроматин-ремоделирующего белка не экспрессируются из-за стоп-кодона, фланкированного сайтами loxP. Последовательность Cre-рекомбиназы под органоспецифичным промотором вместе с гидРНК доставляется в клетки аденоассоциированным вирусом. Удаление стоп-кодона запускает экспрессию гибридного белка. Ученые показали возможность экспрессии белка в селезенке, скелетных мышцах, печени, поджелудочной железе и сердце.
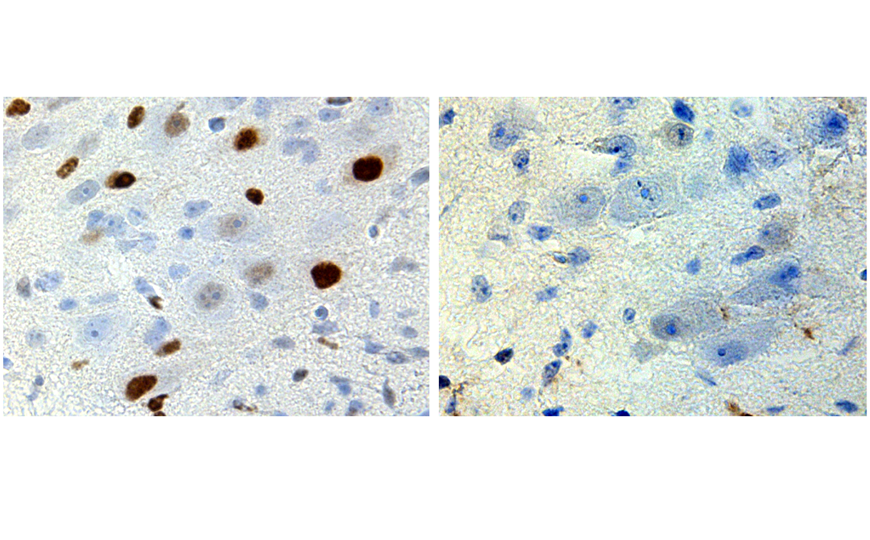
В качестве эпигенетического активатора был выбран белок p300. Садясь на промотор, он ацетилирует гистон H3 по лизину в 27 положении, что активирует транскрипцию. Авторы добились увеличения уровня мРНК гена Pdx1 в печени в несколько тысяч раз, а также изменения уровня экспрессии гена Fos в гиппокампе. На уровне физиологии мыши также были зафиксированы изменения. Для достижения органоспецифичности Cre-рекомбиназа находилась под регуляцией промоторов CBh и Syn1 соответственно.
Для подавления экспрессии использовали белок KRAB. Он трижды метилирует гистон H3 по лизину в 9 положении, что подавляет транскрипцию соответствующего гена. С помощью этой системы авторы снизили экспрессию гена Pcsk9 в печени на 90%. Кроме того, как активацию, так и подавление экспрессии гена Foxp3 провели ex vivo на первичных иммунных клетках.
При активации экспрессии с использованием белка p300 авторы столкнулись с небольшим изменением общего профиля экспрессии при использовании Cre-рекомбиназы и без целевой гидовой РНК. Таким образом, для верной интерпретации результатов необходимо использовать контроль без целевой гидРНК. В то же время белок KRAB подавлял экспрессию селективно.
Созданные линии мышей могут быть полезны для дальнейших исследований, в которых требуется осуществить подавление или активацию гена in vivo.
Источник
Gemberling M. P., et al. // Transgenic mice for in vivo epigenome editing with CRISPR-based systems //Nature Methods, 18, 965, 2021. DOI: 10.1038/s41592-021-01207-2


 Меню
Меню





 Все темы
Все темы




 0
0