Новый сенолитик активирует выведение сенесцентных клеток иммунной системой
Высокожировая диета способствует накоплению в организме мыши сенесцентных клеток, которые увеличивают уровень воспаления и способствуют инсулиновой резистентности. Исследователи из Японии показали, что на их число можно повлиять канаглифлозином — ингибитором SGLT2 (ключевого белка, вовлеченного в транспорт глюкозы). Это вещество снижает экспрессию PD-L1 на сенесцентных клетках, и они уничтожаются естественными киллерами и CD8+ T-клетками, число которых возрастает.
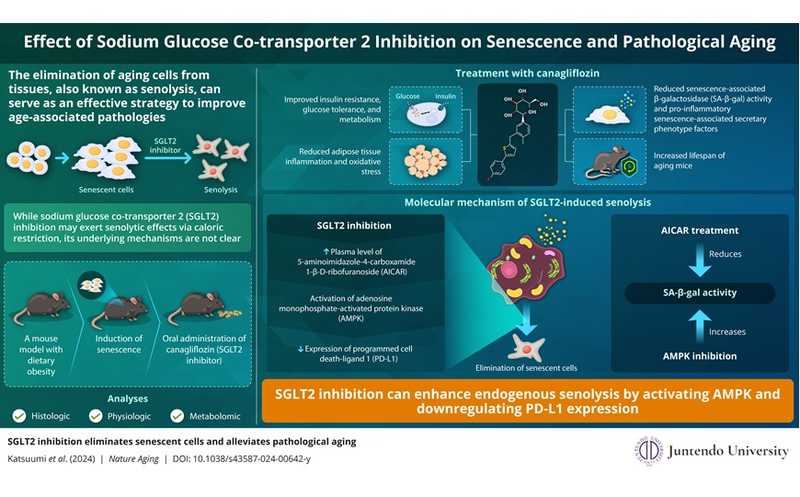
Считается, что накопление сенесцентных клеток в тканях способствует старению организма, а их элиминация (сенолизис) облегчает протекание ассоциированных со старением патологий. Появление сенесцентных клеток в адипозной ткани при ожирении увеличивает уровень воспаления и способствует инсулиновой резистентности, а делеция p53 (регулятора сенесценции) в адипозной ткани защищает от нарушений метаболизма, вызванных диетой. Однако прямое подавление регуляторов сенесценции также способствует опухолеобразованию, что нужно учитывать при разработке сенолитиков.
Ограничение калорий продлевает жизнь некоторым организмам, и это связано с меньшим числом сенесцентных клеток. Ранее было показано, что ингибиторы SGLT2 (ключевого белка, вовлеченного в транспорт глюкозы) подавляют накопление сенесцентных клеток. Ингибиторы SGLT2 снижают потребление калорий, так как глюкоза выводится с мочой. Исследователи из Японии предположили, что ингибиторы SGLT2 обладают сенолитическим эффектом. В новой работе они проверили это предположение и разобрались в механизмах сенолизиса.
Мышей содержали на высокожировой диете 8–10 недель, после чего им давали ингибитор SGLT2 канаглифлозин в течение семи дней. Кратковременный прием препарата не влиял на вес мышей, потребление еды или кислорода, но значительно улучшал инсулиновую резистентность по сравнению с контролями. Даже через неделю после окончания приема канаглифлозина метаболизм глюкозы улучшился у мышей на высокожировой диете.
Канаглифлозин препятствовал накоплению сенесцентных клеток в жировой ткани и других органах и тканях (например, в печени) и снижал активность ассоциированной с сенесценцией β-галактозидазы (SA-β-gal). Также снижалась экспрессия провоспалительных факторов связанного с сенесценцией секреторного фенотипа (SASP). Препарат снижал и другие проявления воспаления и окислительного стресса. Элиминацию сенесцентных клеток подтвердили на трансгенной линии мышей.
Авторы предположили, что кратковременный прием канаглифлозина элиминирует сенесцентные клетки через снижение уровня глюкозы в крови. Чтобы проверить это предположение, мышей содержали на высокожировой диете 8–10 недель, потом давали инсулин в течение недели. Инсулин улучшал инсулиновую резистентность, не влияя на вес тела или жировую массу. Однако число сенесцентных клеток или воспаление не снизились. Четыре недели приема инсулина не повлияли на активность SA-β-gal в жировой ткани. Перевод мышей с высокожировой на нормальную диету также не снижал активность SA-β-gal. Таким образом, эффект канаглифлозина не объяснялся только нормализацией метаболизма глюкозы.
Молодые и сенесцентные клетки человека обрабатывали канаглифлозином. Даже высокие концентрации препарата не действовали на клетки напрямую. Метаболомный анализ мышей, получавших препарат, выявил высокие концентрации метаболита AICAR (5-аминоимидазол-4-карбоксимид-1-β-D-рибофуранозида), активирующего протеинкиназу AMPK (AMP-activated protein kinase).
Сенесцентные клетки активируют иммунную систему через секрецию факторов SASP. Активация иммунной системы, по-видимому, поддерживает гомеостаз и выводит сенесцентные клетки. При старении и патологиях этот механизм не работает, эти клетки накапливаются и провоцируют развитие хронического воспаления. Недавно было показано, что PD-L1 экспрессируется на некоторых популяциях сенесцентных клеток и подавляет их элиминацию.
Известно, что AMPK подавляет экспрессию PD-L1. Авторы подтвердили это в новой работе. У мышей на высокожировой диете повышалось число PD-L1+ сенесцентных клеток, а при введении канаглифлозина это число снижалось, что сопровождалось увеличением количества естественных киллеров и CD8+ T-клеток.
Канаглифлозин замедлял преждевременное старение у мышей с нокаутом Zmpste24. Если давать препарат мышам среднего возраста (50 недель) в течение 20 недель, у них значительно повышается физическая активность и снижается активность SA-β-gal.
Сенолитик — потенциальный препарат для терапии болезни Альцгеймера — проникает в ЦНС
Источник:
Goro Katsuumi, et al. SGLT2 inhibition eliminates senescent cells and alleviates pathological aging // Nature Aging (2024), May 30, 2024, DOI: 10.1038/s43587-024-00642-y


 Меню
Меню





 Все темы
Все темы




 0
0