Перепрограммирование цитокиновых сигналов в T-клетках затормозило рост опухолей у мышей
Цитокины — крайне важные для Т-клеток сигнальные молекулы. «Алфавит» их сигналов мог бы быть куда шире, если бы варианты сигнальных путей JAK-STAT, которые активируются при узнавании цитокина рецептороv, опирались и на неканонические взаимодействия. «Расширением» этого алфавита занялись ученые из Стэнфорда (США), опубликовавшие статью в Nature. Они получили T-клетки с химерными вариантами цитокиновых рецепторов, не встречающихся в природе, и показали, что внутриклеточные механизмы их активации выходят за рамки тех, которые индуцируются естественными цитокинами. Разработку предлагают применять, в частности, для лечения онкозаболеваний — ее уже протестировали на мышиных моделях рака.
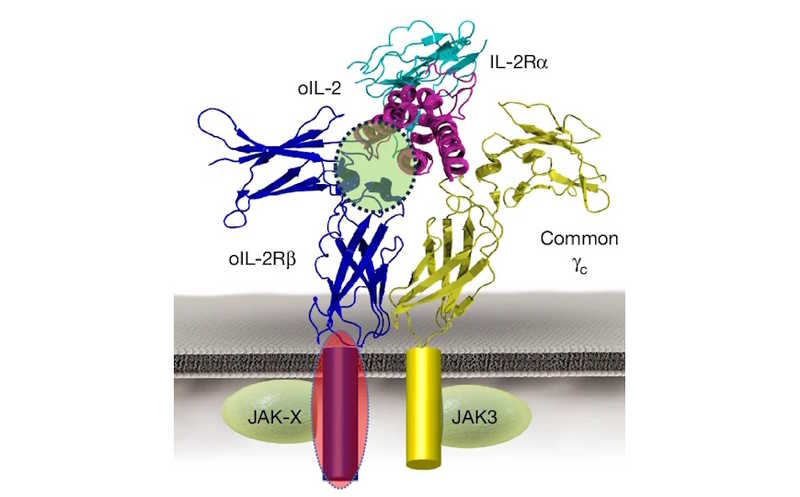
Цитокины играют важную роль в управлении активностью и дифференцировкой T-клеток. Рецепторы к ним в норме экспрессируются на поверхности Т-клеток и обычно активируются димеризацией, которая запускает JAK-STAT сигналинг. Однако цитокиновых рецепторов существует более трех десятков, а в семейство JAK-киназ входят только четыре белка. Авторы статьи в Nature рассудили, что комбинаторное разнообразие цитокиновых сигналов может быть куда шире, если задействовать еще и неканонические взаимодействия.
Для расширения сигнального кода ученые комбинировали общую гамма-цепь рецепторов интерлейкинов (γc) с рецепторными молекулами, активирующими JAK-STAT. Они применили ортогональную платформу с мутантным интерлейкином-2 (oIL-2) и мутантным же рецептором к нему (oIL-2Rβ). Их внеклеточные домены избирательно связываются друг с другом, но не с вариантами дикого типа.
Исследователи получили мышиные T-клетки, которые экспрессировали oIL-2Rβ или химерные рецепторы на его основе — внеклеточный домен был мутантный, а трансмембранный и внутриклеточный заменены на таковые от других цитокиновых рецепторов. Химерный рецептор, содержащий сигнальную часть, например, IL-4R, обозначался как o4R.
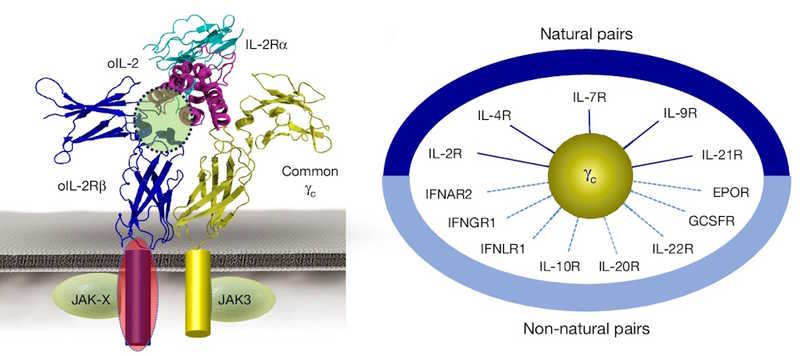 Строение цитокинового рецептора, содержащего γc, и варианты пар, на основе которых можно построить его модифицированную версию.
Строение цитокинового рецептора, содержащего γc, и варианты пар, на основе которых можно построить его модифицированную версию.Credit:
Nature (2025). DOI: 10.1038/s41586-025-09393-1 | CC BY-NC-ND
Авторы проанализировали сигналинг природных димеров γc с цитокиновыми рецепторами (IL-4R, IL-7R, IL-9R, IL-21R). С ними сравнили неканоничные димеры, которые состояли из γc и JAK1-ассоциированных рецепторов (IFNAR2, IFNGR1, IFNLR1, IL-10R1, IL-20R, IL-22R), а также GCSFR и EPOR.
Мышиный oIL-2, сцепленный с сывороточным альбумином для повышения стабильности, дозозависимо индуцировал сигналы pSTAT в мышиных Т-клетках, экспрессирующих ортогональные химерные рецепторы. Лиганд индуцировал гетеродимеризацию и активацию JAK1/2 (основная цепь) и JAK3 (γc). Конструкты, основанные на природных димерах, запускали ожидаемые канонические ответы, o9R и o21R также активировали STAT4.
Химеры с сигнальной частью IFN преимущественно индуцировали ответ через STAT1, причем наиболее мощную активацию вызывал oIFNLR1. Сигнал от o10R обеспечивался в основном через STAT3; o22R активировал STAT1, STAT3, STAT4 и STAT5, а o20R преимущественно действовал через STAT3, хотя активировал и остальные тоже. Наконец, oGCSFR индуцировал pSTAT3 и умеренно затрагивал STAT1 и pSTAT5, а oEPOR демонстрировал слабую активацию STAT5.
Затем авторы проанализировали транскриптомные профили ответов на ортогональные рецепторы. Анализ главных компонент (PCA) выявил отчетливую кластеризацию по внутриклеточному сигналингу: при активации oIFNLR1 и oIFNAR2 клетки группировались с немодифицированными Т-лимфоцитами, обработанными IFNα, IL-21 и IL-10 тесно сгруппировались с их ортогональными парами, передающими сигнал через STAT3. Экспрессия нижележащих в сигнальном каскаде генов согласовалась с этим: oIFNLR1 индуцировал гены под контролем STAT1; o10R и o21R (в меньшей степени также o22R) активировали STAT3-зависимые гены; а o4R — STAT6-зависимые.
Таким образом, ортогональные рецепторы воспроизводят нативные программы STAT и одновременно диверсифицируют клеточные ответы, обеспечивая γc-зависимую активацию не-γc-рецепторов.
Чтобы оценить функциональную роль различных профилей STAT, авторы вводили модифицированные Т-клетки мышам с меланомой. Перед лечением животные подвергались лимфодеплеции. Все варианты показали хорошую переносимость. Среди γc-химер наиболее высокую противоопухолевую активность обеспечил o4R, активирующий STAT6. При этом 1 из 8 мышей достигла полной ремиссии. Химеры рецепторов IFN также сдерживали рост опухоли, и oIFNLR1 обеспечил полный ответ на лечение у 1 из 8 мышей. Крайне эффективными себя показали химеры, основанные на внутриклеточных сигналах IL-10 — среди них o22R обеспечил полную ремиссию у 3 из 9 мышей. Наконец, гомодимерные рецепторы oEPOR и oGCSFR также сдерживали опухоли; oGCSFR вызвал полную ремиссию у 2 из 8 мышей.
Авторы дополнительно проанализировали РНК единичных CD8+ T-клеток, выделенных из опухоли. Они рассмотрели четыре наиболее эффективных против опухоли варианта: o4R, o20R, o22R и oGCSFR. Наибольшая доля CD8+ опухоль-инфильтрирующих Т-лимфоцитов отмечалась при экспрессии o22R (4,62%), за которыми следовали oGCSFR (2,03%), o20R (1,67%) и o4R (0,7%). В контроле их было 0,45%. Более детальное изучение показало, что искусственные цитокиновые сигналы формируют разнообразные профили Т-клеток — они отличались в том числе экспрессией цитотоксических молекул и активностью пролиферации.
Анализ генных регуляторных сетей выявил, что oGCSFR направляет Т-клетки по пути миелоидной дифференцировки, а o4R индуцирует перепрограммирование в цитотоксические и хелперные Т-клетки 2 типа — их недавно связывали с лучшими исходами CAR T-терапии, однако до сих пор не было надежного способа индуцировать и поддерживать их популяцию in vivo.
Наконец, исследователи оценили потенциал Т-клеток, несущих o22R и oGCSFR, на ксенографтных моделях опухолей. Они подсаживали иммунодефицитным мышам клетки лимфомы (линия NALM6), а затем вводили им CAR T-клетки, нацеленные на человеческий CD19. CAR T-клетки, несущие человеческий o22R (ho22R) и hoGCSFR активнее привлекались к опухолевым клеткам. Уровень истощения, оцененный по экспрессии PD-1 и LAG3, у них был ниже, а секреция цитотоксических молекул IFNγ и гранзима B оставалась стабильной.
Результаты опытов на ксенографтной модели солидной опухоли (меланомы) позволяют предположить, что ho22R и hoGCSFR эпигенетически перепрограммируют опухоль-инфильтрирующие лимфоциты. Такое перепрограммирование повышает потенциал терапевтических Т-клеток к самообновлению и защищает от истощения, что усиливает противоопухолевый ответ.
Таким образом, авторы расширили «алфавит» цитокиновых сигналов — они воспользовались перекрестными взаимодействиями и гетеродимерной активацией цитокиновых рецепторов JAK-STAT. Вмешавшись в нее при помощи ортогональной системы IL-2, которая зависит от эндогенного Т-клеточного γc, они дополнили существующую систему цитокинового сигналинга и предложили способы применения своей разработки.
Химерные цитокиновые рецепторы повышают эффективность CAR-T терапии солидных опухолей
Источник
Zhao, Y., et al. Expanding the cytokine receptor alphabet reprograms T cells into diverse states. // Nature (2025). DOI: 10.1038/s41586-025-09393-1


 Меню
Меню





 Все темы
Все темы




 0
0