Почему беременным нельзя принимать лекарства с вальпроевой кислотой
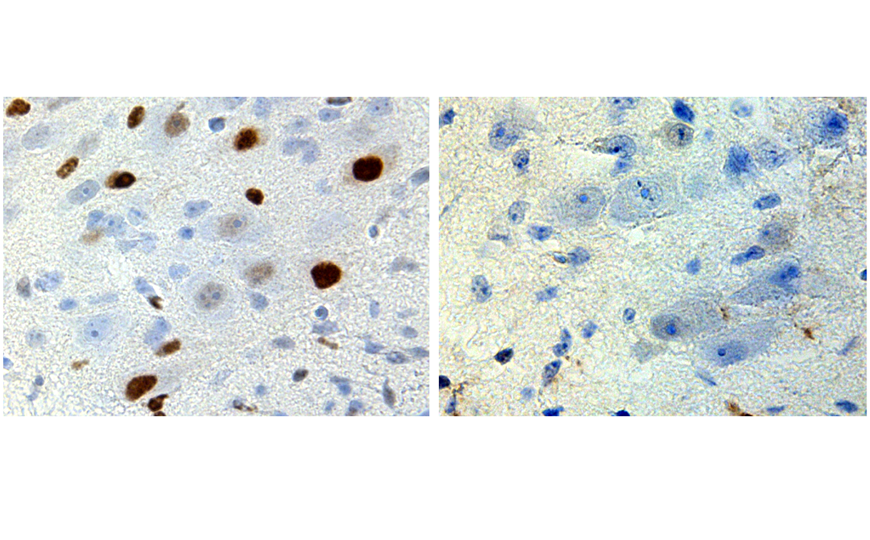
Французские ученые впервые описали молекулярный механизм формирования врожденных дефектов развития у детей, который связан с действием вальпроевой кислоты. Она содержится в препаратах для лечения мигрени, эпилепсии и биполярного расстройства. Исследователи выяснили, что вальпроевая кислота препятствует нормальному росту и делению клеток эмбриона, вызывая клеточное старение в нейроэпителиальных и стволовых клетках, дающих начало ЦНС.
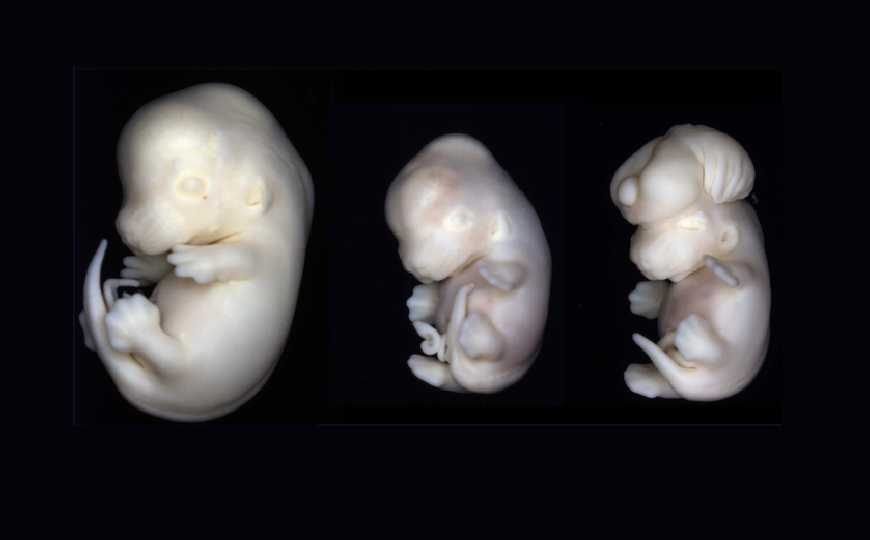
Нормальный эмбрион мыши (слева) и эмбрионы, подвергнутые действию вальпроевой кислоты.
Credit:
Muriel Rhinn
(CC-BY 4.0)
К настоящему времени зарегистрированы тысячи случаев, когда женщины во время беременности принимали препараты для лечения мигрени, содержащие вальпроевую кислоту (valproic acid, VPA), и впоследствии у них рождались дети с тяжелыми пороками развития. В их числе — пороки развития сердца, экзэнцефалия, микроцефалия и т.д. Однако чаще, примерно у трети младенцев, возникают когнитивные нарушения и расстройства аутистического спектра (РАС) без какой-либо серьезной деформации тела. Считалось, что эти отклонения возникают на ранних этапах развития нервной системы (на стадии закрытия нервной трубки), но как именно VPA вызывает эти дефекты, оставалось неизвестным. Предполагалось, что VPA действует в качестве ингибитора гистондеацетилазы (HDACi), напрямую активируя медиаторы клеточного старения, в том числе p21, p16 Ink4a и p19 Arf.
Научный коллектив во главе с Уильямом Кейзом из Института генетики, молекулярной и клеточной биологии (Франция) изучил, может ли аберрантная активация старения под воздействием VPA способствовать нарушению эмбриогенеза. В экспериментах анализировались эмбрионы мышей и органоиды — трехмерные кластеры клеток головного мозга человека.
Введение трех доз препарата беременным мышам вызвало у их потомства экзэнцефалию — дефект головного мозга, при котором он располагается вне черепа, а также микроцефалию и другие пороки развития. Эти фенотипические изменения были заметны даже на ранних стадиях развития мозга мышат и повторяют особенности воздействия VPA на людей.
Дальнейшие эксперименты показали, что VPA вызывает нарушение нейрогенеза, при этом в деформированных тканях эмбрионов мышей обнаружена выраженная индукция старения в нейроэпителиальных клетках (NE). Затем ученые проверили, влияет ли такое аберрантное старение на более позднее развитие коры. В норме NE должны дифференцироваться в предшественников нейронов. У эмбрионов, подвергшихся воздействию VPA, количество предшественников и нейронов значительно снижено. Эти данные связывают раннее аберрантное старение в NE клетках эмбриона со снижением нейрогенеза и нарушением развития коры.
Чтобы выяснить, вызывает ли VPA аналогичные процессы в нейроэпителиальных клетках человека, специально выращенные церебральные органоиды обработали VPA в различных концентрациях и на соответствующих стадиях развития. Результаты исследования оказались близкими — VPA вызвал выраженную индукцию старения в клетках NE, что связано с заметным снижением пролиферации и нейрогенеза. Однако интересно было узнать, есть ли функциональная связь между аберрантным старением и нарушением нейрогенеза. Для этого были использованы генетические модели — беременных мышей, каждая из которых дефицитна по одному из генов основных медиаторов старения (p21, p19 Arf или p16 Ink4a ). Их «лечили» VPA и оценивали фенотипы эмбрионов. Удивительно, но у эмбрионов, дефицитных по генам p21 и p16 Ink4a, не было видимых улучшений ни по одному фенотипу. У эмбрионов, дефицитных по гену p19 Arf, введение VPA не вылечивало от экзэнцефалии, но спасало от микроцефалии. Таким образом, удалось идентифицировать один из ключевых медиаторов процесса старения — p19 Arf.
По словам авторов, эта работа — одна из первых, в которой клеточное старение связывается с дефектами развития. «Хотя клеточное старение долгое время ассоциировалось со старением организма и возрастными заболеваниями, теперь очевидно, что аберрантная индукция старения также может способствовать дефектам развития. Поскольку вальпроевая кислота тесно связана с когнитивными дефектами и расстройствами аутистического спектра, необходимы дополнительные исследования».
Источник
Rhinn M., et al. Aberrant induction of p19Arf-mediated cellular senescence contributes to neurodevelopmental defects. // PLoS Biol 2022. 20(6): e3001664. DOI: 10.1371/journal.pbio.3001664
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0