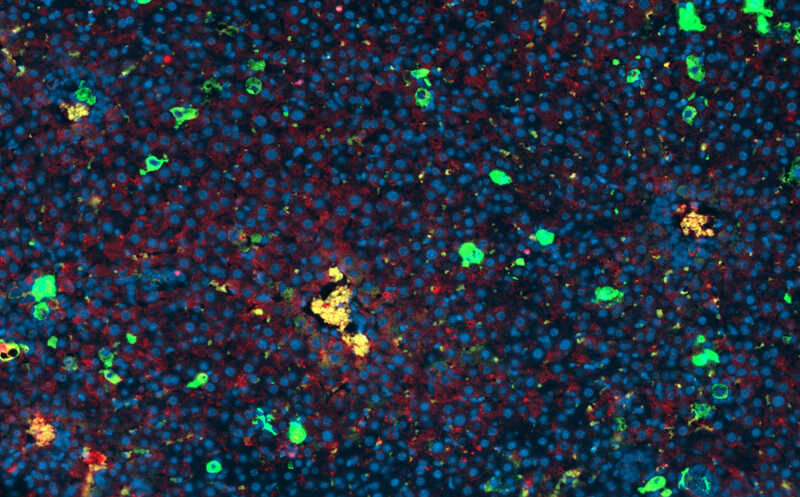
«Починка» ослабленного кишечного барьера замедляет воспалительное старение
Исследование ученых из Испании, США и Японии показало, что нарушение барьерной и иммунной функций кишечника выступает одной из причин старения. Мыши с нарушенной иммунной системой ускоренно теряли массу тела, страдали от мышечной слабости и рано погибали. Пересадка нормальных T-клеток замедляла у них воспалительное старение (инфламмейджинг) за счет восстановления целостности кишечного барьера и нормализации взаимодействия с микробиотой.

С возрастом в организме снижается эффективность иммунного ответа, особенно T-клеточного звена. Это нарушает взаимодействия кишечной микробиоты с организмом хозяина, приводит к повреждениям эпителиального барьера и хроническому воспалению, а в итоге способствует развитию мультиморбидности — сочетания нескольких возрастных заболеваний. Одним из важнейших факторов считается повышение проницаемости кишечника, которое способствует проникновению микробных продуктов в системный кровоток и активации воспалительных каскадов. Однако причинно-следственные связи в этих процессах оставались неизученными.
Чтобы установить их, исследователи из Испании, США и Японии\ использовали генетически модифицированных мышей Tfamfl/flCd4Cre с нарушенной функцией митохондрий в T-клетках. У этих животных примерно с 4–8 месяцев наблюдалась прогрессирующая потеря массы тела, связанная с развитием мультиморбидного фенотипа. На более поздней стадии, характеризующейся кахексией и резкой потерей веса (0,31 г в неделю), у них развивалась гиперпроницаемость кишечного барьера, которую подтвердили пероральным введением FITC-декстрана. Также обнаружились выраженные нарушения структуры тканей кишечника — удлиненные ворсинки, гиперплазия крипт, инфильтрация воспалительными клетками и отечность. Секвенирование РНК тканей толстой кишки выявило активацию сигнальных путей, связанных с воспалением, цитотоксичностью, старением и фиброзом, а также снижение экспрессии ключевых белков плотных межклеточных контактов, таких как ZO-1 и окклюдин.
Метагеномный анализ, проведенный по генам 16S рРНК, выявил значительные изменения в составе микробиоты. В подвздошной и толстой кишке мышей снижались количества полезных симбиотических бактерий, таких как Lactobacillus или представители семейства Ruminococcaceae. Доля микробов, ассоциированных с воспалением (в том числе Enterobacteriaceae), напротив, возрастала. Эти изменения в составе микробных сообществ сопровождались аномальной продукцией короткоцепочечных жирных кислот и указывали на устойчивый дисбиоз.
Чтобы оценить роль микробиоты в развитии патологии, ученые давали мышам на поздней стадии патологии антибиотики. Удаление дисбиотических микробных сообществ способствовало укреплению эпителиального барьера; оно замедлило распространение бактерий и их метаболитов на периферию и восстановило экспрессию генов плотных контактов. Одновременно в крови мышей снижались уровни провоспалительных цитокинов (IFN-γ, TNF, IL-6) и маркеров старения (Cdkn1a, Tp53). У животных улучшались физиологические показатели, включая мышечную силу, глюкозотолерантность и рефлексы, а медианная продолжительность жизни выросла на 71% (с 327 до 560 дней). Однако вопрос о первичности нарушений оставался открытым.
Переходя к иммунной составляющей, авторы сосредоточились на цитометрическом анализе CD4+ T-клеток в пейеровых бляшках и собственной пластинке слизистой кишечника. У мышей с нарушенным митохондриальным метаболизмом было резко снижено количество наивных, фолликулярных и регуляторных Т-клеток (Treg), причем сами клетки приобретали активированный и цитотоксический фенотипы. Они секретировали больше провоспалительных цитокинов, таких как TNF и IFN-γ, и активно экспрессировали хемокин CCL5. Выработка IgA усиливалась до патологических уровней, приводя к гиперопсонизации кишечных микроорганизмов и системной экспозиции IgA.
Ключевым экспериментом стал адоптивный перенос иммунокомпетентных CD4+ T-клеток от молодых животных дикого типа мышам Tfamfl/flCd4Cre. Через 7 недель донорские клетки составляли 46% CD4 T-клеток в крови, а через 2 месяца — почти 60% в лимфоидных органах кишечника. Восстановились пулы наивных, фолликулярных и регуляторных T клеток, снизилось количество воспалительных T-лимфоцитов. В толстой кишке доля Treg-клеток удвоилась, активировались герминативные центры, снизился уровень IgA-опсонизации микробов, а микробный состав нормализовался — увеличилась доля Lactobacillus и снизилась доля Enterobacteriaceae. Для уточнения роли Treg авторы провели дополнительный эксперимент — популяцию CD4+ T-лимфоцитов для переноса обогащали регуляторными Т-клетками. Это также восстановило иммунный профиль в крови и пейеровых бляшках. Обе стратегии снижали инфильтрацию CD8+ T-клетками и долю среди них KLRG1+ лимфоцитов, ассоциированных со старением.
На транскриптомном уровне наблюдалось восстановление экспрессии генов, ответственных за барьерную функцию, а также ослабление сигнатур воспаления, цитотоксичности, старения и фиброза. Иммунофлуоресцентное окрашивание на ZO-1 и окклюдин подтвердило, что их экспрессия частично восстановилась. Уровень проницаемости кишечника у животных снижался. Также уменьшались уровни IFNγ, IL-6, TNF, CXCL1 и CXCL10 в крови, равно как и экспрессия маркеров старения Cdkn1a и Tp53. Таким образом, терапия CD4+ T-клетками имела геропротективный эффект.
Результаты работы демонстрируют, что нарушение иммунного надзора в кишечнике — не следствие, а одна из причин старения организма. Поддержание нормального пула CD4+ Т-клеток, особенно с регуляторным фенотипом, критически важно для замедления воспалительного старения (инфламмейджинга) и продления здоровой жизни. Полученные данные открывают перспективы для разработки стратегий, направленных на укрепление кишечного барьера и восстановление микробиоты в контексте возраст-ассоциированных заболеваний.
Если клетка «думает», что у нее избыток нутриентов, старение организма ускоряется
Источник
Manuel M. Gómez de las Heras et al. ,CD4 T cell therapy counteracts inflammaging and senescence by preserving gut barrier integrity. // Sci. Immunol. 10, eadv0985 (2025). Published online: 1 August 2025. DOI: 10.1126/sciimmunol.adv0985


 Меню
Меню





 Все темы
Все темы




 0
0