Предложена новая генная терапия для «людей-бабочек»
Причиной буллезного эпидермолиза — гиперчувствительности кожи к механическим повреждениям — могут быть мутации в различных генах. В новом исследовании отредактированные клетки больных с мутациями в гене COL7A1 после пересадки мышам продемонстрировали признаки здоровой кожи.
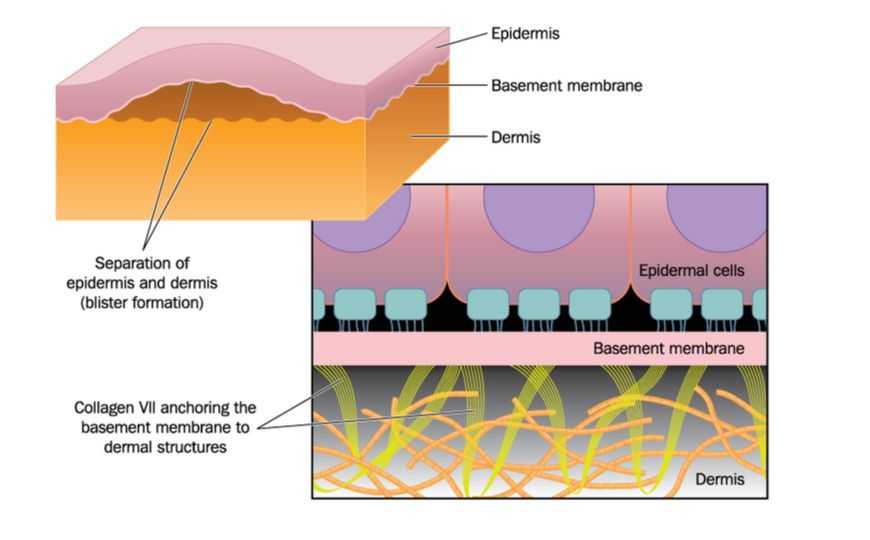
Мутации в гене коллагена VII (на схеме показан желто-зеленым) ослабляют связь между эпидермисом и дермой. Credit: Blamb | Shutterstock.com
Буллезный эпидермолиз — группа тяжелых наследственных заболеваний, для которых характерна гиперчувствительность и ранимость кожи, повреждения в ответ на прикосновения незначительной силы. В СМИ больных буллезным эпидермолизом часто называют «людьми-бабочками». Лечение в основном симптоматическое, хотя в 2017 году была публикация о пересадке пациенту трансгенной кожи, выращенной из его собственных клеток с заменой гена LAMB3.
Буллезный эпидермолиз генетически гетерогенен, в частности, рецессивный дистрофический буллезный эпидермолиз (РДБЭ) вызывается мутациями в другом гене, COL7A1, кодирующем коллаген типа VII (C7), причем тяжесть заболевания зависит от типа мутации. C7 — основной компонент фибрилл заякоривания в зоне базальной мембраны, в норме он обеспечивает связь между эпидермисом и нижележащими слоями кожи.
Одобренных методов лечения этого заболевания в настоящее время не существует. Однако исследователи из США, Японии и Мексики продемонстрировали возможности генной терапии и в этом случае. С помощью CRISPR-Cas9 и гомологично-направленной репарации (то есть дополнительного введения в клетку одноцепочечной ДНК с «правильной» последовательностью гена, которая служит матрицей для редактирования), они исправили мутации гена COL7A1 в индуцированных плюрипотентных стволовых клетках (ИПСК), полученных от двух пациентов с РДБЭ. У одного была гомозиготная мутация в экзоне 19, второй был гетерозиготным: в одном аллельном варианте COL7A1 у него присутствовала мутация в экзоне 19, в другом — в экзоне 32. Для первого удалось добиться 58%-ной биаллельной и 42%-ной моноаллельной коррекции, для второго — 19%-ной биаллельной и 48%-ной моноаллельной.
Из отредактированных ИПСК, дифференцированных в кератиноциты и фибробласты, получили так называемые трехмерные эквиваленты человеческой кожи и привили их иммунодефицитным мышам. У мышей после трансплантации нормально экспрессировался C7, через два месяца восстановились фибриллы заякоривания в базальной мембране. Нецелевого редактирования CRISPR-Cas9 выявлено не было.
Это исследование подтверждает, что применение тканевой инженерии в сочетании с редактированием гена может быть положено в основу терапии рецессивного дистрофического буллезного эпидермолиза; искусственно выращенный эквивалент кожи из трансгенных клеток, пересаженный на раневую поверхность, поможет закрытию незаживающих ран.
Источник
Joanna Jacków, et al. // CRISPR/Cas9-based targeted genome editing for correction of recessive dystrophic epidermolysis bullosa using iPS cells. // PNAS, 2019, DOI: 10.1073/pnas.1907081116


 Меню
Меню





 Все темы
Все темы



 0
0











