Регенерации кожи препятствует активный рост нервов вокруг раны
Кожные раны у эмбрионов млекопитающих могут заживать без рубцов, но после рождения эта способность утрачивается. Исследователи из Гарварда обнаружили, что она не исчезает, а блокируется, и ее можно восстановить. В блокировке участвует особый подтип фибробластов, окружающих рану, которые вызывают активный рост нервных волокон. Оказывается, гипериннервация раны не только повышает болевую чувствительность, но и препятствует регенерации. Подавление роста нервных окончаний в области раны у пятидневных мышат обеспечило восстановление кожи с волосяными фолликулами, капиллярами и другими сложными структурами.
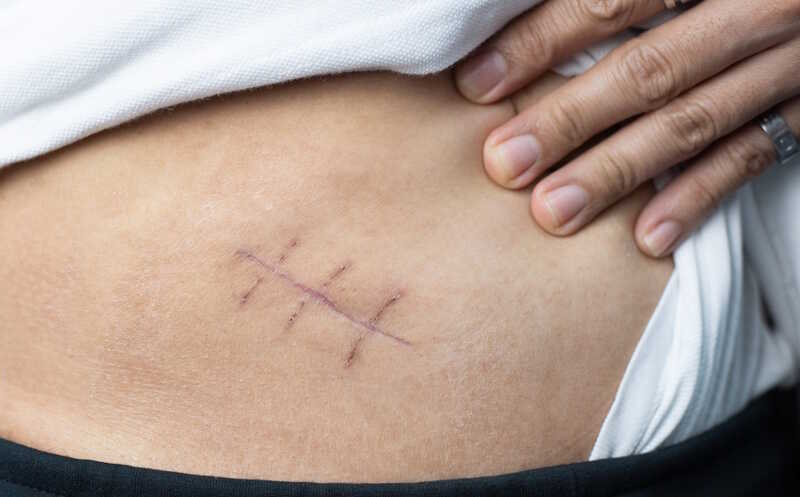
У человека и других млекопитающих при заживлении раны образуется рубец. Заживление без рубца, с восстановлением первоначальной структуры ткани, — важная цель не только из-за борьбы с косметическими дефектами: рубцевание нарушает функции органа. Исследователи из Гарвардского университета и Гарвардской медицинской школы нашли способ разблокировки эмбриональных механизмов регенерации и проверили его на мышах.
Практически у всех млекопитающих регенерация органов, состоящих из разных клеточных линий, сильно ограниченна — может регенерировать кончик пальца. (Хотя существуют и исключения, иглистые мыши, о которых рассказывал Олег Гусев.) Кожа — пример высокорегенеративной ткани. После ранения эпидермальные стволовые клетки закрывают рану, а фибробласты формируют плотную коллагеновую рубцовую ткань. Однако нормальная кожа содержит десятки типов различных клеток и структур — волосяные фолликулы, кровеносные и лимфатические сосуды, потовые железы, пигментные клетки, иммунные клетки, жировые клетки и нервы. В рубце большинство из них не присутствуют.
Эмбрионы млекопитающих до определенного момента развития заживляют раны без образования рубцов. Новорожденные мыши могут регенерировать кардиомиоциты, аксоны спинного мозга и волосяные фолликулы, но способность к регенерации быстро снижается, а склонность к образованию рубцов увеличивается. Тем не менее, согласно новым данным, регенеративный потенциал можно реактивировать у взрослого организма.
Первый автор статьи в Cell, Ханна Там, в настоящее время сотрудник Исследовательского института Скриппс в Калифорнии, уже пять лет занимается этой тематикой. Она выполняла микрохирургические операции на эмбрионах и новорожденных мышах. Инструментом для биопсии удаляли участок кожи на всю толщину мышатам в течение 16-го дня эмбрионального развития, то есть примерно за три дня до рождения; сразу после рождения, на второй, пятый и 24-й день. Затем сравнивали, как заживала ранка у эмбриональных и постнатальных мышей. На эмбрионах места заживших повреждения было сложно найти, приходилось отмечать их флуоресцентными шариками, введенными в рану, и «чернилами» с хной.
Способность кожи к регенерации начинала снижаться еще у эмбрионов. Самые сильные изменения происходили с третьего дня до рождения по пятый день после рождения. У мышей, раненных пренатально, новая кожа была похожа на неповрежденную, в ней присутствовали различные типы клеток. Формировались волосяные фолликулы с мышцами, поднимающими волос, капилляры, лимфатические сосуды и все остальные сложные структуры. Волокна коллагена располагались непараллельно, аналогично нормальной коже. Авторы даже убедились, что новая кожа покрывается мурашками на холоде, то есть все типы клеток демонстрируют согласованный ответ на физиологическое воздействие.
В то же время у мышат возрастом пять дней ранка закрывалась эпителиальными клетками и заполнялась коллагеновой рубцовой тканью с волокнами, параллельными поверхности кожи, в которой присутствовали аномально плотные нервные волокна и иммунные клетки, но не другие структуры и типы клеток.
Секвенирование РНК единичных клеток из раны и кожи вокруг нее у эмбрионов мышей и у пятидневных мышат подтвердило присутствие всех известных клеток и продемонстрировали различия как в составе клеточных популяций, так и в активности генов. Например, по периферии раны у новорожденных мышат, но не у эмбрионов появляется особый подтип специфических для раны фибробластов (postnatal wound-specific fibroblasts, PWF), а также присутствует больше нейтрофилов и макрофагов, экспрессирующих провоспалительные сигнальные молекулы.
Исследователи попыталась определить ключевые факторы, отвечающие за различие регенеративных способностей. Они предположили, что клетки PWF экспрессируют какие-то белки, которые подавляют регенерацию. Чтобы найти гены-кандидаты, они сравнили гены, активно вырабатываемые PWF, с другими наборами генов, предположительно подавляющих регенерацию. (Это были гены, экспрессия которых выше в фибробластах взрослых людей, чем в эмбриональных; гены, экспрессия которых повышена в ранах на спине северного оленя по сравнению с ранами на коже, покрывающей рога; и наконец, гены, экспрессия которых выше в рубцовых ранах кожи человека по сравнению с нерубцующимися ранами слизистой оболочки полости рта, которая, как известно, хорошо регенерирует.)
В результате был получен «короткий список» из девяти генов, и гены из него авторы поочередно оверэкспрессировали в эмбриональных ранах (для этого копии генов доставляли в клетки с помощью вирусных векторах.) Оверэкспрессия генов Ccl7, Cxcl12 или Timp1 нарушала регенерацию кожи эмбриона. В частности, она способствовала формированию скопления нервных окончаний в месте раны — гипериннервации. Особенно сильным было влияние Cxcl12, который также вызывал чрезмерное утолщение эпидермиса, но при этом не повышал количество иммунных клеток в раневое ложе (хотя Cxcl12 и Ccl7 часто рассматриваются как хемокины, привлекающие иммунные клетки).
Гипериннервация в раневых ложах также наблюдается человека, где она ассоциируется с постраневой гиперчувствительностью, но ее роль в подавлении регенерации до сих пор не была исследована. Ханна Там говорит, что сначала команда «зашла в тупик», поскольку предполагала, что угнетение регенерации связано с иммунными клетками. Прорыв произошел, когда они обнаружили, что настоящее препятствие — это гипериннервация: именно ее отключение делает возможной полноценную регенерацию кожи.
Когда исследователи истощили запасы Cxcl12 в ранах у мышей после рождения, «гипериннервация» была подавлена, и в коже восстановился рост различных типов клеток. Аналогичный результат дала обработка раны ботоксом, блокирующим местный нервный сигналинг. На иммунные клетки эти воздействия не влияли.
«Блокировка возникает из-за взаимодействия фибробластов и нервных волокон, — говорит Ханна Там. — Взаимосвязь между этими двумя различными типами клеток не была предметом исследований в области заживления ран. (…) Теперь мы можем рассматривать эти два типа клеток как реальных участников коммуникации».
CXCL12 — многофункциональный секретируемый фактор, для которого предполагают участие как подавлении регенерации, так и в ее поддержке, но его влияние через гипериннервацию до сих пор не рассматривалось. Незрелые нервные волокна могут выделять избыточное количество нейротрансмиттеров и нейропептидов, которые препятствуют регенеративным генным программам. Высокая плотность новых аксонов может физически препятствовать росту волосяных фолликулов и других структур в дерме.
Утрата способности к регенерации по мере роста и развития организма встречается в животном царстве практически повсеместно. Однако убрать блокировку работающего механизма намного проще, чем выстроить его с нуля, отмечают авторы. Это вселяет надежду на создание терапевтических препаратов, способствующих регенерации.
Регенерация против фиброза: почему ранки во рту заживают быстро и без шрамов?
Источники
Hannah T. Tam, et al. Hyperinnervation inhibits organ-level regeneration in mammalian skin // Cell. March 20, 2026. DOI: 10.1016/j.cell.2026.02.027


 Меню
Меню





 Все темы
Все темы




 0
0











