Регулятор системы комплемента DAF служит фактором вирулентности в мышиной модели гриппа
В экспериментах на мышах ученые обнаружили, что дефицит фактора ускорения распада комплемента (DAF) защищает животных от плохих исходов при заражении вирусом гриппа A. Комплексный анализ показал, что взаимодействие DAF с гемагглютинином и нейраминидазой усиливает иммунопатологический эффект инфекции.
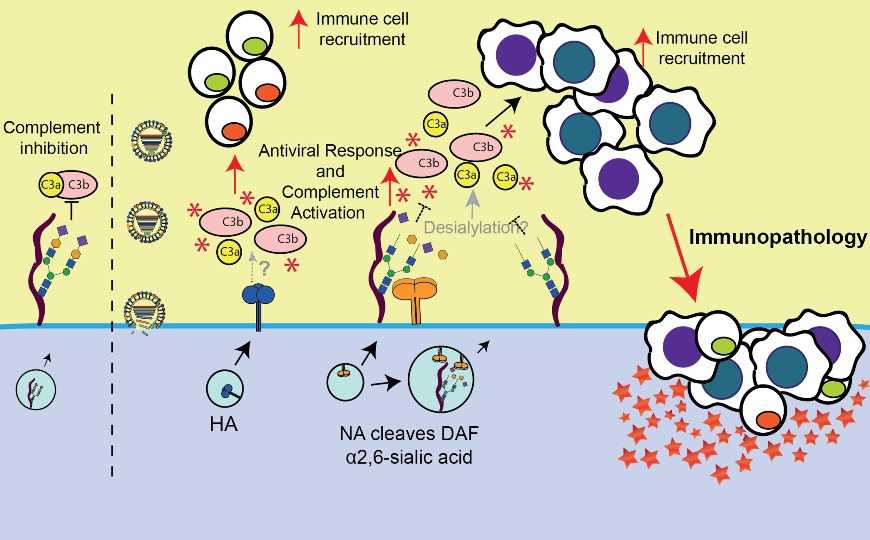
Credit: Nuno Brito Santos, et al., 2021; DOI: 10.1371/journal.ppat.1009381 | CC BY 4.0
До сих пор неясно, как регуляция активации системы комплемента влияет на тяжесть респираторных вирусных инфекций. Команда ученых из Португалии в экспериментах на мышах определила вклад одного из компонентов системы комплемента, фактора ускорения распада комплемента (DAF), в тяжесть протекания инфекции, вызванной вирусом гриппа A (IAV). Полученные ими результаты не соответствуют ожиданиям, основанным на более ранних исследованиях.
DAF способствует распаду C3-конвертаз, защищая здоровые клетки от атаки системой комплемента. Известно, что у людей дефицит DAF приводит к избыточной активации комплемента, что влечет за собой системные нарушения. Более того, SNP в промоторной области DAF, снижающие экспрессию продукта, ассоциированы с повышенным риском тяжелых инфекций при заражении пандемическим или птичьим гриппом.
В новой работе ученые заражали мышей с нокаутом Daf (Daf-/-) и мышей дикого типа различными штаммами IAV. Тяжесть инфекции оценивалась по потере веса и выживаемости в течение 11 дней после заражения. К удивлению ученых, мыши Daf-/- не так сильно теряли в весе, как мыши дикого типа, и выживаемость их была значительно лучше. Это означает, что DAF усиливал разрушительный эффект инфекции IAV, а его отсутствие, напротив, защищало мышей от гибели. Единственным штаммом, вызвавшим гибель всех мышей Daf-/-, оказался высоковирулентный PR8.
Чтобы определить механизм, обеспечивающий защиту мышам Daf-/-, ученые поставили серию опытов с животными, нокаутными по различным компонентам системы комплемента, провели иммуногистохимический анализ легочной ткани и определили состав иммунных клеток и цитокинов в бронхоальвеолярном лаваже. Животных заражали штаммом PR8-HK4,6, обладающим умеренной вирулентностью. Оказалось, что выключение других регуляторов комплемента не дает такого же эффекта при инфекции IAV, как нокаут DAF, что говорит об исключительной роли последнего. Защитный эффект нокаута DAF не был связан с цитотоксичностью или цитолитическими атаками, опосредованными системой комплемента.
Отсутствие DAF не влияло на вирусную нагрузку и распределение вируса в легочной ткани. При этом легкие инфицированных мышей Daf-/- были поражены в меньшей степени, чем легкие мышей дикого типа, что было связано с меньшим количеством клеток врожденной иммунной системы (нейтрофилов и моноцитов) и более низким уровнем провоспалительных цитокинов. Это означает, что отсутствие DAF защищало мышей от иммунопатологии. Нокаут главного регулятора комплемента DAF был связан с меньшей степенью активации системы комплемента, что, по мнению авторов, интересно и нелогично.
Защита, обусловленная нокаутом DAF, не работала при заражении мышей более вирулентным PR8. Штаммы PR8-HK4,6 и PR8 несут различаются по гемагглютинину (HA) и нейраминидазе (NA). Чтобы установить причины штаммоспецифичности защиты, ученые проверили серию экспериментов in vivo и in vitro с использованием химерных вирусов, несущих HA и NA в различных комбинациях, и других приемов. Было показано, что взаимодействие DAF с HA ухудшает исход инфекции у мышей. Нокаут DAF снижает активацию адаптивного иммунного ответа, что вкупе с повышенной вирулентностью штамма может объяснить высокую смертность мышей Daf-/- при заражении штаммом PR8. Различные NA при этом давали разную картину ответа врожденной иммунной системы, а взаимодействие DAF с NA влияло на привлечение в легкие нейтрофилов и моноцитов. Кумулятивный эффект взаимодействий DAF с HA и NA приводит к ухудшению исхода инфекции.
NA обладает сиалидазной активностью. DAF, в свою очередь, является высокосиалированным белком. Оказалось, что NA вырезает сиаловые кислоты, связанные с O-гликанами в составе DAF, и это нарушает регуляторные функции последнего. При этом чем выше ферментативная активность NA, тем сильнее активируется система комплемента.
Таким образом, IAV модулирует иммунный ответ хозяина, изменяя хозяйский белок. По мнению ученых, полученные результаты позволяют считать DAF новым фактором вирулентности при заражении IAV.
Источник
Santos NB, Vaz da Silva ZE, Gomes C, Reis CA, Amorim MJ // (2021) Complement Decay-Accelerating Factor is a modulator of influenza A virus lung immunopathology. // PLoS Pathogens 17(7): e1009381; DOI: 10.1371/journal.ppat.1009381


 Меню
Меню





 Все темы
Все темы




 0
0










