Специфическое ацетилирование гистонов способствует развитию болезни Альцгеймера
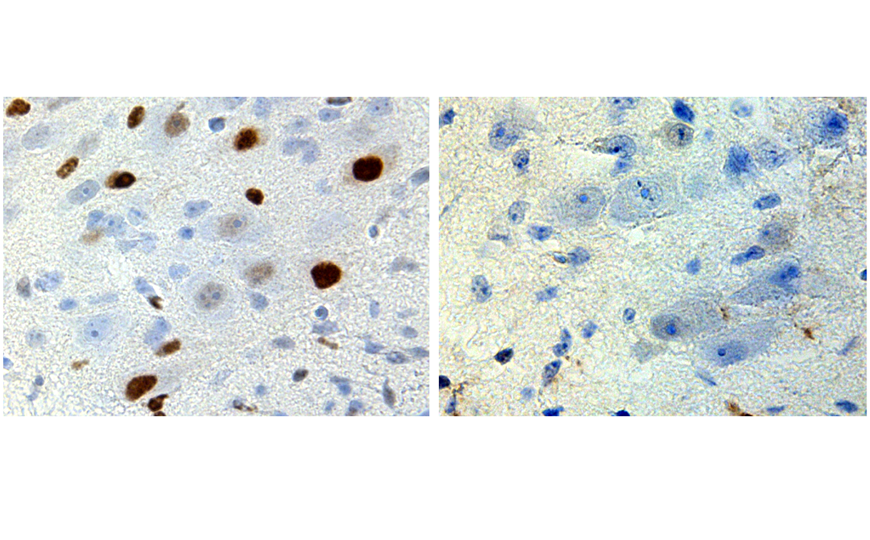
Ученые использовали комплексный мультиомиксный подход к изучению постмортальных образцов мозга пациентов с болезнью Альцгеймера и показали, что с заболеванием ассоциированы ацетилированные варианты гистона H3 — H3K27ac и H3K9ac. Их функциональная значимость была подтверждена in vivo на плодовых мушках.
К характерным признакам болезни Альцгеймера относятся накопление бета-амилоидов и формирование нейрофибриллярных клубков в мозге. Однако молекулярные механизмы развития болезни до сих пор были неясны. Чтобы определить молекулярные пути, вовлеченные в патогенез заболевания, группа ученых из США применила комплексный мультиомиксный подход к изучению постмортальных образцов мозга пациентов.
Ранее этой же командой были сформированы базы транскриптомных данных для образцов боковой части височной доли от 12 пациентов с болезнью Альцгеймера (средний возраст 68 лет) и 18 индивидов без заболевания. Последние были разделены на две группы: более пожилая (10 индивидов, средний возраст 68 лет) и более молодая (8 индивидов, средний возраст 52 года). Выборка индивидов более молодого возраста была включена в исследование для того, чтобы можно было различить в результатах изменения, связанные с болезнью Альцгеймера и с возрастом.
Анализ транскриптомных баз показал, что при болезни Альцгеймера наблюдается существенная апрегуляция 421 гена и даунрегуляция 434 генов. Ученые обратили внимание, что при заболевании повышается экспрессия генов, ответственных за регуляцию транскрипции и структуру хроматина, в том числе генов гистонацетилтрансфераз. Для оценки изменений на уровне хроматина авторы провели протеомный анализ тех же образцов, сосредоточившись на посттрансляционных модификациях гистонов. Они обнаружили сдвиги метилирования и ацетилирования гистонов в образцах от пациентов с болезнью Альцгеймера по сравнению с образцами здорового мозга. У пациентов наблюдалось аномальное ацетилирование гистонов с увеличением уровней вариантов H3K27ac и H3K9ac гистона H3, что соответствовало результатам транскриптомного анализа.
Авторы предположили, что повышение уровней H3K27ac и H3K9ac при болезни Альцгеймера имеет функциональное значение и способствует аберрантной эпигенетической активации. Это предположение было подкреплено сопоставлением полученных данных с результатами проведенного ранее GWAS: среди SNP, ассоциированных с заболеванием, присутствуют варианты, соответствующие модификации H3K27ac.
Наконец, ученые оценили функциональную значимость H3K27ac и H3K9ac in vivo на модельных плодовых мушках (Drosophila). Было показано, что повышенная активность H3K27ac и H3K9ac способствует дегенерации глаз, вызванной накоплением амилоида Aβ42.
Таким образом, авторы выявили эпигеномные изменения, ассоциированные с болезнью Альцгеймера, и идентифицировали H3K27ac и H3K9ac как потенциальные драйверы заболевания, вызывающие нарушения регуляции транскрипции.
«Ранее мы показали, что определенные ацетильные метки защищают мозг во время нормального старения, а сейчас обнаружили, что другие ацетильные метки способствуют заболеванию. Следующим шагом будет определение защитных и разрушающих молекулярных механизмов, что в конечном итоге приведет к более точному подходу к терапии болезни Альцгеймера», — говорит один из руководителей исследования доктор Рафаэлле Нативио, профессор биологии, клеточной биологии и биологии развития Медицинской школы Перельмана Пенсильванского университета.
Источник
Nativio, R., et al. // An integrated multi-omics approach identifies epigenetic alterations associated with Alzheimer’s disease. // Nature Genetics 52, 1024–1035 (2020); DOI: 10.1038/s41588-020-0696-0
Цитата по пресс-релизу

 Меню
Меню





 Все темы
Все темы




 0
0