Специфичный для человека энхансер отличает болезнь Пика от болезни Альцгеймера
Ученые из США сопоставили эпигеном и транскриптом отдельных клеток префронтальной коры при болезни Пика (БП) и болезни Альцгеймера (БА), выявив как общие, так и уникальные регуляторные механизмы. Выяснилось, что при БП сильнее всего страдают возбуждающие нейроны и олигодендроциты, тогда как при БА основные изменения приходятся на микроглию. Особое внимание авторов привлек специфичный для человека энхансер, регулирующий транскрипцию убиквитинлигазы UBE3A, — он активировался только при БП, а экспрессия его мишени парадоксальным образом снижалась. Понимание того, что отличия между БА и БП лежат прежде всего в архитектуре регуляторных сетей, а не в отдельных генах, важно для разработки будущих терапий.
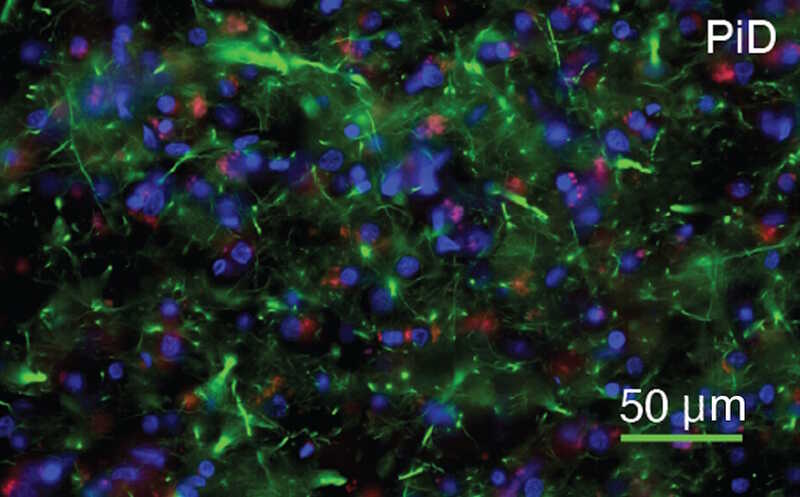
Credit:
Science Advanсes (2025). DOI: 10.1126/sciadv.ads7973 | CC BY
Понимание того, как при разных нейродегенерациях нарушается работа клеток мозга, остается одной из самых трудных задач современной биомедицины. Болезнь Альцгеймера (БА) изучена достаточно глубоко — десятки консорциумов картируют активность микроглии, сигнальные сети и генетические риски. Болезнь Пика (БП) — редкая фронтотемпоральная деменция (FTD), при которой патологический тау-белок формирует характерные скопления — тельца Пика. Симптомы прогрессируют стремительно и тяжело, но из-за редкости случаи БП почти не попадают в масштабные проекты, и молекулярный ландшафт болезни остается слабо охарактеризованным.
Чтобы восполнить этот пробел, исследователи из США картировали регуляцию генов на уровне отдельных ядер клеток мозга и сравнили эти данные между БП, БА и здоровыми людьми. Мультиомиксный анализ охватывал хроматин, транскрипцию, регуляторные связи и факторы транскрипции. Отдельное внимание авторы уделили тому, какие регуляторные элементы (особенно дистальные энхансеры) действительно влияют на активность генов, и как именно изменяются сигнальные пути в разных типах клеток.
Ученые проанализировали единичные ядра с помощью ATAC-seq и секвенирования РНК (snRNA-seq). Для анализа они взяли образцы префронтальной коры людей с БП и контрольных доноров, а затем сопоставили эти данные с ранее собранным аналогичным набором для БА. После фильтрации авторы получили десятки тысяч ядер для каждого метода, выделили основные типы клеток мозга и подтвердили их по маркерным генам. Это позволило сравнить изменения в нейронах, микроглии, астроцитах и олигодендроцитах.
Сначала исследователи собрали единый набор из более чем 600 тысяч пиков открытого хроматина и обнаружили, что распределение пиков по промоторам, интронам и дистальным элементам при БП и БА очень похоже, что говорит о стабильности базовой организации регуляторных элементов. С помощью анализа совместной доступности хроматина они сопоставили дистальные регуляторные элементы с их потенциальными мишенями. Это позволило выделить модули регуляции, характерные для конкретных клеточных функций: синаптических процессов в нейронах, пролиферации в олигодендроцитах, фагоцитоза в микроглии.
Затем ученые интегрировали эти данные с результатами полногеномного поиска ассоциаций (GWAS) для БА и форм FTD. Оказалось, что большая часть однонуклеотидных полиморфизмов (SNP), связанных с риском БА, попадает в открытый хроматин микроглии, подтверждая ее ключевую роль в патогенезе. Но такие гены, как ADAM10, BIN1, PICALM и SORL1 оказались эпигенетически затронуты и в нейронах, и в клетках глии. Авторы нашли несколько FTD-ассоциированных локусов, также экспрессия которых меняется и при БП — это позволяет предположить, что часть генетики FTD может быть релевантна и для болезни Пика.
Следующим этапом стал анализ транскрипционных факторов (ТФ), для оценки связаывания которых с ДНК авторы применили футпринтинг. При БП наблюдалось падение активности множества ТФ в нейронах — гораздо более выраженное, чем при БА, — хотя отдельные факторы транскрипции, наоборот, активировались. При этом часть выявленных изменений была общей для обеих болезней (например, активация RORA, фактора, участвующего в метаболизме липидов). Некоторые ТФ, например, ассоциированный с апоптозом JDP2, напротив, усиленно связывались с ДНК только при БА. Авторы заключили, что болезнь Пика отличается от болезни Альцгеймера не просто набором задействованных генов, а принципиальной архитектурой регуляторных сетей.
Одним из генов, отличавших БП от БА, оказался UBE3A, который снижался только при первом из двух заболеваний. Он кодирует E3 убиквитинлигазу. Авторы обнаружили связанный с ним энхансер, приобретенный человеком в ходе эволюции. Он оказался дистальным регулятором, будучи расположен более чем в 40–80 кб от UBE3A. При БП доступность этого энхансера повышалась, что парадоксально сопровождалось снижением экспрессии UBE3A — это похоже на компенсаторный регуляторный ответ.
Чтобы проверить, действительно ли эта область функционирует как энхансер, авторы вырезали ее с помощью CRISPR-Cas9 из генома нейронов, полученных из ИПСК. В таких клетках экспрессия UBE3A значительно снизилась, что подтвердило регуляторную роль этого участка. Более того, RNA-seq анализ отредактированных нейронов выявил изменения в убиквитинировании, метаболизме и организации хроматина, подчеркивая чувствительность нейронов к потере функции UBE3A.
Анализ тканей мозга подтвердил, что UBE3A в префронтальной коре пациентов с БП снижен на уровне белка и мРНК, но доступность его энхансера повышена. Тот же парадоксальный паттерн был выявлен при анализе единичных нейронов, что говорит о системной, а не локальной дисрегуляции.
В целом полученная карта демонстрирует, что у БП и БА есть общие процессы патогенеза — синаптические нарушения, стрессовые реакции, изменения в активности глии. Однако болезнь Пика сильнее поражает нейронально-олигодендроцитарную ось, а болезнь Альцгеймера — микроглиальную. И эти различия выражаются не столько в самих генах, сколько в их регуляции: работе транскрипционных факторов, активности энхансеров и архитектуре хроматина.
Болезнь Альцгеймера сопровождается рассинхронизацией нервной и сосудистой систем
Источник
Shi Z., et. al. Single-nucleus multi-omics identifies shared and distinct pathways in Pick’s and Alzheimer’s disease. // Science Advanсes (2025), published online 12 November 2025. DOI: 10.1126/sciadv.ads7973


 Меню
Меню





 Все темы
Все темы




 0
0