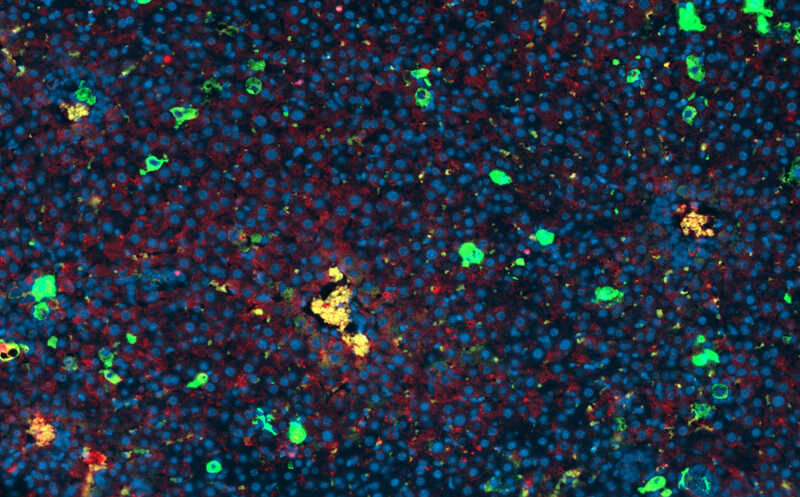
Утечка митохондриальной РНК и активация РНК-сенсинга при сенесценции клеток
Клеточное старение сопровождается развитием воспалительного секреторного фенотипа (SASP), однако его молекулярные причины описаны не до конца. Ученые из США и Испании показали, что при сенесценции митохондриальная РНК накапливается в цитозоле и активирует сенсоры врожденного иммунитета RIG-I и MDA5. Это запускает воспалительные программы и способствует формированию SASP. Утечка митохондриальной РНК зависит от пермеабилизации митохондрий и не связана с апоптозом. Подавление сигнального пути, обеспечивающего пермеабилизацию митохондриальной мембраны, ослабляло признаки сенесценции в модели метаболически ассоциированного стеатогепатита у мышей. Авторы предлагают использовать обнаруженный механизм в качестве мишени для терапии возраст-ассоциированного воспаления.
Клеточное старение (сенесценция) представляет собой устойчивую остановку клеточного цикла, возникающую в ответ на повреждения ДНК, онкогенный стресс или истощение репликативного потенциала. Несмотря на защитную роль сенесценции как противоопухолевого механизма, сенесцентные клетки активно секретируют провоспалительные цитокины, хемокины и факторы ремоделирования матрикса — их объединяют в ассоциированный с сенесценцией секреторный фенотип (SASP). Хроническое воздействие SASP приводит к дисфункции тканей, воспалению и развитию возраст-ассоциированных заболеваний. Ранее было показано, что митохондрии играют ключевую роль в развитии этого фенотипа, в частности за счет утечки митохондриальной ДНК (mtDNA) в цитозоль и последующей активации пути cGAS–STING. Однако другой возможный фактор — митохондриальная РНК (mtRNA) — оставался неизучен в данном контексте. При попадании в цитоплазму mtRNA может оказывать сильный иммуногенный эффект, поскольку ее нуклеотиды лишены защитных модификаций. Ученые из США и Испании проанализировали, накапливается ли mtRNA в цитозоле сенесцентных клеток, какие сигнальные пути она активирует и как это влияет на формирование SASP.
Для анализа авторы использовали несколько моделей клеточной сенесценции: репликативную, индуцированную ионизирующим излучением и химиотерапией. С помощью сверхразрешающей микроскопии и субклеточного фракционирования они показали, что в сенесцентных фибробластах двуцепочечная mtRNA накапливается в цитозоле. Параллельно возрастала экспрессия сенсоров РНК (компонентов врожденного иммунитета) — RIG-I, MDA5 и TLR3.
Функциональную роль mtRNA подтвердили, искусственно внося ее в пролиферирующие фибробласты. Такая обработка приводила к индукции ключевых компонентов SASP и усилению экспрессии сенсоров РНК. Чтобы исключить влияние других митохондриальных функций, авторы использовали модель Parkin-опосредованной митофагии и полностью удаляли митохондрии из сенесцентных клеток. В такие клетках по-прежнему останавливался клеточный цикл, но практически не развивался SASP. Повторное введение mtRNA частично восстанавливало воспалительный транскрипционный профиль, включая интерфероновые и NF-κB-зависимые гены. Сравнение эффектов mtRNA и mtDNA показало, что они активируют как общие, так и уникальные для каждой из них наборы воспалительных генов.
Дальнейшие эксперименты показали, что mtRNA в сенесцентных клетках напрямую связывается с RIG-I и MDA5, что приводит к агрегации адаптерного белка MAVS — ключевого компонента противовирусного сигналинга. Нокаут RIG-I, MDA5 или MAVS резко снижал экспрессию SASP-факторов, не затрагивая саму остановку клеточного цикла, что указывает на избирательную роль этого пути именно в воспалительном компоненте сенесценции.
Однако как именно происходит утечка mtRNA в цитозоль? Авторы показали, что она требует образования макропор во внешней мембране митохондрий, формируемых проапоптотическими белками BAX и BAK — процесса, ранее описанного как неполная митохондриальная пермеабилизация (miMOMP). Делеция BAX и BAK снижала выход mtRNA, активацию сенсоров РНК, агрегацию MAVS и формирование SASP. Транскриптомный анализ выявил общие для подавления miMOMP и РНК-сенсинга сигнальные пути — они были связаны с регуляцией NF-κB-зависимых генов.
Физиологическую значимость этого механизма авторы подтвердили in vivo на модели метаболически ассоциированного стеатогепатита (MASH). У мышей с вызванным диетой поражением печени наблюдались в гепатоцитах признаки сенесценции, активация сенсоров РНК и выраженное воспаление. Специфичный нокаут BAX/BAK или подавление MAVS в гепатоцитах снижал экспрессию SASP-факторов и воспалительных маркеров, а также ослаблял инфильтрацию печени иммунными клетками, не влияя на массу печени и показатели апоптоза.
Таким образом, митохондриальная РНК — независимый и функционально значимый сигналом опасности в сенесцентных клетках. Ее утечка в цитозоль через BAX/BAK-зависимые поры активирует сенсоры врожденного иммунитета RIG-I и MDA5, приводит к агрегации MAVS и запуску воспалительных программ. Это, в свою очередь, свособствует формированию сенесцентного секреторного фенотипа SASP. Полученные результаты расширяют представление о молекулярной природе SASP и указывают на сенсоры РНК как на перспективную мишень для подавления возраст-ассоциированного воспаления без устранения самих сенесцентных клеток.
Предотвратить развитие нейровоспаления у старых мышей после операции могут сенолитики
Источник
Victorelli S., et. al. Mitochondrial RNA cytosolic leakage drives the SASP. // Nature Communications (2025), published online 15 December 2025. DOI: 10.1038/s41467-025-66159-z


 Меню
Меню





 Все темы
Все темы




 0
0