Вирус Зика избегает иммунитета, перемещаясь по туннельным нанотрубкам
Инфекция беременной женщины вирусом Зика способна вызвать патологии развития плода. Однако механизмы, обеспечивающие вертикальную передачу вируса и его уход от иммунного ответа, в том числе плацентарного, ранее не были описаны. Ученые из США установили, что вирус Зика вызывает в зараженных клетках формирование особых структур — туннельных нанотрубок, — через которые могут транспортироваться сами вирусные частицы или их геномы. Ингибирование этой передачи, например, с помощью антител к NS1 — ключевому в этом механизме белку вируса, — может помочь в борьбе с инфекцией, однако это требует дальнейших исследований.
Заражение вирусом Зика во время беременности может вызывать аномалии развития плода, в том числе летальные. До сих пор не было ясно, как вирусу удается пересечь плаценту, которая питает развивающийся плод и образует надежный защитный барьер. Авторы статьи в Nature Communications выяснили, какой механизм позволяет вирусу Зика укрыться от реакции иммунной системы.
Туннельные нанотрубки — это межклеточные каналы, состоящие из F-актина или микротрубочек и напрямую соединяющиеся с плазматической мембраной клеток. Их длина достигает 700 мкм. Межклеточная передача вируса через туннельные нанотрубки, вероятно, защищает его от иммунного ответа, в том числе нейтрализующих антител и/или иммунных клеток. К такой передаче способны вирус гриппа, ВИЧ или SARS-CoV-2, а теперь этот механизм выявили еще и у вируса Зика.
Чтобы отследить инфекцию в клеточной культуре, ученые сконструировали кДНК вируса Зика, содержащую ген флуоресцентного белка mCherry. Полученным на ее основе вирусом заражали экстравиллезные трофобласты (линия HTR-8), цитотрофобласты (JEG-3) и клетки первичной культуры трофобласта человека. Конфокальная микроскопия показала, что вирус Зика индуцировал в зараженных клетках формирование длинных и тонких актиновых филаментов, которые соединяли соседние клетки. Ученые определили эти структуры как туннельные нанотрубки.
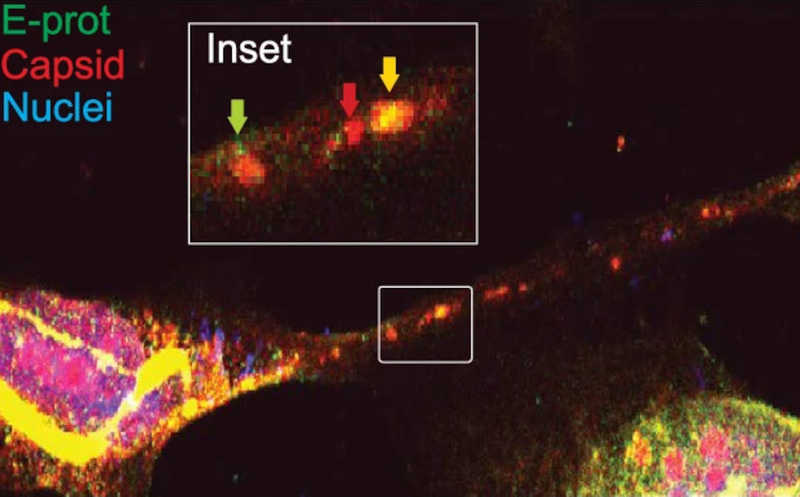
Для проверки функциональной роли нанотрубок в данной модели исследователи окрашивали культуры зараженных клеток антителами к структурным белкам оболочки и капсида вируса. В нанотрубках наблюдались участки колокализации этих двух белков.
Оказалось, что обнаруженные структуры могут служить для распространения вируса, а именно его геномной РНК. Полученные in vitro данные указывают на то, что двуцепочечная РНК вируса Зика способна транспортироваться по туннельным нанотрубках от одной клетки к другой.
Затем ученые установили, какой именно белок вируса Зика индуцирует образование туннельных натотрубок. Они клонировали три структурных белка вируса (белок капсида C, прекурсорный мембранный белок prM и белок оболочки E) и семь неструктурных белков (NS1, NS2A, NS2B-NS3, NS4A, NS4B и NS5). К каждому из белков пришили C-концевую метку mCherry, после чего клетки в культуре трансфицировали каждой из конструкций по отдельности. Так выяснилось, что формирование туннельных нанотрубок в клетке индуцирует белок NS1. При этом белок должен быть ассоциирован с мембраной — растворимая форма NS1 не вызывала образование нанотрубок клеткой.
Дальнейший анализ показал, что NS1 колокализуется с актиновыми и тубулиновыми филаментами в составе туннельных нанотрубок, а также взаимодействует с митохондриальными белками. Благодаря взаимодействию он колокализуется с митохондриями и стимулирует их поглощение из соседних клеток.
Уже известно, что вирусы могут использовать измененную динамику митохондрий в зараженных клетках, чтобы улучшить условия для своей репликации. Авторы статьи установили, что ингибирование митохондриального дыхания или блокирование подвижности митохондрий в клетках трофобласта подавляли репликацию вируса.
Транспорт вирионов, вирусной РНК и белков через туннельные нанотрубки ослабляет интерфероновый ответ на инфекцию. Ранее было показано, что инфицирование трофобласта вирусом Зика ограничено в том числе благодаря быстрой индукции противовирусного ответа, в частности, интерферонов типа III (IFN-λ). В культуре клеток действительно начиналась продукция IFN-β и IFN-λ в ответ на заражение, однако уровни IFN-λ были в 30-60 раз больше, если клетку инфицировал мутантный вирус, лишенный функционального NS1 и не способный стимулировать образование нанотрубок.
Работа раскрывает ранее неизвестный механизм межклеточной передачи, который позволяет вирусу Зика избежать иммунного ответа. Авторы подчеркивают, что необходимы дальнейшие исследования для определения молекулярного механизма, с помощью которого белок NS1 индуцирует туннельных нанотрубок. Понимание этого механизма позволит разработать метод его подавления, а следовательно, борьбы с распространением вируса.
Источник
Michita, R.T., et al. Zika virus NS1 drives tunneling nanotube formation for mitochondrial transfer and stealth transmission in trophoblasts. // Nat Commun 16, 1803 (2025). DOI: 10.1038/s41467-025-56927-2


 Меню
Меню





 Все темы
Все темы




 0
0










