Вирусные инфекции могут способствовать развитию нейродегенеративных заболеваний
Ученые кокультивировали клетки-доноры, которые экспрессировали агрегаты неправильно свернутых белков и вирусные гликопротеины, с реципиентными клетками, которые синтезировали нормальные белки и рецепторы. В результате в клетках-реципиентах образовывалось больше белковых агрегатов, чем в отсутствие вирусных гликопротеинов. Таким образом, вирусы могут «открывать дорогу» нейродегенеративным заболеваниям.
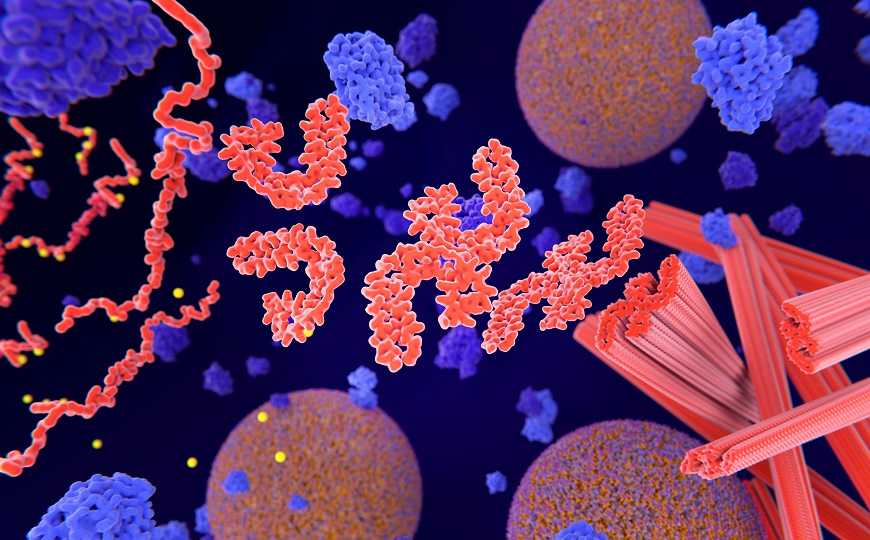
Нейродегенеративные заболевания, в том числе прионные болезни и болезнь Альцгеймера, характеризуются образованием агрегатов неправильного свернутых белков. Такие белки могут возникать в клетках спорадически и затем распространяться по всему мозгу. Механизм передачи белков между клетками и индукции образования новых агрегатов до сих пор не до конца изучены. Считается, что эти процессы могут обеспечиваться тремя путями: высвобождением несвязанных агрегатов, прямой передачей от клетки к клетке через цитонемы и передачей с помощью внеклеточных везикул. Считается, что последний путь слабо выражен в ряде нейродегенеративных заболеваний.
Исследователи из Немецкого центра нейродегенеративных заболеваний совместно с бельгийскими учеными предположили, что низкая активность передачи белков через внеклеточные везикулы обусловлена отсутствием специфических лигандов, которые необходимы для слияния везикулы с клеткой-реципиентом. Тем не менее, как предполагают ученые, процесс становится легче, если на везикуле присутствуют вирусные гликопротеины.
Для проверки данной гипотезы авторы культивировали клетки нейробластомы мыши или HEK, в которых синтезировалась растворимая форма белка Sup35 NM и рецептор LDL. Эти клетки участвовали в качестве реципиентов. Вместе с этими клетками культивировали клетки HEK или N2a, которые содержали агрегаты неправильно свернутых белков, а также VSV-G (гликопротеин вируса везикулярного стоматита). Это были клетки-доноры.
Вирусный гликопротеин VSV-G значительно увеличивал число клеток-реципиентов с агрегатами белков. Рецептор LDL также играл ключевую роль. Авторы показали, что VSV-G помогает формированию неправильно собранных белков благодаря образованию внеклеточных везикул. Экспрессия S-белка SARS-CoV-2 вместо VSV-G не влияла на секрецию внеклеточных везикул, но увеличила образование агрегатов в реципиентных клетках. Таким образом, ученые обнаружили, что наличие вирусных гликопротеинов в клетке способствует передаче неправильно свернутых белков другим клеткам.
«Вирусные лиганды опосредовали эффективный транспорт агрегатов в клетки-реципиенты, где они индуцировали образование новых агрегатов. Лиганды действуют как ключи, который открывают вход в реципиентные клетки и, таким образом, протаскивают опасный труз», — сказала Ина Ворберг, руководитель исследовательской группы и профессор в Боннском университете. Требуются дальнейшие исследования на более сложных моделях, но, тем не менее, данное открытие пролило свет на связь между нейродегенеративными и вирусными заболеваниями.
Источники
Shu Liu, et al. Highly efficient intercellular spreading of protein misfolding mediated by viral ligand-receptor interactions // Nature Communications, 12, published online 19 October, 2021, DOI: 10.1038/s41467-021-25855-2
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0