МД-2025. Поиск мишеней противоопухолевой терапии: от биоинформатики к «мокрой биологии»
Как сейчас идет поиск новых мишеней для противоопухолевой терапии и чем в этом помогает искусственный интеллект? Зачем нужно знать точную структуру рецепторных тирозинкиназ, чтобы на них воздействовать? Какие методы помогают найти таргетируемые химерные гены и биомаркеры ответа глиобластомы на темозоломид? Эти и другие вопросы обсуждались на секции о поиске терапевтических мишеней, прошедшей в рамках конференции «Молекулярная диагностика 2025».
Credit:
123rf.com
Секцию открыл Михаил Федянин, д.м.н., ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» МЗ РФ с окладом «Новые мишени для противоопухолевой терапии в 2025 году (на примере рака молочной железы)».
Ингибиторы циклинзависимых киназ используются в случае развития резистентности, например, к ингибиторам ароматазы. Воздействие на эти мишени дает хороший эффект. В мире уже зарегистрировано пять таких молекул. Причем у молекулы Trilaciclib есть регистрация по профилактике миелотоксичности на фоне химиотерапии во время лечения мелкоклеточного рака легкого. Однако все остальные препараты, которые используют в лечении рака молочной железы, кроме противоопухолевого действия обладают токсичностью (гематологической, гастроинтестинальной). При этом адъювантные препараты предлагается принимать после операции в течение двух-трех лет. Половина женщин не заканчивает курс. Встает вопрос, как минимизировать такую токсичность.
Оказалось, что побочное действие ингибитора CDK4/6 развивается именно за счет ингибирования CDK6, а противоопухолевый эффект реализуется за счет ингибированной CDK4. Пришли к выводу, что нужно сделать селективные CDK4-ингибиторы.
С прошлого года стали появляться первые фазы клинических исследований, которые изучают селективные CDK4-ингибиторы: 90% контроля болезни, 60% объективных ответов, при этом значимо снижается токсичность. После дальнейших испытаний эти препараты могут войти в клиническую практику.
Другой вариант подавления размножения клеток люминального рака — это применение гормонотерапии. Есть ингибиторы ароматазы, есть селективные модуляторы стероидных рецепторов, деградеры и другие препараты. Есть антагонисты и агонисты данных рецепторов.
Появился довольно большой пул молекул, связанных с созданием пероральных селективных деградеров рецепторов эстрогена.
Когда такие молекулы изучали на больных, рефракторных к CDK4/6-ингибиторам, то есть во второй-третьей линии лечения люминальных HER2- форм рака молочной железы, то оказалось, что на общей выборке они не дают никакого эффекта. Есть улучшение общей выживаемости, но стилистически не значимое.
Но исследователи пошли дальше, они отобрали больных женщин, у которых в плазме крови в циркулирующей ДНК были мутации в рецепторах эстрогена, которые зачастую и определяют резистентность к ингибиторам ароматазы или тамоксифену. И в этой когорте препарат значимо улучшили показатели общей выживаемости при прогрессировании на CDK4/6-ингибиторах. Исследование все равно было негативным. Однако эти находки привели к тому, что эту подгруппу стали изучать и в других работах.
Так, камизестрант в качестве препарата первой линии улучшил медиану выживаемости этой подгруппы пациенток на 7 месяцев. Результаты представлены на ASCO. Препарат подан на регистрацию.
Другой интересный подход — протеолитическое разрушение рецепторов. Создается химерная молекула, которая распознает необходимый рецептор, но при этом происходит убиквитин-зависимый протеолиз.
В этом году такой препарат испытали в фазе 3 КИ именно на люминальном раке молочной железы — препарат Vapdegestrant. Пациенты, которые прогрессировали на фоне CDK4/6-ингибиторов, получали этот препарат, его сравнили с фулвестрантом.
Предполагалось, что этот подход разрушения рецепторов будет очень эффективным, особенно учитывая, что он вроде как не зависит от мутации, которая возникает в этом рецепторе.
Да, препарат эффективен. Во второй и третьей линии видно улучшение медианы выживаемости без прогрессирования, но всего на 3 месяца. Этого достаточно, чтобы зарегистрировать препарат, но реальная его эффективность по сравнению с фулвестрантом — это рост медианы с 3 месяцев до 5,5 месяцев.
Еще один вариант воздействия на определенные сигнальные пути при раке молочной железы — это воздействие на те сигнальные пути, которые определяют резистентность, в частности, за счет появления мутации в генах, кодирующих белки сигнального пути PI3K. Это могут быть мутации в PIK3CA, PTEN, других, частота их встречаемости — порядка 20%.
Реальная эффективность таких препаратов при раке молочной железы будет довольно низкой. Начали появляться новые AKT-ингибиторы, с ними есть некое улучшение, но результаты довольно скромные, выживаемость без прогрессирования максимум 3–4 месяца.
На HER2+ рак молочной железы обычно действуют ни одним препаратом, а комбинацией.
Но сейчас идет эра конъюгатов. Антитело связано с химиотерапевтическим препаратом. И рецептор используется как мишень для того, чтобы «подтянуть» этот препарат к опухолевой клетке. Чем интересен рак молочной железы, при этом заболевании у конъюгатов новых поколений есть свойство «убийства свидетелей». То есть рядом расположенные клетки, имеющие низкую экспрессию HER2, тоже погибают за счет того, что в опухоли создается высокая концентрация данного препарата.
Почти все новые препараты используют ингибиторы полимеризации микрортрубочек и ингибиторы топоизомеразы 1.
Zanidatamab — биспецифичный препарат. То есть используется одна и та же мишень, но при этом антитело взаимодействует с двумя афинными точками в этом рецепторе. Данный препарат хорошо себя зарекомендовал, по крайней мере по результатам 1/2 фазы когортного исследования, в которое включались различные нозологии. Проверяли его эффективность не только в качестве монотерапии, но в комбинации с различными химиотерапевтическими агентами. Частота объективных ответов при раке молочной железы составила по крайней мере 43%, медиана выживаемости без прогрессирования в этом исследовании состояла 16 месяцев.
Можно ли этот биспецифик связать с химиопрепаратом и получить сложный конъюгат? Будет ли он работать? Такие препараты появились, например, молекула TQB2102. Авторы сообщают о довольно хороших результатах, объективный ответ порядка 66%, контроль болезни 100%, но медиана выживаемости без прогрессирования составила 16 месяцев. Молекула показала хорошую эффективность в популяции РМЖ HER2-low. И вот скорее в этой нише препарат займет свое положение.
Кроме того, этот препарат показывает хорошие результаты и вне рака молочной железы, у больных колоректальным раком. Здесь частота ответов 44% с медианой выживаемостью без прогрессирования 12 месяцев.
Другая интересная мишень — это HER3, препарат Iza-bren. Это биспецифик плюс конъюгат плюс химиотерапия в одной молекуле. Он воздействует на EGFR и HER3 одновременно. И авторы показали довольно высокую частоту объективных ответов, под 50%.
В случает прогрессирования тройного негативного рака молочной железы на первой линии опции ограничены. Медиана общей выживаемости у таких женщин катастрофически низкая. Поэтому здесь нужна любая новая терапевтическая опция.
Сацитузумаб говитекан — конъюгат, химиопрепарат вместе с антителом к Trop-2, дал улучшение выживаемости без прогрессирования с 1,7 до 4 месяцев, и его зарегистрировали за рубежом, но пока не в нашей стране. Скорее всего, здесь можно выделить группу больных, более чувствительных к данному препарату (с высоким уровнем экспрессии Trop-2).
Еще среди потенциальных мишеней при тройном негативном раке молочной железы находится CDH6. Этот рецептор, оказалось, представлен на платинрезистентном раке яичников, и в фазе 2 получили объективный ответ порядка 60%. У порядка 15% больных клетки тройного негативного РМЖ могут экспрессировать CDH6.
Интересные рецепторы для тройного негативного рака молочной железы — B7-H3 и B7-H4 — использовали как мишени для того, чтобы притянуть конъюгат. Две молекулы уже прошли первую фазу КИ, объективный ответ порядка 30–40%. Нужно дождаться дополнительных исследований.
Еще одну молекулу — SEZ6 — использовали в качестве мишени для конъюгата. Авторы показали, что в клиническом исследовании фазы 1, куда включались пациенты с различными нозологиями, при раке анального канала была достигнута частота объективного ответа 60%, назофарингеального — 50%, слюнных желез — 33%, при резистентном немелкоклеточном раке легкого — 40%. Есть данные, что этот рецептор экспрессируется и на тройном негативном раке молочной железы.
С докладом «Поиск новых мишеней для иммунотерапии аденокарциономы яичника на основе иммунопептидома опухолевых клеток» выступил Георгий Арапиди, к.б.н., ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России,
Аденокарционома яичника входит в топ-5 причин смертности среди онкологических заболеваний, ее сложно диагностировать на ранних стадиях, и в 85% случаев ее диагностируют уже на поздних стадиях, когда выживаемость крайне низкая. Активно используют хирургическое удаление опухоли, химиотерапию, различные препараты на основе платины, таксаны. Но часто происходит рецидив с химиорезистентностью. Необходимы новые методы терапии этой патологии, отсюда и интерес к иммунотерапии.
Для аденокарциономы яичника считается перспективным поиск вакцин для активации иммунной системы посредством опухолеспецифических неоантигенов. Неоантигены — антигены, которые есть у опухоли, но нет у нормальных тканей. Они появляются вследствие накопления мутаций опухолевыми клетками. Иммунопептидом — это совокупность пептидов, презентированных на поверхности клеток. Исследование иммунопептидома группа докладчика считает перспективным подходом для поиска новых решений для иммунотерапии аденокарциономы яичника. Они разработали подход, который связан с выделением и очисткой лигандов главных комплексов гистосовместимости первого класса. Подход включает в себя выделение мембранных фракций опухолевых клеток с использованием специальных детергентов, в том числе из твердых тканей, иммунопреципитацию, аффинную хроматографию с использованием специфических антител, спектрометрию и биоинформатический анализ идентифицированных пептидов.
При проработке этого протокола учли довольно много этапов, важных для результирующего иммунопептидома. Это вопросы объема биообразца, концентрации, соотношения антител, образца и смолы, вопросы, связанные с детергентом, используемым для лизиса, различные очистки и протоколы масс-спектрометрического анализа.
Анализировали иммунопептидом линии Jurkat. Было идентифицировано более тысячи пептидов в составе клеток. Характерные длины для комплекса гистосовместимости первого класса — это 8–14 аминокислотных остатков. Большая часть — это девятичленные пептиды, и для них тоже выведен характерный паттерн аминокислотных последовательностей.
Проанализировали 25 пациенток с аденокарциномой яичника, материал получен до химиотерапии, и 15 пациенток, для которых химиотерапия предшествовала операции; также была когорта пациентов с доброкачественными кистами в качестве дополнительного контроля. Коллекцию охарактеризовали и проанализировали биологический материал.
У одной из пациенток до химиотерапии идентифицировали 2002 пептида, из них длиной 8–14 аминокислотных остатков — 1728. Они достаточно аффинные, многие из них высокоаффинные. Увидели определенные аминокислоты в тех сайтах, которые важны для связывания иммунопептидов с комплексом гистосовместимости.
У другой пациентки после химиотерапии выявили 1772 пептида, из них длиной 8–14 аминокислотных остатков — 1227. Опять характерный пик на 9-ти аминокислотных остатках и характерные аминокислоты в соответствующих положениях.
Среди идентифицированных пептидов иммунопептидома аденокарциномы яичника обнаружено 97 пептидов-фрагментов опухольспецифичных белков, которые являются перспективными мишенями для иммунотерапии.
Доклад «Структурно-функциональные детерминанты в мембранных доменах рецепторных тирозинкиназ как мишени для терапии онкологических заболеваний» прочитал Эдуард Бочаров, д.ф.-м.н., ГНЦ ИБХ РАН, г. Москва; МФТИ.
Пока мы не поймем, как рецепторы работают, их физические механизмы проведения сигнала через мембрану, мы не сможем на них влиять полностью.
Битопные белки в организме отвечают за передачу биохимического сигнала на большие или малые «расстояния». Это рецепторные протеинкиназы, апоптозные белки, предшественники бета-амилоида, иммунные рецепторы, интегрины, мембранно-связанные ферменты. Мутация в них приводят к различным заболеваниям, в том числе и онкологическим.
Изначально считалось, что тирозинкиназа димеризуется после связывания лиганда. Но в последние годы обнаружили, что чаще всего эти рецепторы уже димеризованы и находятся в «спящем» состоянии. Это состояние очень интересно с точки зрения биофизики и структурной биологии, потому что киназные домены вроде как димеризованы, но при этом сигнал не проходит через мембрану.
Из-за крупного размера тирозинкиназ до сих пор нет их полноразмерной структуры, есть только данные по отдельным доменам. Исходя из структуры и механизма, можно понять, как на эти рецепторы можно влиять не только при заболеваниях, но и в норме.
Группа докладчика получила за несколько лет множество структур димеров тирозинкиназ в разнообразных мицеллах и бицеллах, например, в нанодисках. И структурная информация дала некоторую информацию об их работе. Так, переключение из активной формации в неактивную и обратно может происходить путем изменения, например, липидного состава мембраны.
Также важно не только состояние трансмембранной части. Для передачи сигнала через мембрану важно, как цитоплазматические участки взаимодействуют с теми же самыми мембранами. Это определяет «спящее» или активное состояние. Цитоплазматические участки имеют несколько формаций, в зависимости от лиганда, который связывается с эктодоменом, их формация будет разная. Было показано, например, что для активации EGFR/HER1 нужна молекула холестерина.
В результате сформулировали липидно-опосредованный механизм передачи сигнала через мембрану битопными белками. Этот механизм говорит о том, что важно не только белок-белковое взаимодействие, но и белок-липидное взаимодействие. Механизм позволяет объяснить трансмембранные мутации, которые описаны у человека и приводят к разным заболеваниям, в том числе онкологическим. Также можно предложить новые методы терапии дисфункции тирозинкиназ, такие как «пептиды-перехватчики» или малые молекулы.
Продолжила секцию с докладом «Новые моноклональные антитела к натрий-зависимому фосфатному транспортеру NaPi2b: перспективы создания диагностических тест-систем и противоопухолевых препаратов на их основе» Рамзия Киямова, д.б.н., профессор, Институт фундаментальной медицины и биологии, Казанский (Приволжский) федеральный университет.
NaPi2b — это трансмембранный белок, который экспрессируется в ряде органов и тканей, а также при раке яичников, легкого и целом ряде других новообразований. Гуманизированные антитела, направленные против эпитопа МХ35 в большом внеклеточном домене (ВКД) транспортера NaPi2b, известны. Причем они накапливаются именно в опухолевых очагах, а NaPi2b экспрессируется и в нормальных тканях. Группа докладчицы предложила вариант, почему так происходит.
Исследователи определили топологию ВКД и показали, что в этом домене есть две дисульфидные связи. Потом выявили четыре цистеина, которые располагаются приблизительно на одинаковом расстоянии друг от другу и принимают участие в формировании этих связей, и несколько сайтов N-гликозилирования. Предположительно, в нормальных тканях эпитоп МХ35 экранируется углеводными остатками и становится недоступным для антител. Но углеводы не только экранируют эпитоп, но и играют роль в поддержании конформации для его экспонирования.
Исследователи предположили, что в условиях опухолевого микроокружения, для которого характерен оксидативный стресс и изменение паттерна гликозилирования, этот эпитоп становится более доступным для моноклональных антител, в том числе для терапевтических. Эффект накопления терапевтических антител был уже описан на тот момент. Тогда это опухольспецифический эпитоп, перспективный для терапии антителами.
N-концевой домен в условиях микроокружения опухоли может менять свою локализацию с внутриклеточной на внеклеточную, что делает его еще одним потенциальным опухольспецифическим доменом.
Таким образом, в составе молекулы есть два потенциальных опухольспецифических домена, что открывает большие перспективы для получения биспецифических молекул, которые будут более эффективны.
Идут работы по созданию отечественных моноклональных антител против NaPi2b. Также разрабатывается тест-система для определения уровень экспрессии и для определения мутации в гене транспортера, а малоинвазивная тест-система для определения содержания транспортера в крови пациента (в перспективе).
Доклад «Современные инструменты искусственного интеллекта для поиска и валидации мишеней новых препаратов» прочитал Юрий Вяткин, Институт искусственного интеллекта МГУ им. М.В. Ломоносова; ООО «NOVEL», директор по инновациям.
Существует довольно много вычислительных подходов к поиску мишеней. Это структурные методы (докинг, обратный докинг, виртуальный скрининг, оценка druggability белков), omics + сети, Drug-target interaction (DTI)-модели и репозиционирование, а также текст- и патент-майнинг. И ко всем этим способам поиска терапевтических мишеней можно применить искусственный интеллект.
Прежде всего искусственный интеллект занимается интеграцией данных. Анализ можно проводить с помощью построения графов. Классические методы (например, структурные) получили дополнительное развитие с помощью ИИ. И есть более общая область, которая пытается построить некоторые фундаментальные модели, то, что называется Foundation-модели, которые в теории должны выучивать всю информацию о том, как работает клетка в норме и в патологии. Это пока еще находится в довольно зачаточном состоянии.
В Институте построили и успешно используют модель искусственного интеллекта, которая выучивает то, как на какие-то клеточные линии действуют какие-то вещества. Все это работает на уровне единичных клеток. Обученная модель предсказывает экспрессию генов вне заданного распределения. В основе этой модели лежит идея переноса стиля (стайл-трансфер подход).
В результате анализа открытой метаинформации по экспериментам scRNA-seq (GEO, SRA, DISCO) были отобраны 50 датасетов, пригодных для обучения нейросети.
На вход модели подают экспрессию (ее можно снять обычными средствами секвенирования РНК единичных клеток) и некоторое действующее вещество (в виде химического описания структуры молекулы). Прежде всего здесь речь идет о низкомолекулярных соединениях. И получают новую экспрессию генов, которая так или иначе отражает поведение клетки в условиях действия препарата.
Некоторые применения модели: поиск сопутствующей терапии ингибиторами KRAS при немелкоклеточном раке легкого (метод предсказал увеличение доли гибели раковых клеток, если агент ARS 1620 используется в комбинации с ингибитором трансляции белков INK128); подтверждение эффективности терапии блокадой ИЛ при перикардите; исследование влияния препаратов на различные подтипы рака молочной железы.
Если сократить количество потенциальных мишеней, скажем, до десятков, то можно использовать структурные методы. В частности, группой докладчика был исследован новый препарат, который представляет собой низкомолекулярное соединение, созданное в лаборатории Новосибирского института органической химии. Это препарат против болезни Паркинсона, который уже дошел до фазы 2b клинических испытаний. И попытались посмотреть, на что воздействует этот препарат, путем молекулярного докинга. Для этого использовали еще один подход из мира искусственного интеллекта, который называется диффузионные модели. При этом сначала добавляют шум, а потом из шума восстанавливают некоторые конечные изображения, используя информацию о том, как низкомолекулярные соединения садятся на некоторые белки.
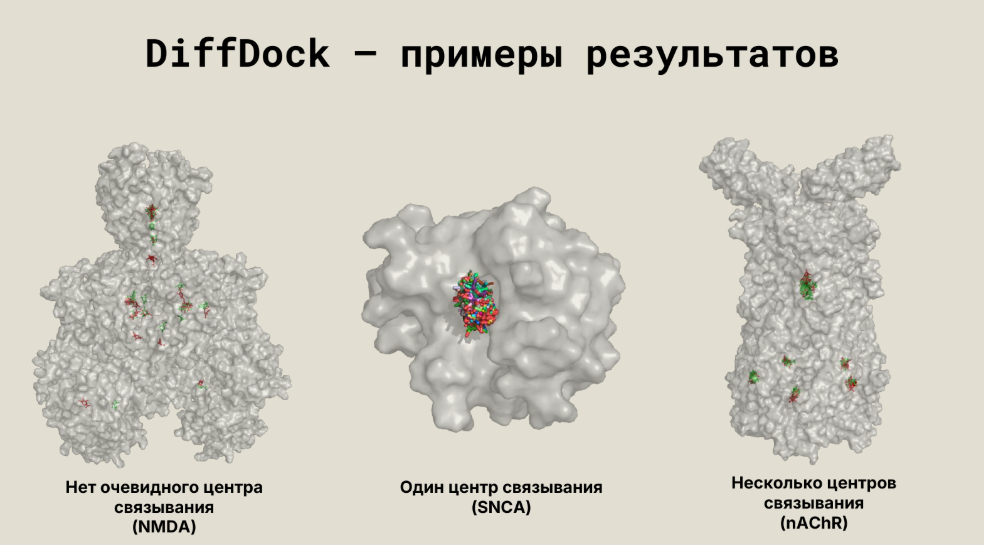
Все это было проделано с тем веществом, которое используется для терапии болезни Паркинсона, и было показано, что есть активные формы этого вещества, а есть неактивные формы. В конце составляется список белков, с которыми связывается активная форма и с которой не связывается неактивная форма этого вещества. На основании этого делается положение, какой рецептор является таргетной мишенью этого низкомолекулярного соединения.
Вопрос об интерпретации патогенности вариантов тоже можно решать с помощью искусственного интеллекта, этим занимается платформа GENOMENAL.
С докладом «Модели машинного обучения для анализа выживаемости: оценка эффектов омиксных биомаркеров и их взаимодействий в онкологии» выступила Маргарита Запевалина, Сколковский институт науки и технологий, Центр молекулярной и клеточной биологии.
Докладчица рассказала об интеграции омиксных и клинических данных, в частности, данных о выживаемости.
Анализ выживаемости — это некий пул методов, когда переменные — это наступление какого-то состояния (например, смерти) и время до этого события, и нас интересует вероятность выживания для пациента.
Когда интегрируется большое количество клинических параметров, а также омиксных биомаркеров, можно посмотреть их влияние на анализ выживаемости, то есть не просто на предсказание наличия и отсутствия заболевания, но и на своего рода агрессивность течения этого заболевания.
Активно развивается deep learning в survival-анализе. Одна из ключевых и активно используемых моделей — это DeepSURV.
Для того, чтобы снизить размерность, самые трендовые методы — это DL-survival методы основаны на аутоэнкодерах и вариационных аутоэнкодерах.
Чтобы проводить анализ выживаемости на данных, где омиксы и мультиомиксы и при этом малое количество пациентов, можно использовать AutoSurv (2024 год). Также можно использовать SurvTRACE для оценки важности фичей а их взаимодействия.
Галина Захарова, к.х.н., ФГАОУ ВО Первый МГМУ имени И.М. Сеченова Минздрава России (Сеченовский Университет), выступила с докладом «Асимметрия покрытия генов при РНК-секвенировании — новый высокоэффективный способ детекции таргетируемых химерных генов в широком спектре опухолей».
Тема работы сконцентрирована на тех тирозинкиназах, которые имеют клиническое значение, и на фьюженах, где тирозинкиназа располагается на 3'-конце. В последнее время во всех рекомендациях идет смещение фокуса на методы РНК-секвенирования, подразумевается использование таргетных панелей. Они дороже, чем остальные методы, но зато позволяют проанализировать сразу много генов и менее субъективны в анализе.
В чем состоит суть методики определения фьюженов по покрытию? Мы имеем некую тирозинкиназу. В случае, если это интактный ген, то при секвенировании или при любом другом методе оценки экспрессии экзонов мы видим либо низкую экспрессию (что нормально, если ген фетальный), либо нормальную экспрессию гена дикого типа. В случае, когда происходит разрыв гена и слияние его с партнером 5', то мы видим, что сохранившийся кусок имеет какую-то экспрессию, а потерянный — не имеет.
Здесь есть свои ограничения. Тот ген, с которым слился тирозинкиназный ген, должен сам по себе экспрессироваться, то есть его промотор должен быть активным.
Оценка дисбаланса в экспрессии начала и конца гена применяется в различных существующих решениях. Но группа докладчицы впервые применила ее для РНК-секвенирования. У них уже была большая когорта собственных пациентов, для которых было проведено полнотранскриптомное секвенирование (больше 1300 пациентов). Для отобранных пациентов, чтобы проверить находки, провели таргетное секвенирование двумя панелями.
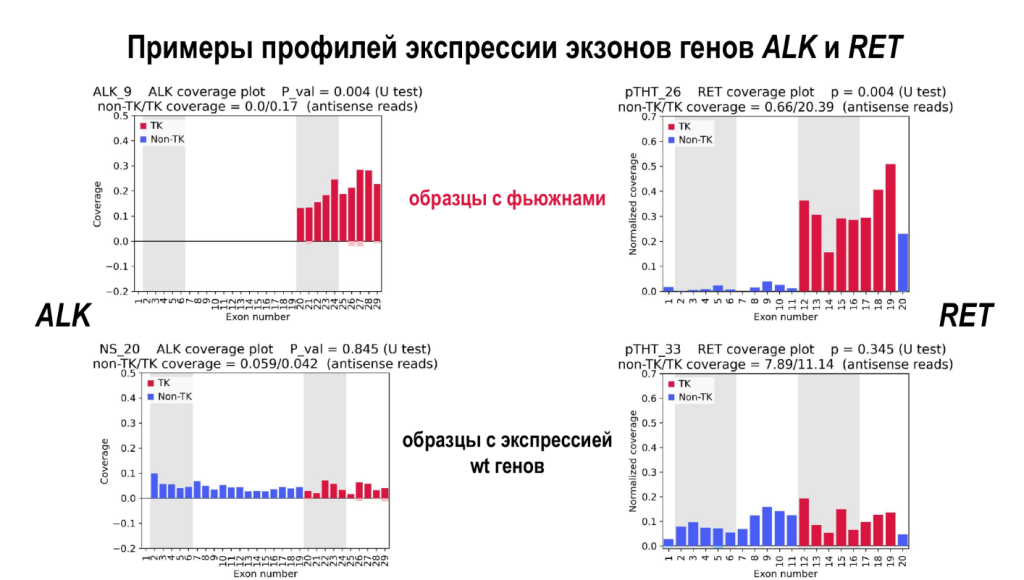
Сходятся ли предсказания о наличии фьюженов с информацией, которая есть в выписках у пациентов? На фьюжены редко проводится анализ, потому что события редкие и всех тестировать затруднительно. Подобрали образцы немелкоклеточного рака легкого, для которых статус ALK был известен. Если смотреть на p-value, то есть статистическую значимость дисбаланса покрытия, то она совпадала с клиническим статусом чуть больше чем в половине случаев. Авторы ожидали большую сходимость, они стали разбираться.
Например, для одного образца оказалось, что ИГХ был сделан некачественно. Решили, что нужен третий метод, чтобы проверить образцы на наличие фьюжена. Этим методом стали панели.
В основном оценка покрытия совпадала с данными, полученными с помощью панелей, кроме одного образца. Клинические данные совпадали гораздо реже.
Дальнейший анализ показал, что одного p-value недостаточно, нужно еще определить, насколько сильно должны отличаться 3' и 5'-концы. Для этого взяли валидационную когорту — 79 образцов различных типов опухолей. Определили пороги, которые позволили отделить образцы, где подтвердились фьюжены, от остальных образцов. Перепроверили на второй когорте, пороги сработали.
В процессе нашли три новых фьюжена, один из которых раньше был описан только для рака легкого, тут его нашли в раке щитовидной железы, и два ранее не были описаны вовсе.
Таким образом, дисбаланс покрытия может быть использован для того, чтобы в данных РНК-секвенирования выявлять фьюжены.
Публикации:
A New Approach of Detecting ALK Fusion Oncogenes by RNA Sequencing Exon Coverage Analysis
Accurate RET Fusion Detection in Solid Tumors Using RNA Sequencing Coverage Imbalance Analysis
Доклад «Уровень экспрессии MGMT и пути репарации ДНК — источники новых молекулярных мишеней и более значимые биомаркеры ответа глиобластомы на темозоломид, чем метилирование» прочитал Александр Модестов, ФГАОУ ВО Первый МГМУ имени И.М. Сеченова Минздрава России (Сеченовский Университет).
Глиобластомы представляет собой агрессивную опухоль центральной нервной системы, основные методы лечения — это хирургическое вмешательство, лучевая терапия и химиотерапия темозоломидом. Темозоломид способен метилировать пуриновые основания ДНК, в частности гуанин с образованием метилгуанина. Однако данный процесс может быть обратим специальным ферментом — MGMT (O6-метилгуанин-ДНК-метилтрансферазой). Далее возможно два сценария: когда промотор данного гена метилирован, его экспрессия понижена, это приводит к чувствительности к темозоломиду и гибели опухолевых клеток; если промотор не метилирован, происходит развитие резистентности к темозоломиду и прогрессирование опухоли. Поэтому на данный момент статус метилирования MGMT представляет собой основной биомаркер, определяющий чувствительность опухоли к темозоломиду.
Однако существуют более эффективные биомаркеры, такие как экспрессия генов, уровень активации пути репарации ДНК, а также сконструированные на основе интерактомной модели человека пути чувствительности к темозоломиду. Основная цель состояла в поиске таких биомаркеров.
Для оценки предполагаемых биомаркеров был проведен анализ выживаемости пациентов с глиобластомой при терапии темозоломидом с помощью расчета отношения рисков. Молекулярные профили экспрессии генов с информацией по общей выживаемости и выживаемости без прогрессирования были получены из баз данных TCGA и CGGA. Также представлены экспериментальные когорты пациентов с глиобластомой.
Пациенты были разделены на группы до и после 2005 года, поскольку именно в этом году терапия темозоломидом стала клиническим стандартом.
Сначала было проверено метилирование MGMT в качестве биомаркера ответа на терапию. Для экспериментальных данных это был эффективный биомаркер с отношением рисков 0,34. Для когорты пациентов TCGA после 2005 года статистически значимые результаты были получены для общей выживаемости, но не для выживаемости без прогрессирования. Примечательно, что для пациентов TCGA до 2005 года вообще отсутствовала какая-либо статистическая значимость связи метилирования с выживаемостью. Аналогичные результаты были получены для когорты CGGA. Поэтому необходимо использовать новые маркеры на основе экспрессии генов и активации пути репарации ДНК.
Экспрессия самого гена MGMT оказалась более эффективным биомаркером, чем статус метилирования. Видна статистическая значимость для всех анализируемых наборов данных. Аналогичным образом посмотрели на все гены-участники репаративных путей для всех трех наборов данных. Было обнаружено 6 генов с благоприятной выживаемостью, также к ним относится путь контроля клеточного цикла в точке G2. К биомаркерам с неблагоприятной выживаемостью относились другие гены путей репарации ДНК.
Далее построили из этих 12 генов-биомаркеров чувствительности к темозоломиду на основе интеракторной модели. Чтобы получился связный молекулярный путь, потому что он не представлял собой единую сеть, дополнительно к 12 генам добавили 5 генов. Рассчитали уровень активации данного пути для экспериментальной когорты и для когорты TCGA. Биомаркеры с благоприятной выживаемостью были активаторами пути, с неблагоприятной выживаемостью — ингибиторами. На основе этого просчитали уровни активации и провели анализ выживаемости, который продемонстрировал отношения рисков от 0,18 до 0,44.
Положительные биомаркеры в основном были вовлечены в процессы остановки клеточного цикла, а также в процессы репарации с помощью негомологичного соединения концов и гомологичной рекомбинации. Отрицательные в основном вовлечены в процесс эксцизионной репарации.
Информация о докладчиках
Михаил Юрьевич Федянин, д.м.н., ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» МЗ РФ, г. Москва
Георгий Павлович Арапиди, к.б.н., ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России, г. Москва
Александр Яневски, PhD, Европейский университет в Санкт-Петербурге, г. Санкт-Петербург
Эдуард Валерьевич Бочаров, д.ф.-м.н., ГНЦ ИБХ РАН, г. Москва; МФТИ, г. Долгопрудный
Рамзия Галлямовна Киямова, д.б.н., профессор Институт фундаментальной медицины и биологии, Казанский (Приволжский) федеральный университет, г. Казань
Юрий Викторович Вяткин, Институт искусственного интеллекта МГУ им. М.В. Ломоносова; ООО «NOVEL» директор по инновациям, г. Москва
Маргарита Кирилловна Запевалина, Сколковский институт науки и технологий, Центр молекулярной и клеточной биологии, г. Москва
Галина Сергеевна Захарова, к.х.н., ФГАОУ ВО Первый МГМУ имени И.М. Сеченова Минздрава России (Сеченовский Университет), г. Москва
Александр Андреевич Модестов, ФГАОУ ВО Первый МГМУ имени И.М. Сеченова Минздрава России (Сеченовский Университет), г. Москва


 Меню
Меню





 Все темы
Все темы



 0
0










