МД-2025: Молекулярно-генетические исследования в неврологии. Часть 2
Существуют ли на самом деле биомаркеры болезни Паркинсона и как на этот вопрос помогут ответить пары близнецов, лишь у одного из которых развилось это заболевание? Что такое когнитивная хрупкость и как ее учитывать в контексте старения? Как связаны конкуренция и старение клеток при нейродегенеративных заболеваниях? Эти и многие другие вопросы обсудили на второй части секции «Молекулярно-генетические исследования в неврологии» конференции «Молекулярная диагностика 2025».

Маргарита Максимовна Руденок, к.б.н., НБИКС-ПТ НИЦ «Курчатовский институт», г. Москва.
Фото:
Андрей Константинов
Анеля Алиева, к.б.н., НИЦ «Курчатовский институт», поделилась результатами экспрессионного профилирования близнецов, дискордантных по болезни Паркинсона.
БП — многофакторное заболевание, которое не всегда объясняется генетическими факторами. Часть случаев обусловлены изменением экспрессии генов.
Подход экспрессионного профилирования монозиготных близнецов позволяет нивелировать влияние генетических и направленно оценить изменения экспрессии. На базе Курчатовского института провели исследование трех пар монозиготных близнецов. От всех участников были получены образцы периферической крови, а также фибробласты кожи, из которых получили культуры ИПСК и затем нейрональных предшественников.
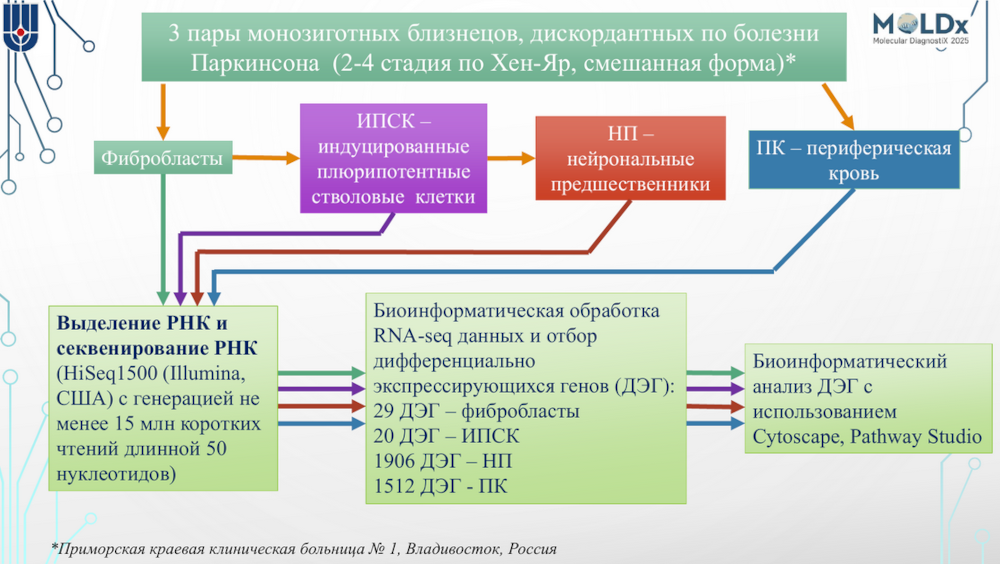
На этих клетках провели секвенирование РНК и анализ дифференциальной экспрессии, причем среди дифференциально экспрессирующихся генов в дальнейшее рассмотрение включали только те, у которых характер изменений совпадал для всех трех пар близнецов.
При полнотранскриптомном анализе фибробластов было выявлено 29 дифференциально экспрессирующихся генов. Анализ обогащения выявил, что эти гены связаны с семью процессами, которые кластеризуются в две группы.
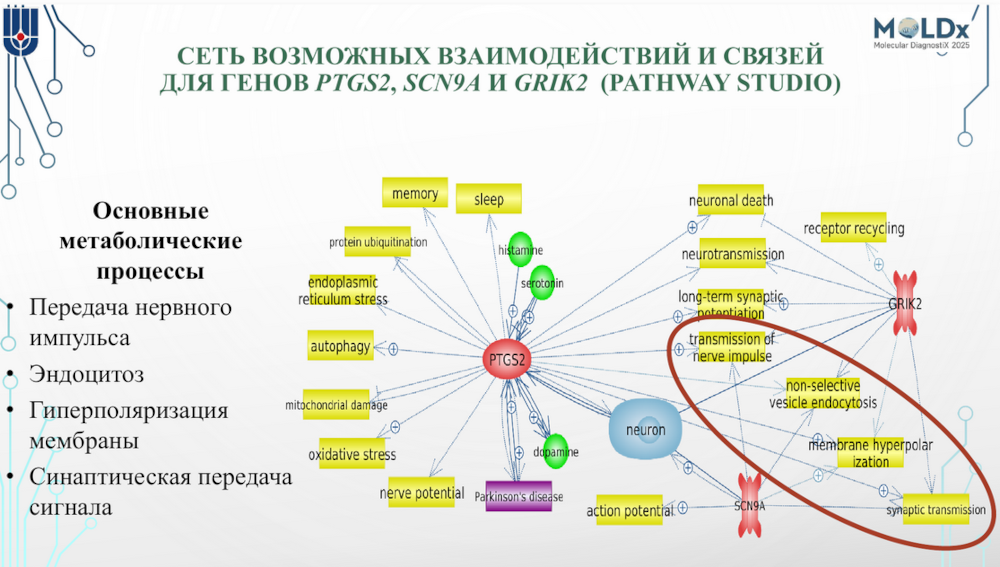
В первую группу вошли гены, участвующие в дифференцировке жировых клеток, синаптической глутаматергической передачей и генерацией потенциала действия. Гены SCN9A, PTGS2 и GRIK2, которые входят в этот кластер, перспективны для дальнейшего более подробного изучения. Функции всех трех связаны с нейронами и передачей нервного импульса.
В ИПСК было выявлено всего 20 дифференциально экспрессирующихся генов. Анализ обогащения на такой выборке не был статистически значимым, однако исследователи все же оценили их функцию в данном контексте. Наиболее интересными докладчица назвала четыре гена: BLNK, DDX43, P2RY12 и NRF2F2. Анализ литературных данных уже указал на связь P2RY12 с болезнью Паркинсона.
В нейрональных предшественниках, дифференцированных из ИПСК, было выявлено уже 1906 дифференциально экспрессирующихся генов. Анализ функционального обогащения позволил выделить 12 процессов, которые кластеризовались в три независимые группы. Наиболее интересные из них, по словам докладчицы, были связаны с нейрогенезом и анатомией нейронов. Скрининг по функции отдельных генов указал на их связь с биогенезом митохондрий, окислением жирных кислот, окислительным стрессом и аутофагией.
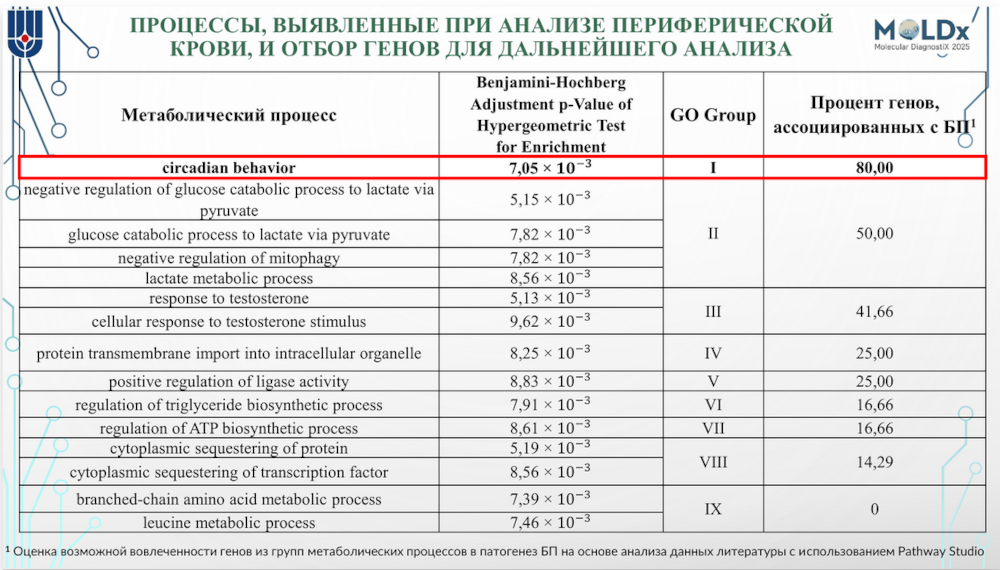
При транскриптомном анализе мононуклеаров периферической крови было обнаружено 1512 дифференциально экспрессирующихся генов. Аналогичная характеризация процессов выявила девять кластеров метаболических процессов, причем особенно выделялись среди них циркадные ритмы и циркадное поведение. Это согласуется с клиническими данными о том, что одним из ранних симптомов БП является нарушение сна.
По совокупности полученных данных исследователи отобрали набор генов, участвующих в нейродегенерации при болезни Паркинсона и компенсанторных процессах, причем в ряде случаев усиленная компенсация может способствовать дальнейшему развитию патологии. Общими и наиболее значимыми процессами оказались окислительный стресс, апоптоз, биогенез митохондрий, аутофагия и циркадные ритмы. Для части из них уже подтверждена роль в патогенезе БП, другие — например, окисление жирных кислот — сравнительно новые в данном контексте. В целом полученные результаты указывают на потенциальные биомаркеры определенных стадий БП.
«В предыдущих выступлениях говорилось, что биомаркеров болезни Паркинсона не существует, но мы верим, что все же сможем их отобрать» — подытоживает докладчица.
О практической части предыдущего исследования, а именно об анализе мРНК для ранней диагностики БП, рассказала Маргарита Руденок, к.б.н., НИЦ «Курчатовский институт».
Патогенез болезни Паркинсона характеризуется длительным бессимптомным периодом — от инициации патологических процессов в мозге до проявления клинических симптомов, по которым ставится диагноз, может пройти до 20 лет. И эти симптомы проявляются при гибели 50-60% дофаминергических нейронов черной субстании и снижении уровня дофамина в стриатуме на 70-80%. В силу того, что изучать эндогенные процессы в мозге живых пациентов практически невозможно, а кровь является одним из наиболее доступным материалом для исследования данного заболевания. Кроме того, клетки крови могут отражать некоторые процессы, характерные для дофаминовых нейронов.
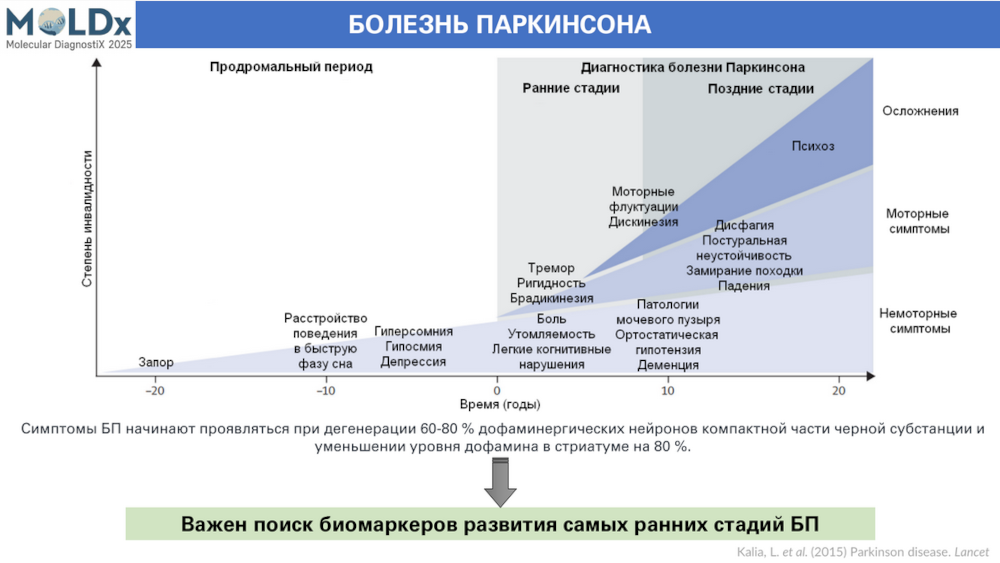
Иными словами, клетки крови можно в определенной степени считать моделью болезни Паркинсона. Поэтому целью работы стал поиск мРНК-биомаркеров БП в периферической крови.
В исследование включили пациентов с болезнью Паркинсона, которые получали и не получали терапию, а также группу сравнения, в которую входили неврологически здоровые добровольцы и пациенты с другими неврологическими заболеваниями.
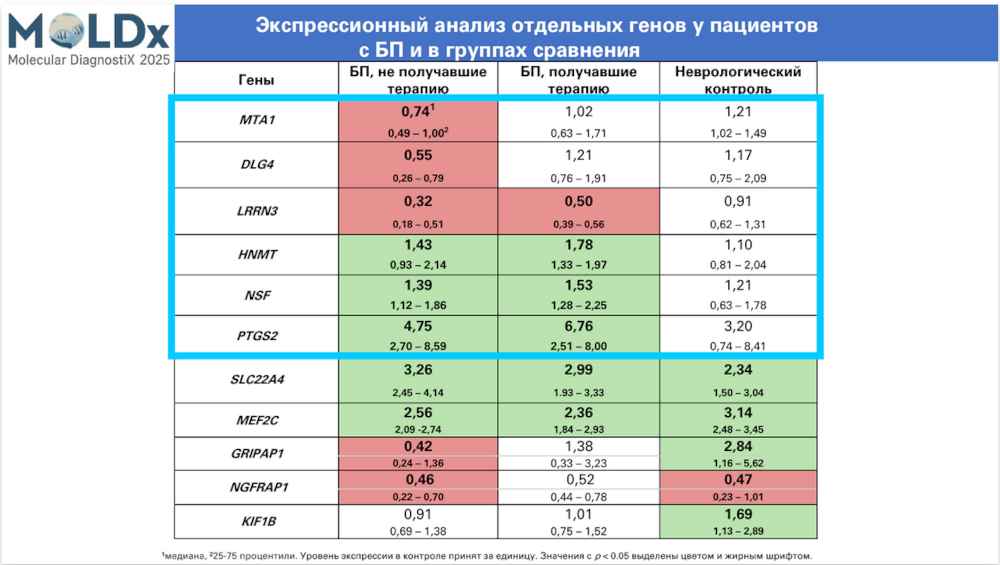
Всех пациентов оценили по шкале Хен—Яра, согласно оценке, они все находились на ранних стадиях БП. После этого из образцов крови были получены коллекции тотальной мРНК и кДНК, которую затем анализировали при помощи ПЦР в реальном времени. Из 11 изученных генов в шести были выявлены статистически значимые изменения, характерные для пациентов с БП.
Первый из них — MTA1 — снижался у пациентов с БП, не получавших терапию. Он участвует в экспрессии циркадных генов и служит коактиватором транскрипции тирозингидроксилазы (фермента синтеза дофамина).
Аналогичным образом менялась экспрессия гена DLG4. Кодируемый им белок регулирует распределение глутаматных рецепторов в синаптической мембране и контролирует синаптическую передачу сигнала. Согласно литературным данным, его недостаток может приводить к перераспределению этого белка из синаптической мембаны в везикулы и нарушать распределение синаптических белков в целом. Это, в свою очередь, приводит к нарушению баланса нейромедиаторов — одной из отличительных особенностей БП.
Следующий ген — LRRN3 — снижал экспрессию у всех пациентов с БП независимо от лечения. Белок, кодируемый им, участвует в развитии и регенерации нейронов. Уже опубликованы данные о том, что он вовлечен в патогенез БП, и экспрессия его гена снижается на ранних стадиях БП как в крови, так и в черной субстанции, и продолжает снижаться по мере прогрессирования болезни.
Экспрессия гена HNMT, который кодирует гистамин-N-метилтрансферазу, возрастала у всех пациентов. Это указывает на то, что на ранних стадиях БП могут активироваться компенсаторные механизмы, направленные на усиление метаболизма гистамина.
Ген NSF кодирует белок, вовлеченный в клеточный транспорт — он отвечает за слияние внутриклеточных синаптических мембран и за сборку/разборку комплекса SNARE. Увеличение экспрессии этого гена у всех пациентов с БП также свидетельствует о развитии компенсаторных механизмов, связанных с синаптическим транспортом.
Наиболее сильно в крови пациентов возрастал уровень экспрессии гена PTGS2. Данный ген кодирует фермент циклооксигеназу 2 (ЦОГ2), которая синтезирует простагландин H2 — предшественник целого ряда воспалительных факторов и факторов, участвующих в аутофагии и апоптозе. Его активация может свидетельствовать о воспалительных процессах при болезни Паркинсона.
Выступление Юлии Комлевой (д.м.н., доцент, Институт мозга ФГБНУ «Российский центр неврологии и нейронаук») было посвящено когнитивной хрупкости и роли нейровоспаления.
Все мы знаем, что будущее стареет. Продолжительность жизни человека стала выше, на сегодняшний день в России около 15% населения — это люди в возрасте 65 лет и старше, и эта доля будет только расти. При этом гериатрическим, то есть стареющим обществом считается то, в котором доля населения старше 65 лет составляет 7% или больше.
Увеличение продолжительности жизни сопровождается ростом частоты возраст-ассоциированных патологий, в том числе когнитивных и неврологических нарушений.
Все мы также понимаем, что люди стареют по-разному — кто-то в 80 лет способен бежать марафон, а кто-то нуждается в серьезной внешней поддержке. И хронологический возраст, хотя и является важным предиктором общего состояния здоровья и выживаемости, не отражает их в полной мере. У каждого человека будет своя траектория старения.
В англоязычной литературе выделяют три категории — нормальное, ускоренное и успешное старение. И существующая вариабельность темпов старения привела к появлению концепции хрупкости (frailty).
В 1979 году концепцию ввели для того, чтобы описать неодинаковые риски смерти у людей одного хронологического возраста. В современной медицине этот термин используется для обозначения вероятности различных неблагоприятных исходов, таких как развитие деменции, инвалидизация, госпитализации. Таким образом, хрупкость — это показатель мультисистемной дисрегуляции, которая приводит к снижению физиологического резерва и повышает уязвимость организма к внешним неблагоприятным факторам.
Хрупкость рассматривают как многокомпонентный и динамический процесс. Существует несколько подходов к определению хрупкости. Один из них — это модель Линды Фрид, которая трактует хрупкость как ухудшение физического функционирования и опирается на пять критериев. Индекс хрупкости по шкале Роквуда использует нефиксированный набор клинических состояний, а сама хрупкость интерпретируется как накопление различных дефицитов (в некоторых исследованиях до 71). И, наконец, активно развивающаяся сейчас модель — это хрупкость как совокупность доменов (социального, психологического и физического).
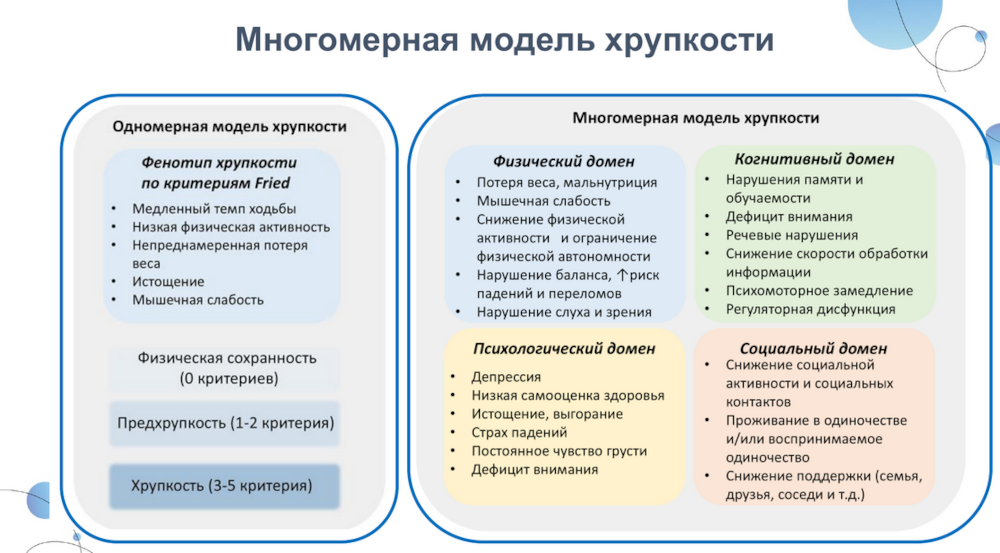
Физическая хрупкость, о которой речь шла изначально, связана с когнитивным статусом у пожилых людей. Эта корреляция между физическим состоянием и когнитивным статусом, подтвержденная в ряде исследований, легла в основу концепции когнитивной хрупкости. Этот термин введен в 2013 году и с тех пор использовался более чем в 500 статей, в основном обзорах и метаанализах. Однако до сих пор существуют разногласия в его точном определении. Международная академия питания и старения совместно с Международной ассоциацией геронтологии и гериатрии определила когнитивную хрупкость как одновременное наличие физической хрупкости и умеренных когнитивных нарушений при отсутствии деменции и других предшествующих заболеваний головного мозга.
Факторы риска когнитивной хрупкости — это в первую очередь возраст, а также женский пол, сопутствующие болезни (например, сердечно-сосудистые заболевания или диабет), а также полифармация, то есть одновременный прием пяти и более препаратов. С точки зрения патофизиологии в этом контексте выделяют воспаление (в том числе нейровоспаление как обособленный фактор), окислительный стресс, накопление сенесцентных клеток, саркопению, не поддающуюся коррекции анемию.
Существуют также клинические маркеры хрупкости и старения, среди ключевых — отклонения уровня кортизола, гипоальбуминемия, провоспалительные факторы (C-реактивный белок), отрицательный белковый обмен, низкий уровень трансферрина и резистентная анемия. Также в качестве клинических маркеров старения могут быть использованы некоторые антиоксидантные метаболиты крови.
Считается, что определение пациентов с субъективными и ранними нарушениями перспективно именно на стадии когнитивной хрупкости — это дает потенциальное терапевтическое окно для вмешательства, а более поздние вмешательства, к сожалению, в настоящее время недостаточно эффективны.
На пять основных доменов — питание, сердечно-сосудистые риски, физическая и социальная активность, ментальная стимуляция — опирается достаточно известное исследование FINGER, проведенное в Финляндии с участием более тысячи человек. Оно посвящено оценке того, как можно предотвратить снижение когнитивных способностей с возрастом.
Еще одно исследование о влиянии внешних факторов подтверждает, что когнитивная хрупкость ассоциирована с депрессией, плохим питанием, низкой физической активностью и отсутствием социальных связей.
Что позитивного дают нам эти данные? Влияние тренировок на метаболизм и когнитивные функции говорит о том, что физическая активность может быть полезным модифицирующим фактором для риска когнитивной хрупкости. Это одно из вмешательств, которые входят в превентивную стратегию, используемую сейчас в Канаде. Аббревиатура AVOID Frailty перечисляет пять модификаторов — это физическая активность (A), необходимость вакцинироваться в пожилом возрасте (V), оптимизация количества принимаемых лекарственных препаратов (O), социальные взаимодействия (I) и здоровая диета (D).
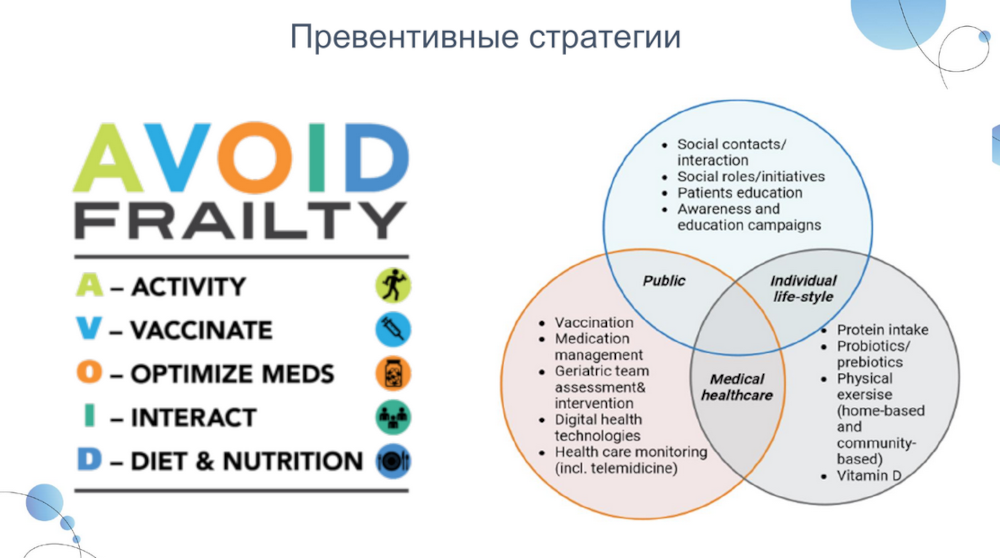
Таким образом, когнитивная хрупкость — это не просто научный термин, а реальное клиническое состояние со своими рисками и возможностями. И важно понимать, что при раннем выявлении мы можем не только замедлить, но и частично обратить ее развитие.
Заключительный доклад в секции прочитала Елизавета Перепелица (Институт мозга «Российский центр неврологии и нейронаук»). Она рассказала о применении органоидов в качестве персонифицированных клеточных 3D-моделей нейродегенерации.
Индуцированные плюрипотентные стволовые клетки (ИПСК) — одна из ценных пациент-специфичных моделей для изучения заболеваний головного мозга, в частности, потому, что это самый доступный материал для прижизненного анализа. Однако двухмерная клеточная культура устроена намного проще, чем ткань мозга, и такие модели не позволяют адекватно проанализировать ряд важных межклеточных взаимодействий. Для решения этой проблемы применяют органоиды, полученные из ИПСК — они точнее отражают структуру реального мозга.
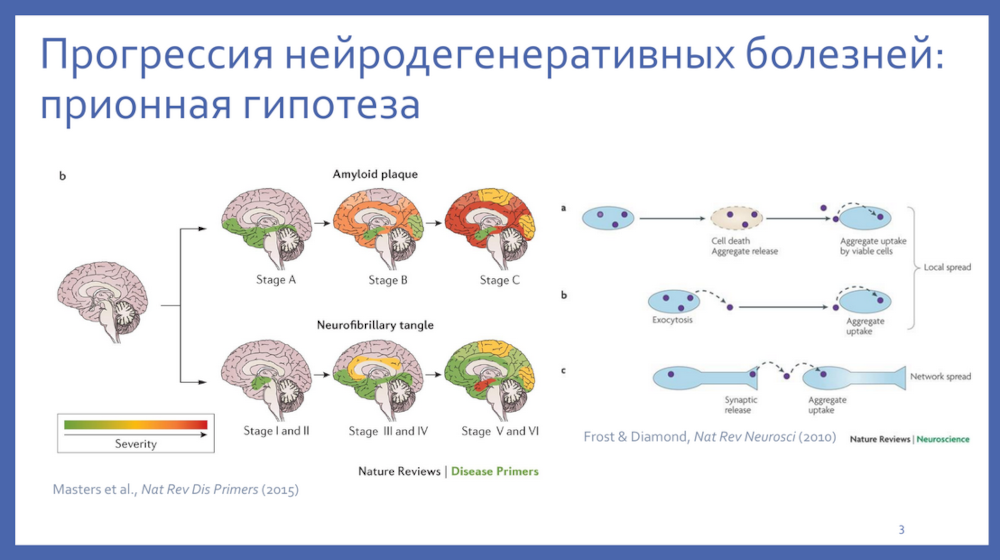
Почему межклеточные взаимодействия важны в контексте неврологических заболеваний, в том числе нейродегенеративных? Примером может служить болезнь Альцгеймера — уже показано, что при этом заболевании нейродегенерация начинается в определенной области мозга и постепенно распространяется, захватывая все большие площади. Механизм связывают в частности с прионной гипотезой, согласно которой аномальные формы белка распространяются между клетками и участвуют в патогенезе. Это подтверждает, что межклеточные взаимодействия вносят вклад в прогрессирование болезни.
Другой важный компонент нейродегенерации — это физиологическое старение, которое затрагивает отдельные клетки и нарушает их функции. В частности, клеточное старение может приводить к нарушениям аутофагии и к митохондриальной дисфункции.
Электронная микроскопия дофаминергических нейронов, полученных из ИПСК пациентов с болезнью Паркинсона, подтверждает накопление липидных капель и аутофагосом. Микрофотографии, полученные в Институте мозга РЦНН, демонстрируют, что в таких нейронах накапливаются дистрофичные митохондрии, в которых отсутствуют кристы, а также образуются гигантские митохондрии.
Однако клеточное старение не только затрагивает отдельные клетки, оно также проявляется на более высоком уровне организации. При клеточном старении клетки могут портить друг другу жизнь. Это связано прежде всего с особым секреторным фенотипом — SASP — который связан с выработкой провоспалительных факторов. При таком фенотипе клетки действуют друг на друга, распространяя старение по всему органу. В контексте мозга это приводит к нейровоспалению.
Это наблюдение привело Елизавету и ее коллег к тому, чтобы рассмотреть связь нейродегенерации с еще одним механизмом — клеточной конкуренцией. Согласно концепции клеточной конкуренции, существует механизм, который разделяет клетки на «победителей» и «проигравших» — они отличаются друг от друга степенью приспособленности (fitness) и, как следствие, конкурентоспособности.
Клетки могут сравнивать друг друга по этому параметру, причем критерии могут быть различны (например, здоровье митохондрий). На молекулярном уровне клетки-«победители» и «проигравшие» способны друг друга различать, маркером для этого различения служит мембранный белок-маркер Flower. Он может быть представлен на мембране в различных изоформах, и определенная комбинация этих изоформ будет сообщать о состоянии клетки.
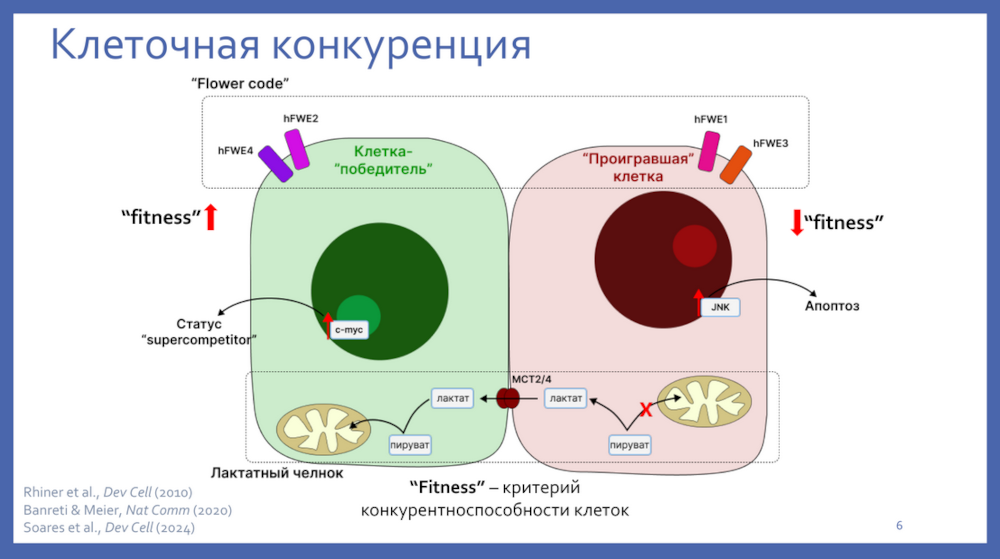
Кроме того, «проигравшие» клетки могут поддерживать метаболизм клеток-«победителей», отдавая им свой лактат. Этот механизм известен как лактатный челнок, его активация приводит к тому, что из проигравшей клетки высосут все соки и она погибнет.
Данный процесс изучался в рамках онкологии, где было также показано, что клетки «победители» способны активно снижать конкурентоспособность окружающих клеток.
Проведенный зарубежным коллективом анализ клеточной конкуренции в оптических нейронах дрозофилы показал, что этот механизм также может участвовать в нейродегенерации. Полученные данные указали на то, что клетки, которые начинают экспрессировать аберрантные белки, устраняются из ткани.
На основании этого была выдвинута гипотеза о том, что клеточная конкуренция — это механизм контроля качества ткани, в том числе ткани головного мозга. На ранних стадиях патологии устранение отдельных нейронов может быть защитным механизмом, который направлен на то, чтобы предотвратить распространение нейродегенерации.
Соответственно, возникает идея интегрировать механизмы клеточной конкуренции и клеточного старения как драйверов нейродегенерации, однако сейчас еще слишком много вопросов остаются не до конца изученными. Возможно, клеточная конкуренция в какой-то момент перестает справляться с устранением дефектных клеток, так как их становится слишком много. Также можно предполагать, что при нейродегенерациях стареющие клетки слишком активно снижают конкурентоспособность окружающих клеток, и оказываются победителями, несмотря на собственные дефекты.
Это подчеркивает важность разработки моделей, которые позволят оценивать клеточные взаимодействия и будут адекватно отражать архитектуру ткани. При этом такие модели должны основываться на человеческих клетках.
В Институте мозга РЦНН проводятся исследования на таких моделях — органоидах, полученных из ИПСК, и много внимания уделяется ангиогенезу и конкуренции клеток в сосудах. Уже известно, что при ангиогенезе эндотелиальные клетки приобретают ту или иную специализацию — формируются концевые клетки, которые направляют рост сосуда в определенную зону, и стеблевые клетки, которые следуют за концевыми и формируют выстилку. Между эндотелиальными клетками постоянно идет динамическая конкуренция за позицию лидера.
Чтобы смоделировать этот процесс, сотрудники РЦНН получили васкулярные агрегаты — эта модель довольно простая, но уже отражает характерный экпрессионный профиль конкурирующих клеток.
Следующим этапом стала более сложная модель — васкулярный органоид из ИПСК. Чтобы их получить, исследователи формировали сфероиды и заключали их в матрикс, состоящий из матригеля и коллагена. В таких структурах наблюдался ангиогенез, индуцированный VEGF и FGF2.
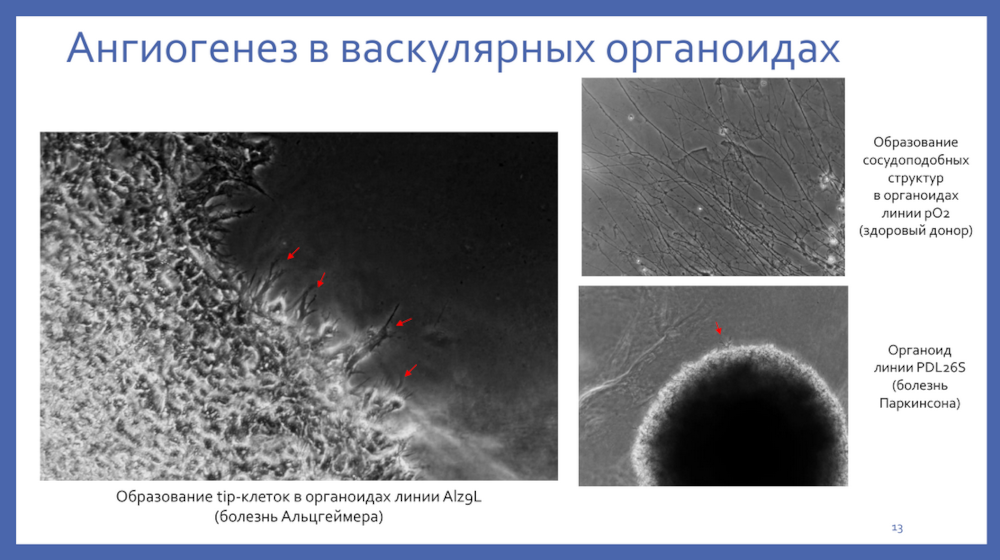
Наконец, были получены органоиды как из ИПСК здоровых доноров, так и из ИПСК пациентов с болезнью Паркинсона или болезнью Альцгеймера. Это значимый этап разработки подходящей модели для изучения нейродегенерации, и уже сейчас речь идет о том, что на основе данного обнаружения можно искать молекулярные маркеры патологий.
МД-2025: Молекулярно-генетические исследования в неврологии. Часть 1
Информация о докладчиках
Алиева Анеля Ханларовна, к.б.н., НБИКС-ПТ НИЦ «Курчатовский институт», г. Москва
Руденок Маргарита Максимовна, к.б.н., НБИКС-ПТ НИЦ «Курчатовский институт», г. Москва
Комлева Юлия Константиновна, д.м.н., доцент, Институт мозга ФГБНУ «Российский центр неврологии и нейронаук», г. Москва
Перепелица Елизавета Сергеевна, Институт мозга ФГБНУ «Российский центр неврологии и нейронаук», г. Москва


 Меню
Меню





 Все темы
Все темы



 0
0