МД-2025: Технологии долголетия
Какие бывают часы старения, как изучают российских долгожителей, где можно пройти научно обоснованный онлайн-тест на когнитивный возраст и чего мы не знаем об аполипопротеине Е, один из аллельных вариантов которого так драматически сокращает жизнь и способствует деменции? Это и многое другое — на секции о долголетии конференции «Молекулярная диагностика 2025».

Секцию открыл чл.-корр. РАН Алексей Москалев (Институт долголетия с клиникой превентивной медицины РНЦХ им. акад. Б.В. Петровского) докладом о биомаркерах старения человека.
Биомаркеры старения — молекулярные, клеточные физиологические и психологические параметры, подверженные изменениям в процессе старения. Воздействие, которое возвращает эти параметры к состоянию, характерному для молодого организма, может рассматриваться как потенциальный геропротектор. Таким образом, биомаркеры старения человека играют важную роль в поиске геропротекторов: их динамика быстро указывает на перспективные воздействия.
Основатель и первый директор Национального института старения США Роберт Батлер предложил в 2004 году следующие критерии: биомаркеры старения должны изменяться с возрастом; эти изменения должны лучше хронологического возраста прогнозировать смертность, а также позволять предсказывать ранние стадии возраст-зависимых заболеваний; наконец, их определение должно быть минимально инвазивным.
Но такие биомаркеры можно назвать поздними, их изменения регистрируются на тех стадиях, когда неблагоприятные процессы уже начали развиваться, отметил Алексей Москалев. Необходимы биомаркеры, указывающие на ранние признаки старения, а не на такие, как старческая хрупкость или повышенный риск смерти. Они должны иметь функцию прогнозирования в разумном диапазоне времени, когда терапевтическое вмешательство еще возможно. Кроме того, они должны иметь низкую аналитическую изменчивость. Например, повышение концентрации С-реактивного белка указывает на воспалительные процессы, которые, в свою очередь, связаны со старением, но также она резко и обратимо возрастает, например, во время простуд.
Согласно классификации, предложенной Алексеем Александровичем, биомаркеры старения делятся на клинические (те же маркеры воспаления, резистентность к глюкозе, эндокринные показатели), функциональные (когнитивные показатели, состояние сердечно-сосудистой системы), а также молекулярные (состояние теломер, уровни определенных белков) и омиксные (профили транскриптома, метилома, протеома, метаболома).
Траектория возрастных изменений человека индивидуальна, различные функциональные системы организма стареют с разной скоростью, кроме того, существуют разные механизмы старения, поэтому стоит использовать панели биомаркеров, отражающих разные его аспекты.
Комплексный биомаркер, основанный на наборе показателей, называется часами возраста или часами старения. Широко известны часы, использующие показатели метилирования ДНК, но существуют часы, включающие и другие типы биомаркеров, в том числе, протеомные.
Классификацией и оценкой биомаркеров старения занимается международный консорциум (обзор концепции в публикации 2023 года). В этом году опубликованы результаты экспертного консенсуса по биомаркерам; среди авторов этой работы был и Алексей Москалев. В ходе трехраундового исследования методом Delphi члены экспертной группы предлагали биомаркеры, затем была сложная система отбора, и в результате сформировался короткий список из 14 биомаркеров, охватывающих ключевые параметры старения, которые могут быть использованы в исследованиях потенциальных геропротекторов. В их число вошли физиологические биомаркеры (например, инсулиноподобный фактор роста 1), функциональные (мышечная масса и сила, скорость ходьбы, тест на равновесие стоя, когнитивное здоровье, артериальное давление и пр.), а также эпигенетические маркеры.

В настоящее время можно выделить уже четыре поколения часов старения. Инструменты первого поколения (часы Стива Хорвата и др.) оценивали хронологический возраст органа или системы, то второе поколение (фенотипические часы PhenoAge, GrimAge) включало как эпигенетические, так и клинические маркеры, связанные со смертностью. Третье поколение — динамические часы — оценивало скорость старения у индивида (DunedinPACE). Наконец, четвертое, пока не нашедшее широкого применения в клинике, указывает на причинно-следственные связи, перспективные для терапии старения (DamAGE, CausAGE). Каузальные часы пока не нашли широкого применения в клинике, но именно этот подход открывает путь к целенаправленному вмешательству.
Исследование российских долгожителей старше 90 лет показало, что эпигенетический возраст у них снижен примерно на 20 лет (в этой работе использовался статус метилирования четырех сайтов CpG). Еще в одной работе автора с коллегами была протестирована нейросетевая модель EchoAge для предсказания биологического возраста сердца по эхокардиографическим параметрам, определяемым при УЗИ. Примечательно, что у детей с прогерией (синдром Хатчинсона-Гилфорда) возраст сердца оказался существенно выше хронологического. В этой работе использовались алгоритмы постобработки решения нейронной сети — объяснимый ИИ (XAI), который позволяет понять, почему решение именно таково. Модель AcidAGE оценивает биологический возраст на основе концентраций органических кислот в моче.
Также докладчик рассказал об исследовании, в котором было показано уменьшение биологического возраста по часам биомаркеров крови (маркеры воспаления, уровень глюкозы, липидный профиль) после прохождения оздоровительных процедур в клинике профилактической медицины. Эффект был значительным, но были и нонреспондеры, и отрицательные респондеры. Очевидно, что не всем подходят одни и те же программы выздоровления.
В заключение Алексей Москалев рассказал о часах старения на основе состояния сосудов: модель предсказывает хронологический возраст по данным о минимальной толщине интимы медиа сонных артерий, степени стеноза, индексе увеличения пульсовой волны и ее скорости.
О нейропротекторных веществах природного происхождения рассказал доктор Витторио Калабрезе (Университет Катании, Университет Мессины, Италия).
Старение неизбежно, но его можно замедлить, и это может быть существенным достижением. По оценкам, сделанным в 2000 году, увеличение на шесть лет средней продолжительности жизни людей, родившихся в 1970–1990 гг, принесло бы доход в $57 триллионов долларов по курсу 1990-х. (Подробнее с расчетами авторов можно ознакомиться здесь.) Десятки триллионов долларов принесла бы победа над раком и ССЗ.
В развитии возраст-ассоциированных нейродегенеративных заболеваний существенную роль играет повышенная продукция свободных радикалов. Сигнальные пути, связанные с клеточным ответом на окислительный стресс, могут стать мишенью для лекарственных препаратов против нейродегенерации.
Докладчик с коллегами предложили понятие витагенов — цитопротективных белков, к которым относит ферменты метаболизма глутатиона, гемоксигеназу 1, шапероны, сиртуины 1 и 2 и др. Витторио Калабрезе также рассказал о предполагаемом механизме активации их экспрессии, опосредованном Nrf2. Этот транскрипционный фактор в норме связан Keap1, но уже при незначительном окислительном стрессе высвобождается и направляется в ядро (или на деградацию в протеасому, что неблагоприятно). По его мнению, этот механизм и является мишенью компонентов пищи, среди которых ищут потенциальные геропротекторы.
В одной и работ докладчика с коллегами ладан — смола Boswellia sacra — при пероральном введении предотвращала апоптоз клеток мозга мыши после травматического повреждения. Этот эффект сопровождался активацией Nrf2.
Важную роль в концепции докладчика играет понятие гормезиса — «нелинейного» действия, характерного для многих препаратов, когда небольшая доза полезна, а большая вредна. («Если вы говорите кому-то «Я тебя люблю», вы вызываете цунами эндорфинов… но если вы повторяете это каждую минуту, вы закончите разводом», — пояснил докладчик.) Возможность терапевтического действия малой дозы и токсичного/ингибирующего действия большой дозы вызывает отторжение из-за ассоциации с псевдонаучными течениями, подобными гомеопатии, тем не менее эту возможность следует иметь в виду при поиске вмешательств, продлевающих жизнь. По мнению автора с коллегами, через сигнальный путь Nrf2-Keap1 могут действовать горметические полифенолы в составе пищи. Они также исследовали действие биодобавок на основе трутовика разноцветного (Coriolus versicolor) на индукцию витагенов.
Докладчик рассказывал и о других полезных компонентах пищевых продуктов, например, оливкового масла или шоколада. Согласно их данным, флаванолы с вяжущим вкусом, такие как процианидины, активируют норадренергическую систему, улучшая память и регулируя вегетативную нервную систему у мышей. Предположительно они активируют функции головного мозга посредством стимуляции ЖКТ.
В заключение Витторио Калабрезе рассказал про работу с органоидами мозга в его лаборатории. Например, на этой модели изучают синергию нейротоксичных генных вариантов и инсектицида хлорпирифоса.
Доклад члена-корреспондента РАН Владимира Митькевича (Институт молекулярной биологии им. В.А. Энгельгардта РАН) назывался «Тетрапептид НАЕЕ как инструмент для анализа и коррекции развития нейродегенеративных заболеваний».
Болезнь Альцгеймера (БА) — разрушительное заболевание, ответственное примерно за 70% случаев когнитивной дисфункции у людей старше 50 лет. Однако до сих пор неизвестно в точности, какие факторы провоцируют развитие БА, почему формируются токсичные олигомеры бета-амилоидов. Внешними факторами могут быть и травмы ЦНС, и перенесенные заболевания.
Агрегация бета-амилоидов начинается с его димеризации через сайт 11EVHH14 в N-концевом металлосвязывающем домене, причем для агрегации нужны ионы Zn2+. На этот процесс могут влиять замены вблизи 11EVHH14 — «английская» мутация (H6R) снижает способность к агрегации, «тайваньская» мутация (D7H), напротив, повышает.
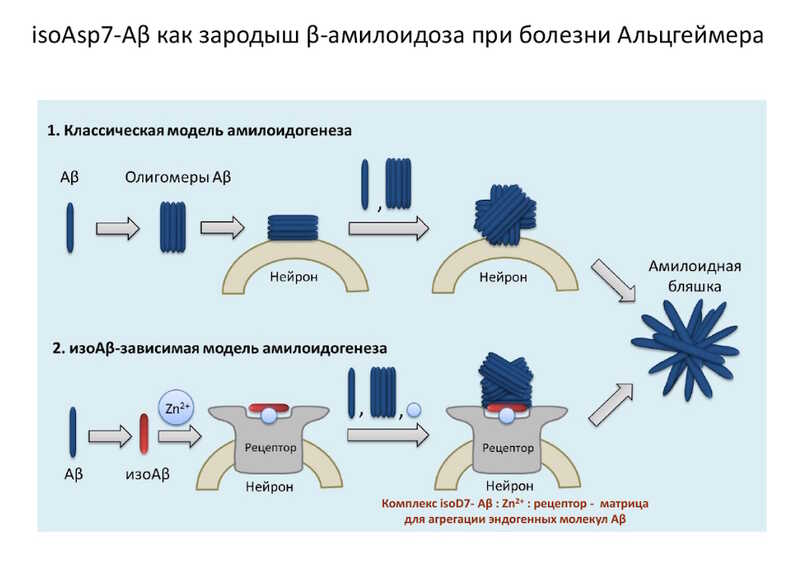
Но существуют также ненаследственные модификации, и это более 90% случаев. Так, посттрансляционная изомеризация остатка аспарагиновой кислоты в положении 7 (iso-Asp7) приводит к спонтанной изомеризации бета-амилоида, усиливая его нейротоксические свойства. Инъекция в желудочки мозга обычного бета-амилоида не наносит вреда животному, тогда как инъекция бета-амилоида с iso-Asp7 вызывает образование амилоидных бляшек в мозгу, влияет на поведение и память. У трансгенных животных, моделирующих БА, с возрастом в мозге накапливается изомеризованная форма бета-амилоида, как и у людей старше 80 лет.
Докладчик с коллегами предложили модель амилоидогенеза, в которой, в отличие от классической, участвует рецептор на мембране нейрона. Комплекс «рецептор — Zn2+ — iso-Asp7 Aβ» становится матрицей для агрегирования молекул бета-амилоида.
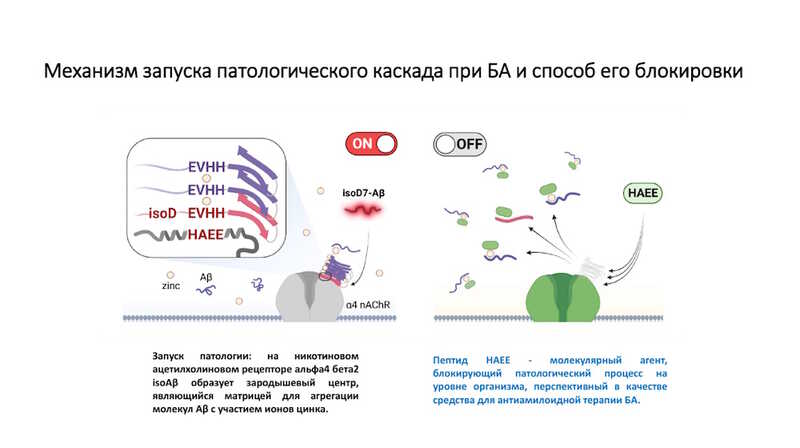
И здесь на сцене появляется тетрапептид НАЕЕ. Известно, что Aβ взаимодействует с ацетилхолиновым рецептором, и ключевую роль в этом взаимодействии играет его мотив EVHH, партнером которого выступает участок НАЕЕ рецептора. Синтетический пептид ацетил-НАЕЕ связывается с участком EVHH и таким образом блокирует агрегацию in vitro. В экспериментах на мышах внутривенное введение НАЕЕ снижало уровень амилоидогенеза и образование бляшек в мозге.
НАЕЕ вмешивается в образование комплекса на рецепторе и подавляет патогенные эффекты ионов цинка и iso-Asp7 Aβ.
Примечательно, что тетрапептид НАЕЕ — нормальный компонент крови человека, что было недавно продемонстрировано в работе под руководством Сергея Козина. Уровень HAEE оказался значительно снижен у пациентов с клиническим диагнозом БА Таким образом, эндогенный HAEE может рассматриваться как потенциальный биомаркер для диагностики этого заболевания.
О секвенировании геномов и других исследованиях долгожителей, которые проводят ЦИП ФМБА России совместно с Российским клиническим НИЦ геронтологии РНИМУ им. Н.И. Пирогова, подробнее рассказала Дарья Каштанова.
Комплексное клиническое обследование долгожителя занимает до 5 часов и включает подробное изучение анамнеза и расширенную гериатрическую оценку. Для биобанкирования отбирают образцы цельной крови и сыворотки с добавлением стабилизатора РНК, а также образцы слюны, стула, буккальные соскобы. Докладчица отдельно отметила слаженную работу медсестер и логистику: работать с пациентами такого возраста нелегко. Затем проводят полногеномное секвенирование ДНК, получают метилом и транскриптом крови, а также метагеномы ротовой полости и кишечника (как по генам 16S РНК, так и методом шотган-секвенирования).
Исследование включает более 5000 долгожителей из 10 субъектов РФ, за которыми ведется продолжительное наблюдение, собрано более 20 000 образцов. Это одна из самых крупных в мире когорт долгожителей с такой широкой географией и подробным анамнезом.
В ходе исследования создан классификатор фенотипов старения — даже долгожители проживают этот процесс по-разному, и не все стареют одинаково благополучно. Выделено пять фенотипов — сохранный. метаболический, мультиморбидный, дементный и низкофункциональный. Система стратификации долгожителей для клинического применения и фундаментальных исследований запатентована.
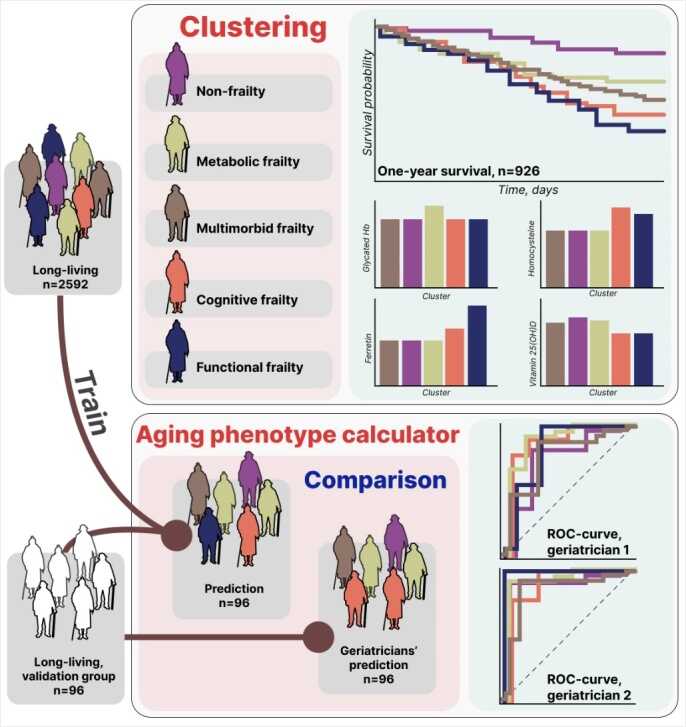 Aging Dis. 2024. DOI:
10.14336/AD.2024.0120
Aging Dis. 2024. DOI:
10.14336/AD.2024.0120
ЦСП ФМБА России — оператор крупнейшей в РФ базы данных результатов полногеномного секвенирования. Это помогло сформировать выборку сравнения (более 20 тысяч человек) для исследования встречаемости вариантов, связанных с возраст-ассоциированными заболеваниями или со здоровым долголетием. В результате был разработан прототип платформы, которая позволяет оценивать генетическую предрасположенность к благополучному или неблагополучному старению, стратифицировать людей по вероятностям достижения долголетия и рискам заболеваний. Проводится также анализ сайтов метилирования и построение эпигенетических часов — инструмент, который позволит оценивать эффективность геропротективных технологий.
Полигенные шкалы тестируются на независимых выборках. Результаты внушают оптимизм, так, ROC AUC для когнитивной сохранности составил 0,69. Недавно вышла статья об эпигенетических маркерах ортостатической гипотензии (падении артериального давления при вставании), от которой страдает примерно треть пожилых людей. Транскриптомные данные указали на ключевые механизмы, связанные с ортостатической гипотензией: метаболическая дисрегуляция, нарушение мышечного тонуса, изменение клеточной пролиферации, воспаление, гуморальная регуляция и нейронная регуляция.
Темой доклада Михаила Иванченко (НИИ биологии старения. Нижегородский государственный университет им. Н.И. Лобачевского) были объяснимые и интерпретируемые решения ИИ для моделей биологического возраста.
Институт биологии старения возник на основе лаборатории системной медицины здорового старения в Нижегородском университете. В 2018 году, Лаборатория получила мегагрант, где ведущим ученым был Клаудио Франчески, почетный профессор Болонского университета, автор концепции «инфламэйджинга» — воспалительного старения. (Клаудио Франчески рассказывал о ней на МД-2023.) В настоящее время институт возглавляет Михаил Иванченко.
Биологический возраст может отличаться от хронологического в ту или другую сторону и находится под влиянием множества факторов, как генетических, так и связанных с окружающей средой и образом жизни. Чтобы учитывать нелинейную сложную взаимосвязь многомерных биомедицинских данных, необходимы инструменты на основе ИИ.
Михаил Иванченко тоже отметил роль биологических часов в исследованиях биологии старения. Многие из существующих часов были созданы для европейских популяций, однако Консорциум по биомаркерам старения недавно запустил проект X-Age, целью которого является разработка комплексной системы оценки старения, адаптированной к китайскому населению.
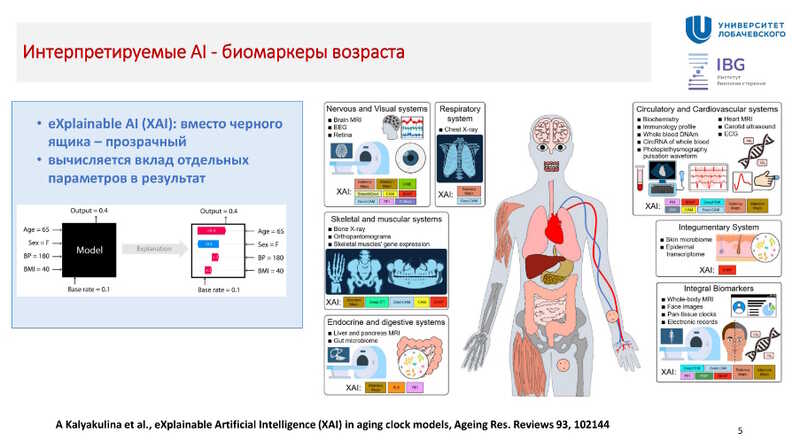
Понятно, что обрабатывать большие данные вручную невозможно. Однако ИИ-модели работают как черный ящик, нам остается верить (или сомневаться), что они работают хорошо. «Сделать черный ящик прозрачным» — объяснять прогнозы сложных моделей, показав вклад отдельных параметров в результат и причины принятия решений, — можно с помощью объясняемого искусственного интеллекта (eXplainable Artificial Intelligence, XAI).
Докладчик рассказал о проекте «Профессиональное долголетие». Индивидуальные рекомендации по замедлению старения могут быть востребованы, поскольку хороший работодатель заинтересован в том, чтобы квалифицированные сотрудники дольше оставались в активном возрасте. В рамках этого проекта ФМБА России осуществляет сбор больших биомедицинских данных, а Центр искусственного интеллекта ННГУ «Лобачевский AI» обеспечивает их обработку, в том числе интеграцию и интерпретацию объяснимых моделей. За год работы пилотного проекта в сотрудничестве с «Росатомом» в нем приняло участие более 1000 человек.
Для оценки биологического возраста участников используются часы различных типов. Часы PhenoAge Морган Левин и соавторов, которые позволяют прогнозировать исходы старения, необходимо скорректировать для российской популяции, прежде чем использовать, отметил докладчик; кез коррекции по показателям PhenoAge все россияне оказывались здоровее, чем на самом деле. Используются также данные общего и биохимического анализа крови.
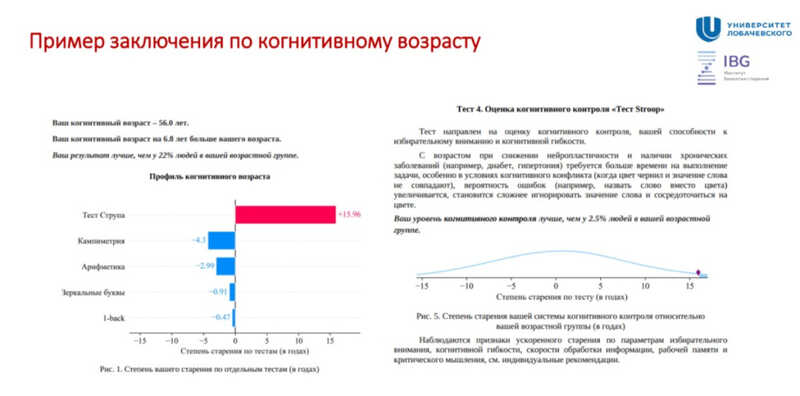
Калькуляторы когнитивного возраста разработали в Нижнем Новгороде. Тесты, отражающие состояние сенсорного и вербального восприятия, рабочую память и способность к принятию решений, можно проходить онлайн. При этом испытуемый не только получит свое значение когнитивного возраста, но и узнает, какая доля людей в его возрастной группе получила худшие результаты, чем у него. Научная статья, суммирующая результаты тестирования на когнитивный возраст, готовится к публикации.
Увеличение возраста по биологическим часам PhenoAge на один год коррелирует с 9%-ным увеличением риска смертности от всех причин, в том числе риска смертности от ССЗ — на10%, от рака — на 7%, от хронических заболеваний нижних дыхательных путей — на 7%. Есть возможность увидеть вклад каждого из показателей в результат.
В конце 2024 года был опубликован обзор почти 300 публикаций, посвященный связям между эпигенетическим ускорением старения с определенными фенотипическими факторами. Ее авторы разработали интерактивную веб-таблицу, которая показывает связь EAA с фенотипами и воздействием факторов окружающей среды.
В заключении по эпигенетическим данным на основе часов DNAmPhenoAge, GrimAge и StocZ представлены сведения об увеличенном или уменьшенном по сравнению с возрастной «нормой» риски ССЗ, метаболических нарушений, нейродегенеративных процессов, дисфункции иммунной системы, а также рекомендации по дальнейшим обследованиям и коррекции образа жизни.
В конце доклада Михаил Иванченко рассказал об иммуновоспалительных часах, разработанных совместно с итальянскими исследователями, где эпигенетические данные связаны с уровнями цитокинов; таким образом, по эпигенетике можно оценивать иммуновоспалительный возраст. «Пока нельзя сказать, что возможно предсказывать самые важные возраст-зависимые заболевания, но мы к этому движемся», — отметил он.
Доклад Ирины Спивак (НИЦ Военно-медицинской академии) назывался «Роль полиморфных вариантов гена BDNF1 в процессах активной адаптации и старения».
Существует предположение, что способность человека адаптироваться к меняющимся и (или) экстремальным условиям во многом связана с его творческим потенциалом, а креативность, как и другие психологические и физиологические особенности, имеет генетическую базу. В свою очередь, устойчивость к стрессу — одна из основ долгожительства.
Докладчица и ее коллеги проверяли на стрессоустойчивость людей, которые едут работать в северные регионы. В исследовании, включающем тестирование на степень креативности и напряженность психологических защитных механизмов, приняли участие мужчины в возрасте 19–35 лет, работающих в Арктике (350 человек) или выполняющие сходную работу в средней полосе РФ (100 человек). У них также проанализировали полиморфизмы в генах, ассоциированных с адаптацией и (или) психотическими состояниями. Изначально это были четыре гена: ангиотензинпревращающего фермента ACE, рецептора серотонина 5HTR2A, нейротрофического фактора BDNF, альфа-актинина-3 ACT-3, потом к ним добавились и другие.
Оказалось, что частоты «слабого» варианта гена BDNF в арктической группе существенно ниже среднеевропейской. Известно, что «слабый» аллель (остаток метионина вместо валина в позиции 166) связан со сниженным уровнем белка и более частыми нейродегенеративными заболеваниями. У носителей повышен уровень тревожности, невротизации.
В данном исследовании уровень невротизации был низким у всех участников (что ожидаемо, поскольку их специально отбирали). Однако у гомозиготных по этому аллелю индивидов, работающих в Арктике, существенно чаще имели место случаи измененного состояния сознания; у работающих в средней полосе такого не отмечалось. Авторы исследования предлагают не направлять в Арктику людей с таким генотипом, тем более, что их не так много. Также у гомозиготных по «слабому» аллелю была достоверно снижена длина теломер.
Еще один интересный факт: генотипирование пациентов гериатрических центров по этому аллелю показало, что «слабый» генотип практически не встречается у людей старше 75 лет — с возрастом он вымывается из популяции.
Что касается креативности — ее максимальный уровень характерен для генотипа Val/Val, промежуточный — для Met/Met, а минимальный — для гетерозигот.
Роль BDNF как нейротрофического фактора мозга в организме исключительно велика. Он участвует в регуляции энергетического гомеостаза, в развитии, поддержании и пластичности центральной и периферической нервной системы, контролирует метаболизм глюкозы, опосредует положительные психологические и физиологические эффекты физической активности и ограничения калорий. Уровень BDNF можно повысить с помощью антидепрессантов или физических упражнений, отметила докладчица.
Завершающий секцию доклад Александры Мамчур (ЦСП ФМБА России) был посвящен аллелям APOE.
Гидрофобные липиды транспортируются к органам и тканям в составе липопротеинов; белки в их составе — аполипопротеины — обеспечивают взаимодействие с клетками. Хорошо известно влияние аллелей APOE и изоформ белка на когнитивную сохранность и продолжительность жизни человека. Аллель Е2 (ε2) является благоприятным, он ассоциирован с большей продолжительностью жизни и лучшей когнитивной сохранность. Аллель Е3 (ε3), наиболее широко распространенный в российской популяции, не влияет на продолжительность жизни и когнитивный статус. Аллель Е4 (ε4) — неблагоприятный, ассоциированный с меньшей продолжительностью жизни и деменцией.
В 2023 году вышла статья докладчицы и ее коллег, подтверждающая ассоциацию аллеля Е4 с тяжелой деменцией у долгожителей. В новых работах, ожидающих публикации, показаны ассоциации этого аллеля с меньшим шансом достижения долголетия и повышенными значениями общего и ЛПНП-холестерина.
Представители разных фенотипов старения, о которых рассказывала Дарья Каштанова, отличаются по частоте аллелей APOE. Ожидаемо, Е4 чаще встречается у менее сохранных фенотипов (дементного и низкофункционального), Е2 — у более сохранных.
Как показал анализ базы данных популяционных частот населения РФ, носительство аллеля Е4 критично для преодоления возрастного порога в 80 лет — в группах более старшего возраста доля носителей начинает сокращаться.
Соблазнительно рассмотреть APOE и аполипопротеин Е как терапевтические мишени — например, использовать для продления жизни удаление аллеля Е4 или его редактирование, удалить эту форму белка с помощью моноклональных антител, изменить его структуру или усилить его липидизацию. Но этот подход затрудняет недостаточное понимание пространственной структуры белка и ее связи с патогенезом.
Можно использовать пептиды — миметики белка Apo; некоторые из них уже проходят доклинические испытания. В таком случае мишенями будут белки, с которыми этот белок взаимодействует, такие как ABCA1, LDLR, LRP1, LRP5/6, TREM2, RAGE, Nrf2.
Патогенез аллеля Е4 связывают со взаимодействием между его доменами, на которое может влиять ключевая замена цистеина аргинином в положении 112. Тем не менее однозначного мнения о пространственной структуре полноразмерного аполипопротеина Е на данный момент нет. На основании имеющихся данных можно предположить, что как Е2, так и Е4 отличаются от нормального белка Е3 большей подвижностью липидсвязывающего сайта, но для Е4 характерна также пониженная стабильность структуры, особенно в области этого сайта. Эту проблему не удалось решить даже с помощью алгоритма AlphaFold — предсказанная им структура отличается от гипотетических структур, выдвинутых на основе данный спектроскопии кругового дихроизма или ЯМР.
Информация о докладчиках
Москалев Алексей Александрович, член-корреспондент РАН, Институт долголетия с клиникой превентивной медицины РНЦХ им. акад. Б.В. Петровского, Москва
Vittorio Calabrese, MD, University of Catania, University of Messina, Italy
Митькевич Владимир Александрович, чл.-корр., д.б.н., ФГБУН Институт молекулярной биологии им. В. А. Энгельгардта РАН, Москва
Каштанова Дарья Андреевна, ФГБУ «ЦСП» ФМБА России, Москва
Иванченко Михаил Васильевич, д. ф.-м. н., доцент, НИИ биологии старения. Нижегородский государственный университет им. Н.И. Лобачевского,
Спивак Ирина Михайловна, к.б.н., доцент, НИЦ Военно-медицинской академии.
Мамчур Александра Александровна, ФГБУ «ЦСП» ФМБА России, Москва


 Меню
Меню





 Все темы
Все темы



 0
0