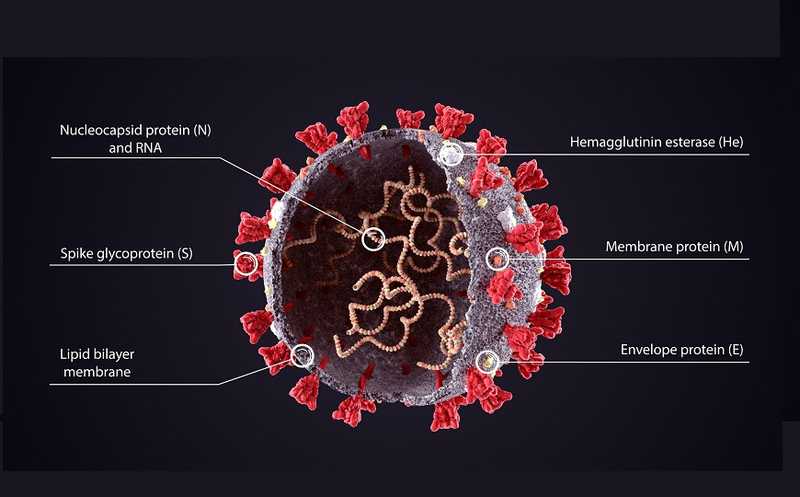
SK Bioscience и GlaxoSmithKline сравнят свою вакцину с препаратом AstraZeneca
Япония приостановила использование вакцины Moderna из-за инородных включений в растворе для инъекций, НМИЦ онкологии им. Н.Н. Петрова начал производство CAR-T продукта, а Минздрав запустит «цифрового двойника» системы здравоохранения. Об этом и многом другом в рубрике «Бизнес-среда».

inkdrop | 123RF.COM
Вакцины/вакцинация
Словакия прекратила вакцинацию «Спутником V»
С 1 сентября Словакия прекратила прививать граждан российской вакциной «Спутник V». Закупленная в марте месяце партия в 200 тысяч ампул была использована лишь частично — вакциной привилось 15 тысяч человек. Оставшиеся дозы были выкуплены Россией обратно. Закупка и использование вакцины, которая на текущий момент так и не зарегистрирована в Евросоюзе, послужили причиной начала политического кризиса в Словакии.
Накануне минздрав Словакии объявил, что 31 августа – последний день, когда жители республики могут получить вторую дозу российской вакцины.
В марте 2021 года ведомство выдало разрешение на использование вакцины Спутник V. Препарат не был зарегистрирован в ЕС. Спустя три месяца в стране стартовала вакцинация российским препаратом. Привился в том числе и глава Минфина Словакии и бывший премьер-министр страны Игор Матович. Решение о закупке вакцины принимал именно он, находясь в должности главы правительства.
Тогда же две партии из коалиции – «За людей» и «Свобода и справедливость» потребовали его отставки. 30 марта Матович ушел в отставку и занял пост министра финансов.
В начале июля минздрав республики заявил, что Россия выкупила у Словакии оставшиеся 160 тыс. неиспользованных доз вакцины «Спутник V» по цене приобретения — $9,95 за дозу. В Российском фонде прямых инвестиций при этом сообщили, что в стране была использована вся закупленная партия.
По мнению представителей РФПИ, против вакцины «Спутник V» в Словакии была развернута информационная кампания, которая являлась частью политической борьбы между различными группами в правительстве.
По данным минздрава Словакии, первую дозу какой-либо вакцины получили 393 402 человека в стране, второй дозой вакцинированы свыше 2,2 млн человек.
Япония приостановила использование вакцины Moderna из-за инородных включений
Во флаконах вакцины против COVID-19 от Moderna, поставленной в Японию, обнаружены инородные включения. В результате приостановлено использование 1.63 млн доз этой вакцины, произведенной в Испании. Дистрибьюцию и продажу вакцины в Японии осуществляет компания Takeda Pharmaceutical.
Черные частицы размером несколько миллиметров были найдены во флаконе с вакциной в префектуре Гумма. Аналогичные включения нашли во флаконе и шприцах в префектуре Окинава, а в другом шприце нашли розовый материал. Информация об инородном веществе в вакцине также поступила из восьми центров вакцинации в пяти префектурах — Айти, Гифу, Ибараки, Сайтама и Токио. Сообщений о каких-либо проблемах со здоровьем у вакцинированных не было.
Эпидемиологическая ситуация в стране сложная, из-за пандемии действует чрезвычайное положение, а 24 августа в стране начались Паралимпийские игры. Префектуры Гумма и Окинава уже возобновили вакцинацию другими препаратами в тех центрах, где произошли инциденты. Moderna сообщила, что проводит расследование.
В Японии одобрены вакцины Pfizer/BioNTech, AstraZeneca и Moderna. На данный момент в стране первую дозу вакцины получили 68,1 млн человек (53,6% населения), а две дозы — 54.1 млн (42,6%).
Вакцину GSK и SK от COVID-19 сравнят с препаратом AstraZeneca
Компании SK Bioscience (SK) и GlaxoSmithKline (GSK) запускают фазу 3 клинического исследования вакцины-кандидата от COVID-19 — GBP510. Показатели безопасности и иммунногенности будут сравниваться не с плацебо, а с результатами вакцины AZD1222 от компании AstraZeneca. В КИ запланировано участие 4 тысяч человек. Результаты должны быть получены в первом полугодии 2022 года.
Антиген кандидатной вакцины был разработан SK в сотрудничестве с Институтом дизайна белков (IPD) Вашингтонского университета, при поддержке Фонда Билла и Мелинды Гейтс и Коалиции за инновации для готовности к эпидемиям (CEPI) в рамках инвестиционного проекта Wave2 по созданию более доступных вакцин против COVID-19.
Вакцина содержит самособирающиеся наночастицы, которые включают рецептор-связывающий домен (RBD) спайк-белка SARS-CoV-2. Ее будут использовать в комбинации с адъювантом AS03 на основе сквалена, разработанным в GSK. Фаза 1-2 КИ уже показала положительные результаты. (О вакцине на сайте IPD.)
В случае успешных КИ планируется использование вакцины по программе Всемирной организации здравоохранения COVAX.
«Сейчас сохраняется потребность в доступных и недорогих вакцинах против COVID-19. Они необходимы, чтобы обеспечить равный доступ к вакцинации во всем мире. Мы рады внести свой вклад в разработку адъюванта GSK для борьбы с пандемией и работать с SK для масштабных поставок вакцины через COVAX, если она будет одобрена», — заявил главный специалист по глобальному здравоохранению GSK Томас Бройер.
ГНЦ «Вектор» зарегистрировал новую вакцину против COVID-19
Государственный научный центр вирусологии и биотехнологии «Вектор» зарегистрировал свою вторую пептидную вакцину от COVID-19 — «ЭпиВакКорона-Н». Вакцина содержит два пептида (в ранее зарегистрированной «ЭпиВакКороне» их три). Срок ее хранения — шесть месяцев при температурном режиме 2-8 °С. Коммерческое название новой вакцины — «AURORA-CoV».
Фаза 1-2 открытого КИ «ЭпиВакКороны-Н» началось в апреле 2021 года. В них принимали участие три группы по 75 человек. Одна группа получала две дозы с интервалом в 21 день, вторая – три дозы (третья вводилась через 60 дней после первой). Третья же группа участников получала зарегистрированную ранее вакцину «ЭпиВакКорона». Результаты данного исследования пока не обнародованы.
В центре «Вектор» заявляли, что новая вакцина позволит упростить процесс производства и быстрее его масштабировать. Производиться «ЭпиВакКорона-Н» будет на мощностях самого центра и компании «Герофарм».
Согласно инструкции, «ЭпиВакКорона-Н» может применяться для иммунизации лиц в возрасте от 18 до 60 лет. Интервал между двумя дозами — не менее 14 дней. Дата окончания действия регистрационного удостоверения — 1 января 2022 года.
«ЭпиВакКорона Н» стала пятой вакциной от COVID-19, зарегистрированной в России, после «Спутника V» и «Спутника Лайт» от НИЦЭМ им. Н.Ф. Гамалеи, «ЭпиВакКороны» и «КовиВака» от ФНЦИРИП им. М.П. Чумакова РАН.
Новые препараты
«Аденовейт» от Takeda против гемофилии А зарегистрирован в России
Фармацевтическая компания Takeda получила российское регистрационное удостоверение на препарат «Аденовейт» (руриоктоког альфа пэгол). Лекарство применяется для терапии гемофилии A. Препарат одобрен к применению в Евросоюзе, США, Канаде, Швейцарии, Исландии, Норвегии и других странах.
Препарат был одобрен Управлением по контролю продуктов и лекарств США (FDA) еще осенью 2015 года для терапии гемофилии A у детей от 12 лет и взрослых. В 2018 году «Аденовейт» рекомендован к применению у детей до 12 лет в Канаде. В том же году одобрило препарат и Европейское агентство лекарственных средств.
В российский перечень «14 высокозатратных нозологий» на 2021 год для терапии гемофилии включены эмицизумаб («Гемлибра» от Roche) и симоктоког альфа («Нувик» от Octapharma).
Гемофилия А — это заболевание, вызванное врожденным отсутствием фактора свертывания VIII. «Аденовейт» представляет собой рекомбинантный фактор свертывания крови VIII с длительным периодом полувыведения.
Центр онкологии им. Н.Н. Петрова начал производство CAR-T продукта
Национальный центр онкологии им. Н.Н. Петрова запустил в тестовом режиме производство CAR-T продукта (Т-клеток с химерными рецепторами антигена), применяемого в онкогематологии. Центр также планирует лицензировать собственную лабораторию в соответствии с требованиями законодательства о биомедицинских клеточных продуктах (БМКП), чтобы лечить до трех пациентов в месяц.
Тестовое производство CAR-T-продуктов началось на базе лаборатории НМИЦ им. Н.Н. Петрова в июне, сообщает Vademecum, но лечение пока не проводилось. Мощности лаборатории позволяют производить до трех таких продуктов в месяц. Заявку на лицензирование производства планируется подать в июне 2022 года.
Сейчас центр использует для модификации T-клеток вирусный вектор немецкой компании Miltenyi Biotec. Однако в дальнейшем планируется разработать собственный вектор.
В настоящий момент в мире одобрены к применению четыре коммерческих CAR-T-продукта: Tecartus и Yescarta от компании Gilead Sciences, Kymriah производства Novartis, Abecma от BMS.
В 2022 году Novartis рассчитывает зарегистрировать по правилам ЕАЭС свой CAR-T-продукт Kymriah. Это позволит начать его реализацию на территории России. Цена терапии — 475 тысяч долларов. В НМИЦ им. Н.Н. Петрова рассчитывают, что стоимость разработанной ими CAR-T-терапии будет намного дешевле.
Roche и ShapeTX разработают генную терапию для лечения болезни Альцгеймера
Биотехнологическая компания Shape Therapeutics (ShapeTX), разрабатывающая мРНК-технологии для генной терапии, заключила соглашение с компанией Roche. Компании планируют совместно развивать генную терапию для лечения болезней Альцгеймера, Паркинсона и ряда редких заболеваний.
В разработке будут использоваться платформа ShapeTX — RNAfix для редактирования РНК,а также, возможно, AAVid для создания тканеспецифических капсидов аденоассоциированных вирусов. ShapeTX проведет доклинические исследования новых методик лечения заболеваний, обнаруженных с помощью ее платформ. Roche отвечает за разработку и коммерциализацию препаратов, созданных в сотрудничестве.
ShapeTX имеет право на получение первоначальной выплаты и платежей за разработку и продажу препаратов. Общая сумма выплат может превысить 3 млрд долларов. Кроме того, компания имеет право на многоуровневые лицензионные платежи за продажи потенциальных продуктов, созданных совместно Roche.
Регуляторика
Минздрав представил новую редакцию рекомендаций по вакцинации от COVID-19
Министерство здравоохранения России рекомендует медучреждениям начать индивидуальную работу с пациентами старше 60 лет по профилактике COVID-19 и напоминает, что вакцина «Спутник Лайт» с августа разрешена для ревакцинации этой категории граждан. Каким образом необходимо выстроить индивидуальную работу, в документе не уточняется.
Также добавлен раздел о вакцинации пациентов с ВИЧ-инфекцией. Ведомство отмечает, что вакцина «Спутник V» рекомендуется для профилактики COVID-19 пациентам с ВИЧ-инфекцией, если они получают АРВ-терапию минимум четыре недели. Использовать вакцину Минздрав рекомендует вне зависимости от уровня иммунного статуса, схем АРВ-терапии и вирусной нагрузки.
Проблему с доступом пациентам с ВИЧ-инфекцией к вакцинации от COVID-19 поднимал комитет по здравоохранению Санкт-Петербурга. Комитет даже выпускал разъяснения, из которых следовало, что врач при обращении ВИЧ-инфицированного в пункт вакцинации должен выяснить, получает ли тот АРВ-терапию, подавлена ли у него виремия и каково количество CD4-лимфоцитов.
Первая версия рекомендаций Минздрава по вакцинации против COVID-19 была опубликована в конце июня 2021 года. Там впервые была прописана периодичность вакцинации — раз в полгода, пока уровень коллективного иммунитета не достигнет 60%, а затем раз в год.
На программу «14 высокозатратных нозологий» просят выделить дополнительно 20 млрд рублей
Общественная палата России сформировала и направила главе Правительства рекомендации по решению дефицита препаратов по госпрограмме «14 ВЗН». Эксперты предлагают выделить дополнительное финансирование на текущий год в размере 20 млрд рублей.
Недостаточную обеспеченность пациентов лекарствами по программе «14 ВЗН» представители пациентских организаций поднимали еще в марте 2021 года.
«Уже в третьем квартале текущего года ожидается дефицит лекарственных препаратов, закупаемых отдельным категориям пациентов, входящих в федеральный перечень “Программа “14 ВЗН”. Пока непонятно, что правительство и, в частности, Минздрав планируют предпринять, поскольку недофинансирование программы налицо», - сообщила профильному изданию «Фармацевтический вестник» зампред комиссии Общественной палаты по социальной политике Екатерина Курбангалеева.
Общественная палата предлагает запретить ежемесячные замены лекарственных препаратов аналогами и одновременный прием медикаментов, выпущенных разными производителями.
Ранее с предложением дофинансировать программу выступал Всероссийский союз пациентов. При этом заместитель министра здравоохранения Сергей Глаголев сообщал, что объем заявок на закупку препаратов по программе ВЗН уже превышает ее бюджет.
По мнению членов союза пациентов, серьезным препятствием для расширения программы инновационными препаратами стали и установленные государством правила формирования перечня лекарств.
Комиссия по формированию лекарственных перечней Минздрава отклонила заявки на включение в программу аклабрутиниба, венетоклакса, нилотиниба, пембролизумаба, ибрутиниба, сипонимода.
Минздрав начинает масштабную модернизацию первичного звена здравоохранения
Минздрав России планирует масштабную модернизацию первичного звена здравоохранения. Министр здравоохранения Михаил Мурашко сказал, что в рамках проекта будет создан «цифровой двойник системы здравоохранения». Реализация данного проекта должна напрямую повлиять на взаимодействие пациентов и медработников, а также потребует модернизации инфраструктуры.
Проект будет реализован на нескольких уровнях: потребуется модернизация инфраструктурных процессов — закупка транспорта, обновление медоборудования. Состояние пациента и другие данные будут вноситься в его цифровой профиль. Это, согласно задумке ведомства, позволит создавать программы профилактики и сопровождения.
«Мы формируем аналитический блок, который позволяет уйти врачу от рутины. Система будет подсказывать и предлагать врачу алгоритмы, необходимые для максимального сохранения здоровья, продления жизни, сопровождения пациента», — пояснил Мурашко.
Программа позволит вносить все данные о вакцинации пациента и получение им необходимых справок в один ресурс. Ее общий бюджет — более 500 млрд рублей. Программа, рассчитанная до 2025 года, стартовала в текущем году. Запланировано строительство и реконструкция более 5,5 тыс. медучреждений, а также приобретение более 20 тысяч единиц автотранспорта и более 97 тысяч единиц медицинского оборудования.


 Меню
Меню





 Все темы
Все темы




 0
0