Биофабрика противораковых препаратов с доставкой в опухоль
Ученые создали бактерию, экспрессирующую ингибиторы контрольных точек иммунного ответа и колонизирующую опухоли. Единичная инъекция мышам бактерий, производящих антитела, оказалась эффективнее введения самих антител.
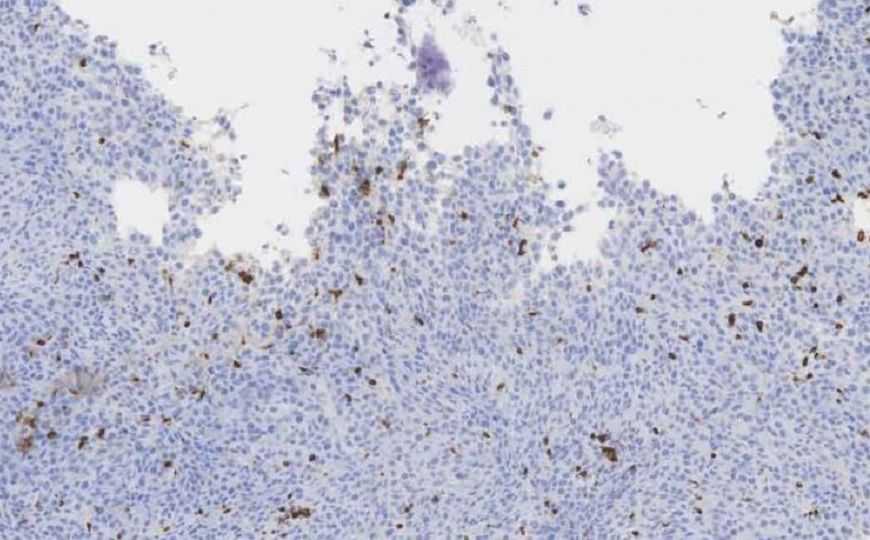
Т-клетки в ткани колоректальной опухоли
Credit: Piper Treuting/University of Washington
Ученые создали бактериальную «биофабрику», которая способна синтезировать ингибиторы контрольных точек иммунного ответа и высвобождать их непосредственно в опухолях без побочных эффектов для других органов. Исследователи, опубликовавшие статью в журнале Science Translational Medicine, продемонстрировали эффективность терапии на лимфомах и колоректальных опухолях у мышей.
Терапия ингибиторами контрольных точек иммунного ответа (ИКТ) нацелена на такие белки, как PD-L1 и CTLA-4, активация которых в иммунных Т-клетках не позволяет им бороться с раковыми опухолями. Несмотря на перспективность такого подхода к лечению, ингибиторы контрольных точек очень ограниченно применяются в клинической практике из-за их профиля безопасности: при системном введении они очень токсичны и вызывают серьезные побочные эффекты у 70% пациентов, и это особенно критично при введении комбинации препаратов. (О терапии блокадой ИКТ читайте и смотрите лекцию Нобелевского лауреата Джеймса Эллисона.)
Чтобы повысить безопасность лекарства, ученые из Колумбийского университета в Нью-Йорке и их коллеги придумали, как ограничить место действия ИКТ только пораженными раком тканями. Они воспользовались тем фактом, что микробы легко могут колонизировать опухоли, и разработали специальный штамм бактерии E.coli, который способен непрерывно производить и высвобождать фрагменты антител, нацеленных на PD-L1 и CTLA-4 непосредственно в опухоли. Ученые максимизировали терапевтический эффект бактерии, создав регуляторный контур, обеспечивающий синхронный лизис бактерий при достижении критической плотности популяции. Помимо синхронного выделения терапевтических антител, такой конструкт гарантирует контроль над ростом популяции бактерий. (Подробнее о схеме синхронного лизиса, основанного на чувстве кворума бактерий, читайте в нашем материале о другой работе этой же группы исследователей.)
Однократная инъекция таких бактерий мышам внутрь лимфомы или колоректальной раковой опухоли более эффективно уменьшала размер опухоли, чем традиционная терапия комбинацией анти-PD-L1 и анти-CTLA-4 препаратов. Гистологический анализ показал, что бактерии успешно колонизировали опухоли и продолжали выделять нанотела в организме грызунов в течение двух недель, не распространяясь при этом на близлежащие органы и ткани.
Этот способ терапии помог избежать побочных эффектов, таких как потеря веса. Авторы сообщают также, что организмы тех животных, у которых опухоль была полностью ликвидирована в результате терапии, избавлялись также и от привнесенных бактерий. Этот эффект они связывают с тем, что исчезал специфический субстрат колонизации — опухолевые клетки.
Источник
Gurbatri, C. R., et al. // Engineered probiotics for local tumor delivery of checkpoint blockade nanobodies // Sci. Transl. Med. 12, eaax0876 (2020); DOI: 10.1126/scitranslmed.aax0876


 Меню
Меню





 Все темы
Все темы




 0
0